名校
1 . 下列有关 的说法中不正确的是
的说法中不正确的是
 的说法中不正确的是
的说法中不正确的是A.3.9g  与足量的 与足量的 充分反应,转移电子数目为0.1 充分反应,转移电子数目为0.1 |
B.3.1g  在足量 在足量 中充分燃烧,生成 中充分燃烧,生成 的数目为0.1 的数目为0.1 |
C.7g DTO(水)含有的中子数约为3.67 |
D.已知: ,向1L 0.1mol/L ,向1L 0.1mol/L  溶液中加入足量KClO固体,溶液中 溶液中加入足量KClO固体,溶液中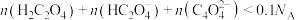 |
您最近一年使用:0次
2024-06-03更新
|
57次组卷
|
2卷引用:2024年江西省宜春市第一中学高三下学期第三次模拟考试化学试卷
2 . 常温下,分别向MnCl2、ZnCl2、CH3COOH溶液中滴加NaOH溶液,溶液pX[pX=-lgc(X),X代表Mn2+、Zn2+、OH-, ]与pH关系如图所示。已知:Ksp[Mn(OH)2]>Ksp[Zn(OH)2]。下列叙述正确的是
]与pH关系如图所示。已知:Ksp[Mn(OH)2]>Ksp[Zn(OH)2]。下列叙述正确的是
 ]与pH关系如图所示。已知:Ksp[Mn(OH)2]>Ksp[Zn(OH)2]。下列叙述正确的是
]与pH关系如图所示。已知:Ksp[Mn(OH)2]>Ksp[Zn(OH)2]。下列叙述正确的是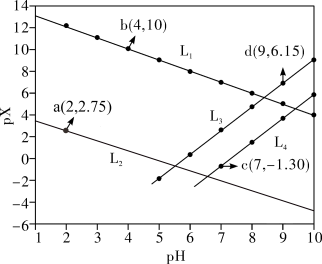
A.图中L2代表 ,L3代表Mn2+ ,L3代表Mn2+ |
| B.室温下,Ksp[Zn(OH)2]的数量级为10-13 |
C.同时产生两种沉淀时,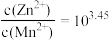 |
D.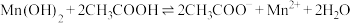 的平衡常数K=105.8 的平衡常数K=105.8 |
您最近一年使用:0次
2024-06-02更新
|
108次组卷
|
4卷引用:江西省部分重点中学2024届高三下学期第二次联考化学试题
3 . 已知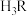 是二元弱酸,常温下向其溶液中加入NaOH调节溶液的pH,测得溶液中含R微粒的物质的量分数(
是二元弱酸,常温下向其溶液中加入NaOH调节溶液的pH,测得溶液中含R微粒的物质的量分数( )与溶液pH的关系如图所示,下列说法中错误的是
)与溶液pH的关系如图所示,下列说法中错误的是
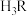 是二元弱酸,常温下向其溶液中加入NaOH调节溶液的pH,测得溶液中含R微粒的物质的量分数(
是二元弱酸,常温下向其溶液中加入NaOH调节溶液的pH,测得溶液中含R微粒的物质的量分数( )与溶液pH的关系如图所示,下列说法中错误的是
)与溶液pH的关系如图所示,下列说法中错误的是
A.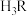 溶液中, 溶液中, |
B.常温下, 的数量级为 的数量级为 |
C.b点溶液中, |
D.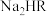 溶液中, 溶液中, |
您最近一年使用:0次
4 . 室温下,向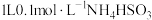 溶液中加入
溶液中加入 固体,溶液中
固体,溶液中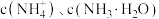 、
、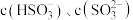 随
随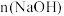 的变化如下图所示(忽略该过程中溶液体积和温度的变化)。已知:室温时,
的变化如下图所示(忽略该过程中溶液体积和温度的变化)。已知:室温时,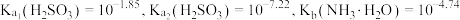 。下列说法不正确的是
。下列说法不正确的是
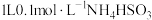 溶液中加入
溶液中加入 固体,溶液中
固体,溶液中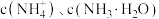 、
、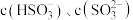 随
随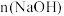 的变化如下图所示(忽略该过程中溶液体积和温度的变化)。已知:室温时,
的变化如下图所示(忽略该过程中溶液体积和温度的变化)。已知:室温时,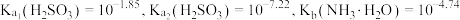 。下列说法不正确的是
。下列说法不正确的是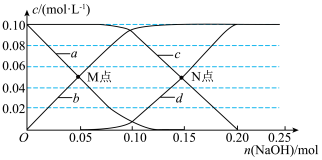
A.曲线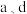 分别代表 分别代表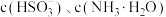 的变化 的变化 |
B.随 的加入, 的加入,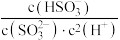 的值不断减小 的值不断减小 |
C.M点存在: |
D.N点时,溶液的 为9.26 为9.26 |
您最近一年使用:0次
2024-04-07更新
|
348次组卷
|
3卷引用:江西省南昌市2024届高三下学期第三次模拟测试化学试题
5 . 人体血液存在H2CO3/ ,
, /
/ 等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值lgx [x表示
等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值lgx [x表示 或
或 ]与pH的关系如图所示。已知碳酸pKa1=6.4、磷酸pKa2=7.2 (pKa=-lgKa)。则下列说法错误的是
]与pH的关系如图所示。已知碳酸pKa1=6.4、磷酸pKa2=7.2 (pKa=-lgKa)。则下列说法错误的是

 ,
, /
/ 等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值lgx [x表示
等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值lgx [x表示 或
或 ]与pH的关系如图所示。已知碳酸pKa1=6.4、磷酸pKa2=7.2 (pKa=-lgKa)。则下列说法错误的是
]与pH的关系如图所示。已知碳酸pKa1=6.4、磷酸pKa2=7.2 (pKa=-lgKa)。则下列说法错误的是
A.曲线I表示lg 与pH的变化关系 与pH的变化关系 |
| B.a→b的过程中,水的电离程度逐渐增大 |
C.当pH增大时, 逐渐减小 逐渐减小 |
D.当c(H2CO3) =c( ) 时,c( ) 时,c( ) <c( ) <c( ) ) |
您最近一年使用:0次
解题方法
6 . 综合利用炼锌矿渣[主要含铁酸镓Ga2(Fe2O4)3、铁酸锌ZnFe2O4]获得3种金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如下:
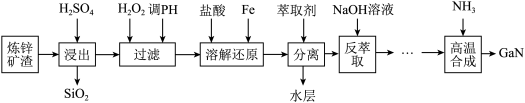
已知:常温下,浸出液中各离子形成氢氧化物沉淀的pH和金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见表。
请回答:
(1)写出铁酸锌(ZnFe2O4) 中铁元素的化合价_______ 。
(2)Ga位于周期表IIIA族,性质与Al相似,反萃取后水溶液中镓元素以_______ (用化学式表示)存在。
(3)处理浸出液时,调节pH至5.4的目的是_______ 。
(4)加入铁的原因为_______ 。
(5)写出“高温合成”操作中Ga(CH3)3与NH3反应生成GaN的化学方程式_______ 。
(6)利用炼锌矿矿渣所获得的三种金属盐,分别为镓盐、_______ 和_______ 。(用化学式表示)
(7)取一定量GaN样品溶于足量的热NaOH溶液中,用H3BO3溶液将产生的NH3完全吸收,用标准浓度的盐酸滴定,通过消耗盐酸的体积,可测定样品的纯度。已知:NH3+ H3BO3= NH3·H3BO3;NH3·H3BO3 +HCl= NH4Cl+H3BO3,硼酸的Ka=10-9.24,从滴定角度分析可用过量H3BO3溶液吸收NH3的可能原因是_______ 。

已知:常温下,浸出液中各离子形成氢氧化物沉淀的pH和金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见表。
| 金属离子 | Fe2+ | Fe3+ | Zn2+ | Ga3+ |
| 开始沉淀pH | 8.0 | 1.7 | 5.5 | 3.0 |
| 沉淀完全pH | 9.6 | 3.2 | 8.0 | 4.9 |
| 萃取率(%) | 0 | 99 | 0 | 97~98.5 |
(1)写出铁酸锌(ZnFe2O4) 中铁元素的化合价
(2)Ga位于周期表IIIA族,性质与Al相似,反萃取后水溶液中镓元素以
(3)处理浸出液时,调节pH至5.4的目的是
(4)加入铁的原因为
(5)写出“高温合成”操作中Ga(CH3)3与NH3反应生成GaN的化学方程式
(6)利用炼锌矿矿渣所获得的三种金属盐,分别为镓盐、
(7)取一定量GaN样品溶于足量的热NaOH溶液中,用H3BO3溶液将产生的NH3完全吸收,用标准浓度的盐酸滴定,通过消耗盐酸的体积,可测定样品的纯度。已知:NH3+ H3BO3= NH3·H3BO3;NH3·H3BO3 +HCl= NH4Cl+H3BO3,硼酸的Ka=10-9.24,从滴定角度分析可用过量H3BO3溶液吸收NH3的可能原因是
您最近一年使用:0次
7 . 下列实验操作、现象和结论或解释均正确的
| 选项 | 实验操作 | 实验现象 | 结论或解释 |
| A | 将Na2O2与SO2反应后的固体物质加水溶解后,先加足量的稀硝酸,再滴加BaCl2溶液 | 产生白色沉淀 | 说明Na2O2与SO2反应后生成了Na2SO4 |
| B | 铜丝和浓硫酸加热一段时间后冷却,向反应后的溶液中加水稀释 | 溶液呈蓝色 | 说明反应生成了硫酸铜 |
| C | 向无水乙醇中加入浓硫酸,加热至170°C,将产生的气体通入酸性KMnO4溶液中 | 紫红色褪去 | 乙醇发生消去反应生成乙烯 |
| D | 向Na2S溶液中通入足量CO2,然后再将产生的气体导入CuSO4溶液中 | CuSO4溶液中产生黑色沉淀 | Kal(H2CO3)>Kal(H2S) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-03-11更新
|
580次组卷
|
3卷引用:江西省上饶市2023届高三第一次高考模拟考试理综化学试题
名校
解题方法
8 . 常温下,用0.1000 mol/L的盐酸滴定20.00 mL未知浓度的一元碱BOH溶液。溶液中,pH、B+的分布系数δ随滴加盐酸体积VHCl的变化关系如图所示。已知B+的分布系数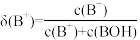 。下列叙述正确的是
。下列叙述正确的是

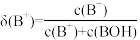 。下列叙述正确的是
。下列叙述正确的是
| A.BOH的电离常数Kb=1.0× 10-6 |
| B.滴定时,可以选择甲基橙作指示剂 |
| C.滴定过程中,水的电离程度: n<m<p |
| D.n点溶液中,粒子浓度大小为c(Cl-)>c(B+)> c(BOH) |
您最近一年使用:0次
2023-03-08更新
|
484次组卷
|
3卷引用:江西省南昌市2023届高三一模理综化学试题
江西省南昌市2023届高三一模理综化学试题(已下线)广东省广州市天河区2023届高三二模化学试题变式题(选择题11-16)四川省宜宾市叙州区第一中学校2023-2024学年高三上学期开学考试理综化学试题
名校
解题方法
9 . 室温,向 和
和 的混合溶液中逐滴加入
的混合溶液中逐滴加入 溶液,溶液中
溶液,溶液中 与
与 的变化关系如图所示。下列说法正确的是
的变化关系如图所示。下列说法正确的是
(已知: 的
的 、
、 分别为
分别为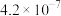 、
、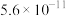 ;
;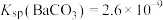 )
)

 和
和 的混合溶液中逐滴加入
的混合溶液中逐滴加入 溶液,溶液中
溶液,溶液中 与
与 的变化关系如图所示。下列说法正确的是
的变化关系如图所示。下列说法正确的是(已知:
 的
的 、
、 分别为
分别为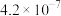 、
、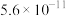 ;
;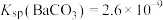 )
)
| A.a对应溶液的pH小于b |
B.b对应溶液的 |
C.a→b变化过程中,溶液中的 减小 减小 |
D.a对应的溶液中一定存在: |
您最近一年使用:0次
2023-03-05更新
|
782次组卷
|
3卷引用:江西省景德镇市2023届高三下学期第二次综合模拟考试理综化学试题
10 . 某元素M的氢氧化物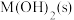 在水中的溶解反应为:
在水中的溶解反应为: 、
、 ,
, 与
与 的关系如图所示,c为
的关系如图所示,c为 或
或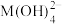 浓度的值,下列说法
浓度的值,下列说法错误 的是

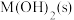 在水中的溶解反应为:
在水中的溶解反应为: 、
、 ,
, 与
与 的关系如图所示,c为
的关系如图所示,c为 或
或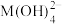 浓度的值,下列说法
浓度的值,下列说法
A.曲线②代表 与 与 的关系 的关系 |
B.向 的 的 溶液中加水稀释,平衡: 溶液中加水稀释,平衡: 逆向移动, 逆向移动,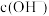 增大 增大 |
C. 的 的 约为 约为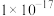 |
D. 时,溶液中的 时,溶液中的 |
您最近一年使用:0次
2023-01-14更新
|
953次组卷
|
4卷引用:江西省上饶市2023届高三第一次高考模拟考试理综化学试题



