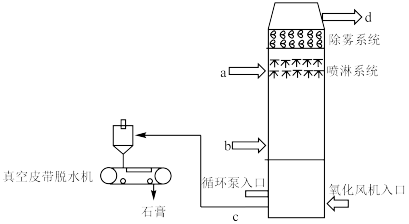
1 . 下图是石灰石膏法脱硫的示意图。烟气在脱硫塔内与脱硫剂(石灰石/生石灰浆液)接触混合,继而与鼓入的空气中的氧气发生化学反应,生成石膏(CaSO4·2H2O)。脱硫后的烟气经过除雾器除去雾滴后,排至大气。
1.烟气进口:_____ 。(填a或b)
2.为避免操作不当引起的中间产物CaSO3结垢和堵塞现象,某公司在脱硫剂中加入少量甲酸,效果很好。写出少量甲酸和CaSO3反应的化学方程式:_____ 。
| HCOOH | Ka=1.80×10-4 | |
| H2SO3 | Ka1=1.2×10-2 | Ka2=6.2×10-8 |
| H2CO3 | Ka1=4.2×10-7 | Ka2=4.8×10-11 |
1.烟气进口:
2.为避免操作不当引起的中间产物CaSO3结垢和堵塞现象,某公司在脱硫剂中加入少量甲酸,效果很好。写出少量甲酸和CaSO3反应的化学方程式:
您最近一年使用:0次
解题方法
2 . 油气开采、石油化工、煤化工等行业废气中普遍含有硫化氢,需要回收处理并加以利用。
I.已知下列反应的热化学方程式:
①2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ∆H1
②4H2S(g)+2SO2(g)=3S2(g)+4H2O(g) ∆H2
③2H2(g)+O2(g)=2H2O(g) ∆H3
④2H2S(g)=S2(g)+2H2(g) ∆H4
(1)∆H4=
(2)已知∆H4>0,
A.低温 B.高温
(3)处理H2S普遍采用的方法是克劳斯工艺,即利用反应①和②生成S2;另一种方法是利用反应④分解H2S。相比克劳斯工艺,分解法的优点是
II.在1373K、100 kPa下,分别将n(H2S):n(Ar)为4:1、1:1、1:4、1:9的H2S-Ar混合气体置于密闭容器中发生反应④,反应过程中H2S转化率随时间的变化如下图所示:
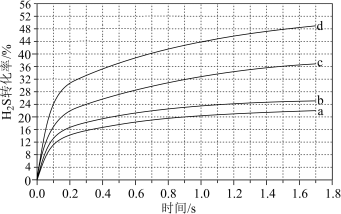
(4)n(H2S):n(Ar)=1:9对应图中曲线
A.a B.b C.c D.d
(5)n(H2S):n(Ar)=1:4的混合气体投料后,若将温度升高至1473K,达到平衡时混合气体中H2S与H2的分压相等,H2S平衡转化率为
III.在真空克劳斯法脱硫中,用K2CO3溶液吸收H2S。
电离平衡常数 | H2CO3 | H2S |
K1 | 4.2×10-7 | 5.6×10-8 |
K2 | 5.6×10-11 | 1.2×10-15 |
(6)下列关于K2CO3溶液中微粒关系正确的是___________。
A.c(OH-)>c(HCO ) ) | B.c(H+)>c(HCO ) ) |
C.c(OH-)=c(H+)+c(HCO )+2c(H2CO3) )+2c(H2CO3) | D.2c(K+)=c(CO )+c(HCO )+c(HCO )+c(H2CO3) )+c(H2CO3) |
(7)K2CO3溶液吸收少量H2S的离子方程式为
您最近一年使用:0次
解题方法
3 . 资源化利用二氧化硫,一方面能保护环境,另一方面能提高经济效益,具有深远意义。
(1)下列生产、生活活动中,不易产生 的是___________。
的是___________。
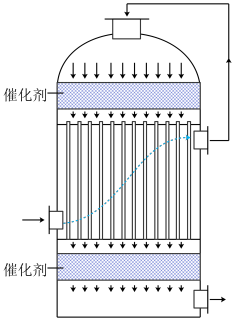
(2)工业中可用含 的冶炼烟气为原料生产硫酸,在如图装置中完成“
的冶炼烟气为原料生产硫酸,在如图装置中完成“ 转化”工序。使用该装置实现了___________。
转化”工序。使用该装置实现了___________。
(3)研究 的性质有利于探索其资源化利用。下列实验方案设计正确的是
的性质有利于探索其资源化利用。下列实验方案设计正确的是___________ 。
钠碱法的启动吸收剂为 溶液,捕捉
溶液,捕捉 后生成
后生成 和
和 的混合液。
的混合液。
(4)常温下进行“钠碱法”的模拟实验。用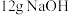 固体配成一定浓度的溶液,这些
固体配成一定浓度的溶液,这些 理论上最多可吸收
理论上最多可吸收 的体积约为
的体积约为___________ L(折算成标准状况)。若实验时只吸收了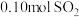 ,则反应后的吸收液中,所含阴离子的浓度由大到小的顺序为
,则反应后的吸收液中,所含阴离子的浓度由大到小的顺序为___________ 。
(5)当钠碱法的吸收液 达到4~6时,混合液中含较多量
达到4~6时,混合液中含较多量 。加热该溶液可回收得到较高纯度的
。加热该溶液可回收得到较高纯度的 ,剩余溶液可循环使用,进一步吸收
,剩余溶液可循环使用,进一步吸收 ,剩余溶液的主要溶质是
,剩余溶液的主要溶质是________ (填写化学式)。
(6)将 通入
通入 溶液时,得到一组
溶液时,得到一组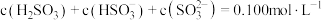 的混合溶液,溶液中部分微粒的物质的量浓度随
的混合溶液,溶液中部分微粒的物质的量浓度随 的关系曲线如下图所示。
的关系曲线如下图所示。
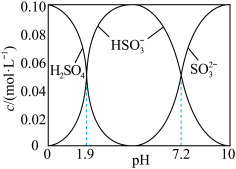
若溶液的 ,溶液中
,溶液中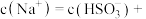
___________ ,此时溶液中
___________  。(选填“
。(选填“ ”“
”“ ”或“
”或“ ”)
”)
(7)上述混合液中存在多个水解平衡,与化学平衡一样,水解平衡也有自己的平衡常数( )。以醋酸钠(
)。以醋酸钠( )为例,其水解平衡常数存在以下定量关系:
)为例,其水解平衡常数存在以下定量关系: (
( 为水的离子积常数,
为水的离子积常数, 为
为 的电离常数)亚硫酸为二元弱酸,
的电离常数)亚硫酸为二元弱酸, 时,其电离常数
时,其电离常数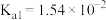 ,
,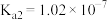 。请结合相关数据说明
。请结合相关数据说明 溶液呈酸性的理由。
溶液呈酸性的理由。___________
(8)“钙碱法”的工作原理与“钠碱法”相似,一般选择消石灰的悬浊液为 吸收剂。请对照“钠碱法”,尝试通过比较反应物和生成物的不同性质,从生产成本和设备维护两方面对“钙碱法”做出评价
吸收剂。请对照“钠碱法”,尝试通过比较反应物和生成物的不同性质,从生产成本和设备维护两方面对“钙碱法”做出评价_____ 。
(1)下列生产、生活活动中,不易产生
 的是___________。
的是___________。| A.燃放鞭炮 | B.火力发电 | C.火山爆发 | D.海水晒盐 |
(2)工业中可用含
 的冶炼烟气为原料生产硫酸,在如图装置中完成“
的冶炼烟气为原料生产硫酸,在如图装置中完成“ 转化”工序。使用该装置实现了___________。
转化”工序。使用该装置实现了___________。
| A.充分利用热能 | B.防止形成酸雾 | C.加速转化 | D.获取纯净 |
(3)研究
 的性质有利于探索其资源化利用。下列实验方案设计正确的是
的性质有利于探索其资源化利用。下列实验方案设计正确的是 |  |  |  |
A.制取 | B.收集 | C.验证 水溶液的酸性 水溶液的酸性 | D.验证 的还原性 的还原性 |
钠碱法的启动吸收剂为
 溶液,捕捉
溶液,捕捉 后生成
后生成 和
和 的混合液。
的混合液。(4)常温下进行“钠碱法”的模拟实验。用
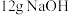 固体配成一定浓度的溶液,这些
固体配成一定浓度的溶液,这些 理论上最多可吸收
理论上最多可吸收 的体积约为
的体积约为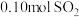 ,则反应后的吸收液中,所含阴离子的浓度由大到小的顺序为
,则反应后的吸收液中,所含阴离子的浓度由大到小的顺序为(5)当钠碱法的吸收液
 达到4~6时,混合液中含较多量
达到4~6时,混合液中含较多量 。加热该溶液可回收得到较高纯度的
。加热该溶液可回收得到较高纯度的 ,剩余溶液可循环使用,进一步吸收
,剩余溶液可循环使用,进一步吸收 ,剩余溶液的主要溶质是
,剩余溶液的主要溶质是(6)将
 通入
通入 溶液时,得到一组
溶液时,得到一组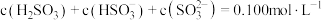 的混合溶液,溶液中部分微粒的物质的量浓度随
的混合溶液,溶液中部分微粒的物质的量浓度随 的关系曲线如下图所示。
的关系曲线如下图所示。
若溶液的
 ,溶液中
,溶液中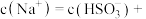

 。(选填“
。(选填“ ”“
”“ ”或“
”或“ ”)
”)(7)上述混合液中存在多个水解平衡,与化学平衡一样,水解平衡也有自己的平衡常数(
 )。以醋酸钠(
)。以醋酸钠( )为例,其水解平衡常数存在以下定量关系:
)为例,其水解平衡常数存在以下定量关系: (
( 为水的离子积常数,
为水的离子积常数, 为
为 的电离常数)亚硫酸为二元弱酸,
的电离常数)亚硫酸为二元弱酸, 时,其电离常数
时,其电离常数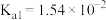 ,
,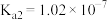 。请结合相关数据说明
。请结合相关数据说明 溶液呈酸性的理由。
溶液呈酸性的理由。(8)“钙碱法”的工作原理与“钠碱法”相似,一般选择消石灰的悬浊液为
 吸收剂。请对照“钠碱法”,尝试通过比较反应物和生成物的不同性质,从生产成本和设备维护两方面对“钙碱法”做出评价
吸收剂。请对照“钠碱法”,尝试通过比较反应物和生成物的不同性质,从生产成本和设备维护两方面对“钙碱法”做出评价
您最近一年使用:0次
4 . 已知:常温下,HCOOH的酸性强于CH3COOH。现将 pH=3,体积均为V0的两种酸溶液分别加水稀释至体积 V,pH 随lg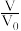 的变化如图所示。下列叙述正确的是
的变化如图所示。下列叙述正确的是

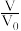 的变化如图所示。下列叙述正确的是
的变化如图所示。下列叙述正确的是
| A.溶液中水的电离程度:a>b>c>d |
| B.a 点的两种酸溶液分别与 NaOH 恰好完全中和后,溶液中n(Na+)相同 |
| C.曲线I表示CH3COOH溶液的变化曲线 |
| D.同温下 pH 相同的 NaOH 溶液、CH3COONa 溶液、HCOONa 溶液、NaHCO3溶液的浓度:c(NaOH)<c(NaHCO3)<c(CH3COONa)<c(HCOONa) |
您最近一年使用:0次
5 .  是一种有毒气体,能溶于水,人们常用
是一种有毒气体,能溶于水,人们常用 溶液除去气体中混有的
溶液除去气体中混有的 杂质,生成黑褐色的CuS沉淀,下列说法正确的是
杂质,生成黑褐色的CuS沉淀,下列说法正确的是
 是一种有毒气体,能溶于水,人们常用
是一种有毒气体,能溶于水,人们常用 溶液除去气体中混有的
溶液除去气体中混有的 杂质,生成黑褐色的CuS沉淀,下列说法正确的是
杂质,生成黑褐色的CuS沉淀,下列说法正确的是A.离子方程式: |
B.溶解或电离出 能力: 能力: |
C.足量 溶液吸收 溶液吸收 可得到 可得到 |
D.稀释 溶液,溶液中的离子浓度都降低 溶液,溶液中的离子浓度都降低 |
您最近一年使用:0次
解题方法
6 . 在 时,将
时,将 氨水以固定速率滴入
氨水以固定速率滴入 盐酸中,溶液
盐酸中,溶液 和温度随加入氨水体积变化如下表所示。下列有关说法正确的是
和温度随加入氨水体积变化如下表所示。下列有关说法正确的是
 时,将
时,将 氨水以固定速率滴入
氨水以固定速率滴入 盐酸中,溶液
盐酸中,溶液 和温度随加入氨水体积变化如下表所示。下列有关说法正确的是
和温度随加入氨水体积变化如下表所示。下列有关说法正确的是| 序号 | ① | ② | ③ | ④ |
加入氨水体积 | 0 | 10.00 | b | 25.00 |
溶液温度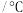 | 25 | 28 | 27 | 25 |
溶液 | 0.0 | a | 7.0 | 9.4 |
A.水的电离程度: |
B.③中 一定等于 一定等于 |
C.②→④溶液温度下降说明 水解过程是吸热的 水解过程是吸热的 |
D.若将盐酸换成等浓度的醋酸,则②的温度将高于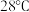 |
您最近一年使用:0次
7 . 某温度下,向浓氯水(由0.12mol氯气溶于水配制而成)中,以恒定速率滴入NaOH溶液,溶液中 和
和 的物质的量与时间t的关系曲线如图:
的物质的量与时间t的关系曲线如图:

下列说法正确的是
 和
和 的物质的量与时间t的关系曲线如图:
的物质的量与时间t的关系曲线如图:
下列说法正确的是
A.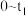 时,溶液中的含氯微粒为: 时,溶液中的含氯微粒为: 、 、 |
B. 时,发生的离子反应是: 时,发生的离子反应是: |
C. 时,溶液中存在如下关系: 时,溶液中存在如下关系: |
D. 时,溶液中含NaCl 0.20mol 时,溶液中含NaCl 0.20mol |
您最近一年使用:0次
8 . 常温时,同浓度的①V1mLCH3COOH溶液 ②V2mLNaOH溶液 ③V3mLCH3COONa溶液,下列结论中正确的是
| A.①与②混合若pH>7,则V2>V1 |
| B.当V2=V3时,溶液中离子种数③>② |
| C.将①稀释10倍,溶液中c(H+)∙c(OH−)增大 |
| D.③溶液中:c(H+)−c(OH−)=c(CH3COO−)−c(CH3COOH) |
您最近一年使用:0次
名校
9 . 已知: ,
, 时,
时, 的
的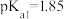 ,
,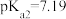 。常温下,用
。常温下,用
 溶液滴定
溶液滴定

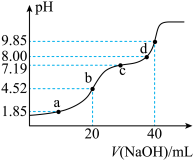
 溶液的滴定曲线如下图所示(曲线上的数字为
溶液的滴定曲线如下图所示(曲线上的数字为 )。下列说法不正确的是
)。下列说法不正确的是
 ,
, 时,
时, 的
的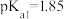 ,
,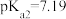 。常温下,用
。常温下,用
 溶液滴定
溶液滴定

 溶液的滴定曲线如下图所示(曲线上的数字为
溶液的滴定曲线如下图所示(曲线上的数字为 )。下列说法不正确的是
)。下列说法不正确的是
A. 点所得溶液中: 点所得溶液中: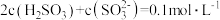 |
B. 点所得溶液中: 点所得溶液中: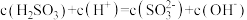 |
C. 点所得溶液中: 点所得溶液中: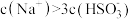 |
D. 点所得溶液中: 点所得溶液中: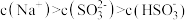 |
您最近一年使用:0次
2021-10-09更新
|
908次组卷
|
16卷引用:上海市奉贤中学2016年高三模拟考试(三模)化学试题
上海市奉贤中学2016年高三模拟考试(三模)化学试题2017届湖北省八校(荆州中学、襄阳五中、襄阳四中等)高三下学期第二次联考理综化学试卷2017届湖北省八校高三第二次联考(3月)理综化学试卷辽宁省沈阳市东北育才学校2017届高三第八次模拟考试理科综合化学试题贵州省铜仁市2020届高三第三次模拟理科综合化学试题2016届江苏省扬州中学高三下3月质检化学试卷2016届福建省厦门一中高三下周考(三)理综化学试卷陕西省西藏民族学院附属中学2017届高三4月月考理科综合化学试题【全国百强校】福建省厦门外国语学校2017-2018学年高二6月月考化学试题【全国百强校】吉林省延边市第二中学2018-2019学年高二下学期开学考试化学试题湖北省麻城市实验高级中学2021-2022学年高二上学期9月月考化学(A卷)试卷(已下线)必考点07 盐类的水解-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)黑龙江省大兴安岭呼玛县高级中学2021-2022学年高二上学期期末考试化学试题(已下线)专题21 电解质溶液图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题11 水溶液中的离子平衡图像(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(已下线)专题四 电解质溶液图象(练)
名校
10 . 水的电离常数如图两条曲线所示,曲线中的点都符合 常数,下列说法错误的是
常数,下列说法错误的是


 常数,下列说法错误的是
常数,下列说法错误的是


A.图中温度 |
B.图中五点 间的关系: 间的关系: |
| C.曲线a、b均代表纯水的电离情况 |
D.若处在B点时,将 的硫酸溶液与 的硫酸溶液与 的KOH溶液等体积混合后,溶液显碱性 的KOH溶液等体积混合后,溶液显碱性 |
您最近一年使用:0次
2020-02-09更新
|
1047次组卷
|
17卷引用:上海市闵行区2015届高三下学期质量调研考试(一模)化学试题
上海市闵行区2015届高三下学期质量调研考试(一模)化学试题夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——水的离子积常数的应用辽宁省铁岭市开原市第二高级中学2020-2021学年高二上学期期初考试化学试题第26讲 水的电离和溶液的pH (精讲)-2021年高考化学一轮复习讲练测贵州省安顺市大洋实验学校2020-2021学年高二上学期期中考试化学试题(已下线)练习10 水的电离和溶液的pH-2020-2021学年【补习教材·寒假作业】高二化学(苏教版)重庆市石柱中学校2020-2021学年高二上学期第二次月考化学试题(已下线)第24讲 水的电离和溶液的pH(精讲)-2022年一轮复习讲练测(已下线)课时40 水的电离与溶液的酸碱性-2022年高考化学一轮复习小题多维练(全国通用)(已下线)3.2.1 溶液的酸碱性(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)甘肃省永昌县第一高级中学2021-2022学年高二上学期期末考试化学试题(已下线)第24讲 水的电离和溶液的pH(讲)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第22讲 水的电离与溶液的pH(练)-2023年高考化学一轮复习讲练测(新教材新高考)四川省宜宾市第四中学校2022-2023学年高二上学期期中考试化学试题内蒙古自治区呼伦贝尔市鄂温克族自治旗第三中学2021-2022学年高二上学期第一次月考化学试题山西省太原市英才学校2021-2022学年高二上学期第二次月考化学试题黑龙江省绥化市绥棱县第一中学2022-2023学年高二上学期期中考试化学试题



