1 . 在20 mL 0.1 mol·L-1的醋酸溶液中,能使溶液的c(H+)增大,而且使醋酸的电离平衡向逆反应方向移动,可加入的试剂是( )
| A.20 mL水 | B.浓盐酸 | C.冰醋酸 | D.NaOH溶液 |
您最近一年使用:0次
名校
解题方法
2 . 能影响水的电离平衡,并使溶液中c(H+)>c(OH-)的操作是( )
| A.向水中投入一小块金属钠 | B.加入NaHCO3固体 |
| C.向水中加入CH3COONa晶体 | D.向水中加入NH4Cl溶液 |
您最近一年使用:0次
2020-01-07更新
|
79次组卷
|
4卷引用:云南省永德县第一中学2019-2020学年高二12月月考化学试题
3 . 已知K2HPO4溶液呈碱性,即HPO42-结合H+的能力大于其电离产生H+的能力。下列操作能使该溶液中c(H3O+)增大的是( )
| A.加水 | B.加热 | C.加消石灰 | D.加K2HPO4 |
您最近一年使用:0次
名校
4 . 下列关于醋酸溶液的说法正确的是
| A.升高温度,溶液中的CH3COOH分子浓度不变 |
| B.室温下,稀释0.1 mol·L-1 CH3COOH溶液,溶液的导电能力增强 |
| C.稀醋酸中加入少量醋酸钠能增大醋酸的电离程度 |
| D.向醋酸溶液中加入少量氢氧化钠固体,能促进醋酸的电离 |
您最近一年使用:0次
2020-02-15更新
|
110次组卷
|
3卷引用:湖北省武汉市武昌区武汉中学2019-2020学年高二上学期化学(人教版选修4)期末复习试题:专题1 弱电解质的电离复习题
解题方法
5 . 稀氨水中存在如下平衡:NH3+H2O  NH3·H2O
NH3·H2O NH4+ + OH-,下列向稀氨水中加入下列物质时的描述错误的是
NH4+ + OH-,下列向稀氨水中加入下列物质时的描述错误的是
 NH3·H2O
NH3·H2O NH4+ + OH-,下列向稀氨水中加入下列物质时的描述错误的是
NH4+ + OH-,下列向稀氨水中加入下列物质时的描述错误的是| A.加入氯化铵固体,平衡逆向移动,溶液pH降低 |
| B.通入更多氨气,平衡正向移动,溶液碱性增强 |
| C.加入氢氧化钠固体,平衡逆向移动,溶液导电性增强 |
| D.加入适量 NaCl溶液,平衡不移动,溶液pH不变 |
您最近一年使用:0次
解题方法
6 . 醋酸溶液中存在电离平衡CH3COOH H++CH3COO-,下列叙述不正确的是( )
H++CH3COO-,下列叙述不正确的是( )
 H++CH3COO-,下列叙述不正确的是( )
H++CH3COO-,下列叙述不正确的是( )| A.0.1 mol·L-1的CH3COOH溶液加水稀释,溶液中c(OH-)增大 |
| B.0.1 mol·L-1的醋酸溶液,由水电离出来的c(H+)=1.0×10-13 mol·L-1 |
| C.CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动 |
| D.常温下,pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7 |
您最近一年使用:0次
7 . 氨水中存在NH3·H2O NH4++OH-,要是此平衡逆向移动且从c(OH-)减小,应加入少量( )
NH4++OH-,要是此平衡逆向移动且从c(OH-)减小,应加入少量( )
 NH4++OH-,要是此平衡逆向移动且从c(OH-)减小,应加入少量( )
NH4++OH-,要是此平衡逆向移动且从c(OH-)减小,应加入少量( )| A.固体氯化铵 | B.稀硫酸 | C.固体氢氧化钠 | D.水 |
您最近一年使用:0次
解题方法
8 . 在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答:
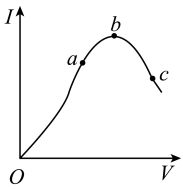
(1)“O”点处冰醋酸的导电能力为0的原因是_______________________ ;
(2)在a、b、c三点处,溶液中c(H+)由小到大的顺序为________ (用字母表示);
(3)在a、b、c三点处,电离程度最大的是________ (用字母表示);
(4)若使c点处的溶液中c(CH3COO-)增大,c(H+)减小,可采取的措施有①_____________ ;②______________ ;③____________ 。

(1)“O”点处冰醋酸的导电能力为0的原因是
(2)在a、b、c三点处,溶液中c(H+)由小到大的顺序为
(3)在a、b、c三点处,电离程度最大的是
(4)若使c点处的溶液中c(CH3COO-)增大,c(H+)减小,可采取的措施有①
您最近一年使用:0次
名校
9 . 醋酸溶液中存在电离平衡 CH3COOH CH3COO- + H+,下列叙述不正确的是
CH3COO- + H+,下列叙述不正确的是
 CH3COO- + H+,下列叙述不正确的是
CH3COO- + H+,下列叙述不正确的是| A.升高温度,平衡正向移动,醋酸的电离常数Ka增大 |
| B.CH3COOH溶液加少量的CH3COONa固体,平衡逆向移动 |
| C.室温下,欲使0.1 mol/L醋酸溶液的电离度α增大,可加入少量冰醋酸 |
| D.0.10 mol/L的CH3COOH 溶液加水稀释,溶液中c(CH3COOH)/c(CH3COO-)减小 |
您最近一年使用:0次
2019-12-07更新
|
228次组卷
|
4卷引用:江西省赣州市2019-2020学年高二上学期期中考试化学试题
10 . 室温下,稀氨水中存在电离平衡NH3•H2O NH4++ OH-,有关叙述正确的是( )
NH4++ OH-,有关叙述正确的是( )
 NH4++ OH-,有关叙述正确的是( )
NH4++ OH-,有关叙述正确的是( )| A.加入氯化铵固体,溶液中c(OH-)增大 | B.加水不断稀释,溶液碱性一定增强 |
| C.加水稀释,平衡常数Kb增大 | D.加入NaOH固体,平衡逆向移动 |
您最近一年使用:0次



