名校
1 . 开发和利用海水资源是当前科学研究的一项重要任务,如图是某化工厂对海水资源综合利用的示意图。下列说法正确的是
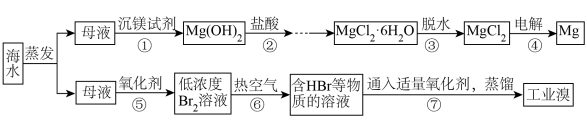

| A.工业生产中步骤①的沉镁试剂为NaOH |
| B.步骤③中氯化镁晶体直接加热脱水可以得到无水氯化镁 |
C.步骤⑥中还需要 的参与 的参与 |
D.实验室中步骤⑦可以通过如图装置完成蒸馏操作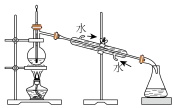 |
您最近一年使用:0次
2023-11-30更新
|
236次组卷
|
2卷引用:辽宁省沈阳市第二中学2023-2024学年高三上学期期中考试化学试题
名校
2 . 化学是一门以实验为基础的学科,如图所示的实验装置或操作能达到实验目的的是
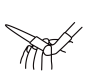 | 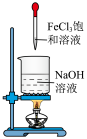 | 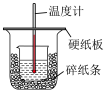 |  |
| A.酸式滴定管排气泡操作 | B.制备Fe(OH)3胶体 | C.中和热的测定 | D.制备无水MgCl2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-20更新
|
799次组卷
|
4卷引用:辽宁省沈阳市东北育才学校高中部2023-2024学年高三上学期第三次模拟考试 化学试题
名校
3 . 摩尔盐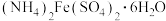 是一种常见的复盐。在空气中比一般的亚铁盐稳定,在工业上常作废水处理的混凝剂。以下是摩尔盐的制备及纯度测定过程。
是一种常见的复盐。在空气中比一般的亚铁盐稳定,在工业上常作废水处理的混凝剂。以下是摩尔盐的制备及纯度测定过程。
【步骤1】铁屑净化。
取1g废铁屑于锥形瓶中,加适量 溶液,小火加热煮沸,一段时间后,倾去碱液,并用蒸馏水洗涤2-3次,干燥备用。
溶液,小火加热煮沸,一段时间后,倾去碱液,并用蒸馏水洗涤2-3次,干燥备用。
【步骤2】制备
在盛有 的
的 稀硫酸的锥形瓶中分次加入干净铁屑,铁屑稍过量,在通风橱中水浴加热,趁热减压抽滤。
稀硫酸的锥形瓶中分次加入干净铁屑,铁屑稍过量,在通风橱中水浴加热,趁热减压抽滤。
【步骤3】制备摩尔盐。
称取适量 并用无氧水制成饱和溶液,加入到盛有硫酸亚铁溶液的蒸发皿中,经过系列操作制得
并用无氧水制成饱和溶液,加入到盛有硫酸亚铁溶液的蒸发皿中,经过系列操作制得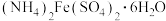 。
。
【步骤4】纯度测定。
请回答相关问题:
(1)“步骤1” 溶液的作用
溶液的作用___________ ,加热的目的___________ ;
(2)“步骤2”铁屑稍过量的目的是___________ ,减压抽滤装置如图所示。和普通过滤相比,抽滤的优点是___________ ;

(3)“步骤3”系列操作为___________ ;
(4) 含量是影响产品品质的关键指标。定量测定方法是:取1.00g产品于烧杯中,加入适量盐酸溶解,并加入3滴KSCN溶液,定容至
含量是影响产品品质的关键指标。定量测定方法是:取1.00g产品于烧杯中,加入适量盐酸溶解,并加入3滴KSCN溶液,定容至 ,取溶液置于比色管中,与标准色阶进行目视比色,确定产品级别。可以根据颜色确定产品级别的原理是
,取溶液置于比色管中,与标准色阶进行目视比色,确定产品级别。可以根据颜色确定产品级别的原理是___________ (用恰当的化学用语及文字说明);
(5)“步骤4”的具体操作如下:
取ag所制得的固体(摩尔盐的摩尔质量为 )于小烧杯中,加入适量稀疏酸,溶解后在
)于小烧杯中,加入适量稀疏酸,溶解后在 容量瓶中定容。取
容量瓶中定容。取 于锥形瓶中,用
于锥形瓶中,用 的
的 ,溶液滴定至终点。终点的现象为
,溶液滴定至终点。终点的现象为___________ 。平行操作三次,消耗 溶液的平均体积为
溶液的平均体积为 。此样品中摩尔盐的含量为
。此样品中摩尔盐的含量为___________ %(用含M、a、c、v等表达式表示,化成最简形式)。导致测定结果偏高的可能原因是___________ 。
A.配溶液定容时俯视刻度线 B.取摩尔盐溶液的滴定管没有润洗
C.取待测液的锥形瓶洗净后未干燥 D.摩尔盐的结晶水数量不足
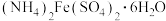 是一种常见的复盐。在空气中比一般的亚铁盐稳定,在工业上常作废水处理的混凝剂。以下是摩尔盐的制备及纯度测定过程。
是一种常见的复盐。在空气中比一般的亚铁盐稳定,在工业上常作废水处理的混凝剂。以下是摩尔盐的制备及纯度测定过程。【步骤1】铁屑净化。
取1g废铁屑于锥形瓶中,加适量
 溶液,小火加热煮沸,一段时间后,倾去碱液,并用蒸馏水洗涤2-3次,干燥备用。
溶液,小火加热煮沸,一段时间后,倾去碱液,并用蒸馏水洗涤2-3次,干燥备用。【步骤2】制备

在盛有
 的
的 稀硫酸的锥形瓶中分次加入干净铁屑,铁屑稍过量,在通风橱中水浴加热,趁热减压抽滤。
稀硫酸的锥形瓶中分次加入干净铁屑,铁屑稍过量,在通风橱中水浴加热,趁热减压抽滤。【步骤3】制备摩尔盐。
称取适量
 并用无氧水制成饱和溶液,加入到盛有硫酸亚铁溶液的蒸发皿中,经过系列操作制得
并用无氧水制成饱和溶液,加入到盛有硫酸亚铁溶液的蒸发皿中,经过系列操作制得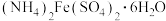 。
。【步骤4】纯度测定。
请回答相关问题:
(1)“步骤1”
 溶液的作用
溶液的作用(2)“步骤2”铁屑稍过量的目的是

(3)“步骤3”系列操作为
(4)
 含量是影响产品品质的关键指标。定量测定方法是:取1.00g产品于烧杯中,加入适量盐酸溶解,并加入3滴KSCN溶液,定容至
含量是影响产品品质的关键指标。定量测定方法是:取1.00g产品于烧杯中,加入适量盐酸溶解,并加入3滴KSCN溶液,定容至 ,取溶液置于比色管中,与标准色阶进行目视比色,确定产品级别。可以根据颜色确定产品级别的原理是
,取溶液置于比色管中,与标准色阶进行目视比色,确定产品级别。可以根据颜色确定产品级别的原理是(5)“步骤4”的具体操作如下:
取ag所制得的固体(摩尔盐的摩尔质量为
 )于小烧杯中,加入适量稀疏酸,溶解后在
)于小烧杯中,加入适量稀疏酸,溶解后在 容量瓶中定容。取
容量瓶中定容。取 于锥形瓶中,用
于锥形瓶中,用 的
的 ,溶液滴定至终点。终点的现象为
,溶液滴定至终点。终点的现象为 溶液的平均体积为
溶液的平均体积为 。此样品中摩尔盐的含量为
。此样品中摩尔盐的含量为A.配溶液定容时俯视刻度线 B.取摩尔盐溶液的滴定管没有润洗
C.取待测液的锥形瓶洗净后未干燥 D.摩尔盐的结晶水数量不足
您最近一年使用:0次
名校
解题方法
4 . 一种以菱镁矿(主要含 ,杂质为
,杂质为 、
、 、
、 )为原料制备
)为原料制备 的流程如下:
的流程如下:
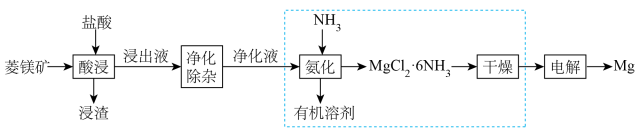
已知:25℃时,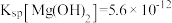
回答下列问题:
(1)“酸浸”时为了提高酸浸速率可采取的措施是___________ (任答一项);
(2)“浸渣”的主要成分为___________ ;
(3)①除去浸出液中的杂质,在实验室中可选择的除杂试剂是___________ (填化学式);
②假设浸出液中 的浓度
的浓度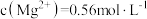 ,欲除尽杂质离子,需调节
,欲除尽杂质离子,需调节 不超过
不超过___________ ;
(4)①净化液“氨化”的化学方程式为___________ ;
②若用 与
与 结晶水合物共热也可以获得无水
结晶水合物共热也可以获得无水 ,用适当的化学用语和简要的文字说明
,用适当的化学用语和简要的文字说明 在此过程中所起的作用
在此过程中所起的作用___________ ;
③上述②方法与原流程虚线框中方法对比,弊端是___________ ;
(5)阐述电解法制 不用
不用 溶液的理由
溶液的理由___________ 。
 ,杂质为
,杂质为 、
、 、
、 )为原料制备
)为原料制备 的流程如下:
的流程如下:
已知:25℃时,
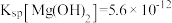
回答下列问题:
(1)“酸浸”时为了提高酸浸速率可采取的措施是
(2)“浸渣”的主要成分为
(3)①除去浸出液中的杂质,在实验室中可选择的除杂试剂是
②假设浸出液中
 的浓度
的浓度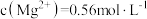 ,欲除尽杂质离子,需调节
,欲除尽杂质离子,需调节 不超过
不超过(4)①净化液“氨化”的化学方程式为
②若用
 与
与 结晶水合物共热也可以获得无水
结晶水合物共热也可以获得无水 ,用适当的化学用语和简要的文字说明
,用适当的化学用语和简要的文字说明 在此过程中所起的作用
在此过程中所起的作用③上述②方法与原流程虚线框中方法对比,弊端是
(5)阐述电解法制
 不用
不用 溶液的理由
溶液的理由
您最近一年使用:0次
5 . 某 溶液可能含有
溶液可能含有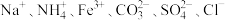 中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,气体全部逸出):
中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,气体全部逸出):

下列说法错误的是
 溶液可能含有
溶液可能含有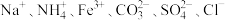 中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,气体全部逸出):
中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,气体全部逸出):
下列说法错误的是
A.原溶液一定存在 | B.原溶液一定存在 |
C.原溶液一定不存在 | D.原溶液中c(Na+)≥0.1mol/L |
您最近一年使用:0次
6 . 化学与生产生活密切相关。下列说法错误的是
| A.洗涤油污常用热的碳酸钠溶液 | B.铵态氮肥与草木灰不得混合施用 |
| C.电解精炼铜时,粗铜做阴极 | D.为除去水垢中的 ,可先用醋酸溶液处理 ,可先用醋酸溶液处理 |
您最近一年使用:0次
7 . 化学与生产、生活密切相关,下列说法正确的是
| A.活性炭可用于自来水的杀菌消毒 |
| B.热的纯碱溶液可用于洗涤餐具上的油污 |
C.废水中的 、 、 ,可加入 ,可加入 而被除去 而被除去 |
| D.煤的气化是煤在高温条件下由固态转化为气态的物理变化过程 |
您最近一年使用:0次
2023-11-12更新
|
193次组卷
|
2卷引用:辽宁省葫芦岛市协作校2023-2024学年高三上学期第二次考试化学试题
名校
解题方法
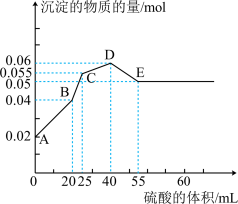
8 . 将由 三种固体组成的混合物溶于足量的水中,用玻璃棒搅拌,充分溶解,一段时间后,向稳定的混合物溶液中滴加
三种固体组成的混合物溶于足量的水中,用玻璃棒搅拌,充分溶解,一段时间后,向稳定的混合物溶液中滴加 的稀硫酸,加入稀硫酸的体积与生成沉淀的物质的量关系如图所示。下列有关判断不正确的是
的稀硫酸,加入稀硫酸的体积与生成沉淀的物质的量关系如图所示。下列有关判断不正确的是
 三种固体组成的混合物溶于足量的水中,用玻璃棒搅拌,充分溶解,一段时间后,向稳定的混合物溶液中滴加
三种固体组成的混合物溶于足量的水中,用玻璃棒搅拌,充分溶解,一段时间后,向稳定的混合物溶液中滴加 的稀硫酸,加入稀硫酸的体积与生成沉淀的物质的量关系如图所示。下列有关判断不正确的是
的稀硫酸,加入稀硫酸的体积与生成沉淀的物质的量关系如图所示。下列有关判断不正确的是
A.AB段发生反应的离子方程式为: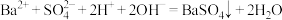 |
| B.D点表示的溶液呈酸性 |
| C.混合物中FeSO4和AlCl3的物质的量相等 |
D.BC段发生反应的离子方程式为: 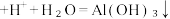 |
您最近一年使用:0次
9 . 化学与人类生产、生活密切相关,下列说法中错误的是
| A.晒少量用氯气消毒的自来水养小金鱼利用的是勒夏特列原理 |
| B.热的纯碱溶液洗涤油污的能力比冷的纯碱溶液强 |
| C.饱和石灰水中加入一定量生石灰,温度明显升高,所得溶液的pH减小 |
D.将 溶液和 溶液和 溶液混合可以制作泡沫灭火剂与盐类的水解无关 溶液混合可以制作泡沫灭火剂与盐类的水解无关 |
您最近一年使用:0次
10 . 已知:氮、磷、砷元素广泛应用于生产生活中,NH3、N2H4、NO、NO2、HNO3等是氮的重要化合物,白磷(P4)易自燃,易溶于CS2,Ca(H2PO4)2是磷肥的有效成分;砷化镓是重要的半导体材料。下列有关说法正确的是


| A.N2H4、NO2、HNO3中N的杂化方式均为sp2 |
| B.白磷分子(P4)是非极性分子,可保存在冷水中 |
| C.磷肥与草木灰混合施肥效果更佳 |
| D.砷化镓的晶胞结构如图所示,镓原子配位数为8 |
您最近一年使用:0次
2023-11-08更新
|
434次组卷
|
3卷引用:辽宁省沈阳市同泽高级中学2023-2024学年高二上学期第二次月考化学试题



