解题方法
1 . 下列化学用语或图示表达不正确的是
A.砷原子的简化电子排布式为: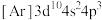 |
B. 的水解方程式: 的水解方程式: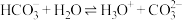 |
C.硫酸钡在水中的沉淀溶解平衡: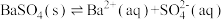 |
| D.一个电子从3p能级跃迁到3s能级,产生的原子光谱为发射光谱 |
您最近一年使用:0次
名校
解题方法
2 . 下列有关化学用语表示正确的是
A.HS-水解:HS-+H2O S2- +H3O+ S2- +H3O+ |
B.醋酸溶液中滴加Na2CO3溶液:2H++ =CO2↑+H2O =CO2↑+H2O |
C.电解MgCl2溶液:2Cl-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
D.已知Ka(HCN)=4.9×10-10,H2CO3:Ka1=4.3×10-7;Ka2=5.6×10-11,向KCN(ag)中通入少量的CO2气体: CO2+H2O+CN-=HCN+ |
您最近一年使用:0次
名校
解题方法
3 . 下列离子方程式与所述事实相符且书写正确的是
A.洪水过后,用明矾净化生活用水: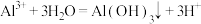 |
B.滴加氨水,除去 溶液中的 溶液中的 : : |
C.用酸性 溶液滴定草酸溶液: 溶液滴定草酸溶液: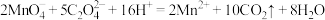 |
D.用惰性电极电解 溶液: 溶液: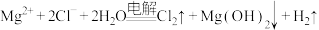 |
您最近一年使用:0次
2024-01-07更新
|
100次组卷
|
2卷引用:河南省驻马店市遂平县第一高级中学2023-2024学年高二上学期期中考试化学试卷
名校
4 . 有关化学反应原理的下列说法中正确的是
A. 溶液水解的离子方程式: 溶液水解的离子方程式: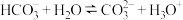 |
B.常温下,反应 不能自发进行,则该反应的 不能自发进行,则该反应的 |
| C.在酶催化淀粉水解反应中,温度越高淀粉水解速率越快 |
| D.常温下,向纯水中加入钠或氢氧化钠都能使水的电离平衡逆向移动,水离子积不变 |
您最近一年使用:0次
名校
解题方法
5 . 下列离子方程式正确的是
A. 水解反应的离子方程式: 水解反应的离子方程式: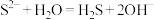 |
B.用氯化铁溶液刻蚀铜电路板: |
C.向硫酸氢钠溶液中滴加氢氧化钡溶液至中性: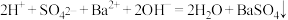 |
D.向 溶液通入少量 溶液通入少量 : : |
您最近一年使用:0次
2023-12-01更新
|
101次组卷
|
2卷引用:河南省驻马店高级中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
6 . 醋酸是日常生活中最常见的调味剂和重要的化工原料,醋酸钠是其常见的盐。[已知:25℃,Ka(CH3COOH)=1.69×10-5]。请回答下列问题:
(1)写出醋酸钠溶液中存在的平衡(离子方程式):___________ 。
(2)常温时,pH=3的醋酸和pH=11的NaOH溶液等体积混合后,溶液中c(Na+)___________ c(CH3COO-)(填“>”“<”或“=”),该溶液中电荷守恒表达式为___________ 。
(3)常温时,将mmol·L-1的醋酸和nmol·L-1的NaOH溶液等体积混合后,所得溶液的pH=7,则m与n的大小关系是m________ n,醋酸溶液中c(H+)_________ NaOH溶液中c(OH-)(填“>”“<”或“=”)。
(4)某小组研究25℃下CH3COOH电离平衡的影响因素。
提出假设稀释CH3COOH溶液或改变CH3COO-浓度,CH3COOH电离平衡会发生移动。
设计方案并完成实验用浓度均为0.1mol·L-1的CH3COOH和CH3COONa溶液,按下表配制总体积相同的系列溶液;测定pH,记录数据。
①根据表中信息,补充数据:a=___________ ,b=___________ 。
②由实验Ⅰ和Ⅱ可知,稀释CH3COOH溶液,电离平衡___________ (填“正”或“逆”)向移动;结合表中数据,给出判断理由:___________ 。
③由实验Ⅱ~Ⅷ可知,增大CH3COO-浓度,CH3COOH电离平衡逆向移动。
实验结论假设成立。
(1)写出醋酸钠溶液中存在的平衡(离子方程式):
(2)常温时,pH=3的醋酸和pH=11的NaOH溶液等体积混合后,溶液中c(Na+)
(3)常温时,将mmol·L-1的醋酸和nmol·L-1的NaOH溶液等体积混合后,所得溶液的pH=7,则m与n的大小关系是m
(4)某小组研究25℃下CH3COOH电离平衡的影响因素。
提出假设稀释CH3COOH溶液或改变CH3COO-浓度,CH3COOH电离平衡会发生移动。
设计方案并完成实验用浓度均为0.1mol·L-1的CH3COOH和CH3COONa溶液,按下表配制总体积相同的系列溶液;测定pH,记录数据。
| 序号 | V(CH3COOH)/mL | V(CH3COONa)/mL | V(H2O)/mL | n(CH3COONa)∶n(CH3COOH) | pH |
| Ⅰ | 40.00 | / | / | 0 | 2.86 |
| Ⅱ | 4.00 | / | 36.00 | 0 | 3.36 |
| … | |||||
| Ⅶ | 4.00 | a | b | 3∶4 | 4.53 |
| Ⅷ | 4.00 | 4.00 | 32.00 | 1∶1 | 4.65 |
②由实验Ⅰ和Ⅱ可知,稀释CH3COOH溶液,电离平衡
③由实验Ⅱ~Ⅷ可知,增大CH3COO-浓度,CH3COOH电离平衡逆向移动。
实验结论假设成立。
您最近一年使用:0次
7 . 请按要求用化学用语作答。
(1)已知 在氧气中燃烧完全转化为S单质放出
在氧气中燃烧完全转化为S单质放出 热量,完全转化为
热量,完全转化为 放出
放出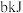 热量,写出表示
热量,写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式_______ 。
(2)明矾[化学式为 ]可以作净水剂的原因是
]可以作净水剂的原因是_______ (用离子方程式表示)。
(3)已知 是一种一元酸,写出它的正盐水解的离子方程式
是一种一元酸,写出它的正盐水解的离子方程式_______ 。
(4) 溶液可通过调节
溶液可通过调节 改变颜色,原因是
改变颜色,原因是_______ (用离子方程式表示)。
(5)将 固体放入水中,写出该反应的化学方程式
固体放入水中,写出该反应的化学方程式_______ 。
(1)已知
 在氧气中燃烧完全转化为S单质放出
在氧气中燃烧完全转化为S单质放出 热量,完全转化为
热量,完全转化为 放出
放出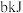 热量,写出表示
热量,写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式(2)明矾[化学式为
 ]可以作净水剂的原因是
]可以作净水剂的原因是(3)已知
 是一种一元酸,写出它的正盐水解的离子方程式
是一种一元酸,写出它的正盐水解的离子方程式(4)
 溶液可通过调节
溶液可通过调节 改变颜色,原因是
改变颜色,原因是(5)将
 固体放入水中,写出该反应的化学方程式
固体放入水中,写出该反应的化学方程式
您最近一年使用:0次
8 . 已知:25℃时, 、
、 、
、 。
。

(1)常温下,将pH和体积均相同的 和
和 溶液分别稀释,溶液pH随加水体积的变化如图:
溶液分别稀释,溶液pH随加水体积的变化如图:
①曲线I代表___________ 溶液(填“ ”或“
”或“ ”)。
”)。
②a、b两点对应的溶液中,水的电离程度a___________ b(填“>”“<”或“=”)。
③向上述 溶液和
溶液和 溶液分别滴加等浓度的NaOH溶液,当恰好中和时,消耗NaOH溶液体积分别为
溶液分别滴加等浓度的NaOH溶液,当恰好中和时,消耗NaOH溶液体积分别为 和
和 ,则
,则
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
④酸度(AG)也可表示溶液的酸碱性, 。常温下,pH=2的硝酸溶液AG=
。常温下,pH=2的硝酸溶液AG=___________ 。
(2)25℃时,往 溶液中加入NaOH溶液。
溶液中加入NaOH溶液。
①当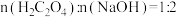 ,生成
,生成 ,
, 水解的离子方程式为
水解的离子方程式为___________ 。
②当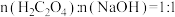 ,溶液显
,溶液显___________ 性(填“酸”、“碱”或“中”),
③等浓度等体积的 、
、 混合,溶液中
混合,溶液中
___________ 。
 、
、 、
、 。
。
(1)常温下,将pH和体积均相同的
 和
和 溶液分别稀释,溶液pH随加水体积的变化如图:
溶液分别稀释,溶液pH随加水体积的变化如图:①曲线I代表
 ”或“
”或“ ”)。
”)。②a、b两点对应的溶液中,水的电离程度a
③向上述
 溶液和
溶液和 溶液分别滴加等浓度的NaOH溶液,当恰好中和时,消耗NaOH溶液体积分别为
溶液分别滴加等浓度的NaOH溶液,当恰好中和时,消耗NaOH溶液体积分别为 和
和 ,则
,则
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。④酸度(AG)也可表示溶液的酸碱性,
 。常温下,pH=2的硝酸溶液AG=
。常温下,pH=2的硝酸溶液AG=(2)25℃时,往
 溶液中加入NaOH溶液。
溶液中加入NaOH溶液。①当
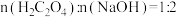 ,生成
,生成 ,
, 水解的离子方程式为
水解的离子方程式为②当
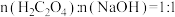 ,溶液显
,溶液显③等浓度等体积的
 、
、 混合,溶液中
混合,溶液中
您最近一年使用:0次
解题方法
9 . 下列原理的应用及离子方程式书写均正确的是
A.用 水解制备 水解制备 (加大量水并加热): (加大量水并加热): |
B.泡沫灭火器原理: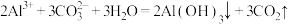 |
C.铅蓄电池放电时正极上的反应: |
D.某弱酸的酸式盐NaHB在水溶液中的水解: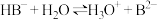 |
您最近一年使用:0次
名校
10 . 下列化学用语表达正确的是
A. 的电离方程式: 的电离方程式: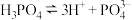 |
B.以 溶液为电解质溶液,氢氧燃料电池负极的电极反应式: 溶液为电解质溶液,氢氧燃料电池负极的电极反应式: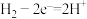 |
C. 水解的离子方程式: 水解的离子方程式: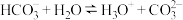 |
D. 的溶解平衡表达式: 的溶解平衡表达式: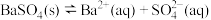 |
您最近一年使用:0次
2023-02-13更新
|
132次组卷
|
2卷引用:河南省商丘市第一高级中学2022-2023学年高二下学期3月份考试化学试题



