1 . 根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向2mL0.01mol/LNa2S溶液中先滴入几滴0.01mol∙L-1CuSO4溶液有黑色沉淀生成,再滴入0.01mol/LZnSO4溶液,又有白色沉淀生成 | Ksp(ZnS)<Ksp(CuS) |
| B | 室温下,用pH计测得0.1mol/LCH3COONH4溶液的pH小于0.1mol/LNaHCO3溶液 | 水解平衡常数:Kh(CH3COO-)<Kh( ) ) |
| C | 常温下,测得0.1mol/LNaA溶液的pH小于0.1mol/LNa2B溶液的pH | 酸性:HA>H2B |
| D | 向5mL0.005mol/LFeCl3溶液中加入5mL0.015mol/LKSCN溶液,溶液变红,再加入少量铁粉,溶液颜色变浅 | 加入铁粉后,Fe3++3SCN-⇌Fe(SCN)3向逆反应方向移动 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
2 . 粗硫酸铜中常含有难溶性杂质和少量 、
、 ,某小组用粗硫酸铜制取较纯净的胆矾晶体并用碘量法测定其纯度,请回答下列问题:
,某小组用粗硫酸铜制取较纯净的胆矾晶体并用碘量法测定其纯度,请回答下列问题:
Ⅰ.胆矾晶体( )的制备
)的制备
配制硫酸铜溶液:将一定质量的粗硫酸铜置于盛有稀硫酸的烧杯中,加热并不断搅拌使可溶性部分充分溶解,停止加热。
除杂:往溶液中加入过量3%的 溶液并加热,充分反应后再持续加热一段时间,冷却后调节溶液pH至3.5~4,过滤、洗涤,将滤液和洗涤液转移至蒸发皿中。
溶液并加热,充分反应后再持续加热一段时间,冷却后调节溶液pH至3.5~4,过滤、洗涤,将滤液和洗涤液转移至蒸发皿中。
结晶:用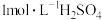 调节pH至1~2,然后经过一系列实验操作,最后经洗涤、干燥得到胆矾晶体。
调节pH至1~2,然后经过一系列实验操作,最后经洗涤、干燥得到胆矾晶体。
(1)结合上述操作,除所给仪器外,配制硫酸铜溶液的过程中还需要的玻璃仪器有_______ (填仪器名称)。
(2)除杂过程中,加入 反应的离子方程式
反应的离子方程式_______ ,是调节溶液pH至3.5~4的目的是_______ 。
(3)结晶过程中,调节pH的目的是_______ ,“一系列实验操作”步骤有_______ 。
Ⅱ.碘量法测定胆矾晶体的纯度:
称取胆矾晶体m g,加适量稀硫酸和水配成250mL溶液,每次取25.00mL,加入过量的KI溶液(杂质不参与反应),再加几滴淀粉溶液,用 溶液滴定至终点
溶液滴定至终点
(已知: ,
, )。
)。
(4)有关滴定管的正确操作顺序为(填字母):_______ 。
检漏→蒸馏水洗涤→→→→→→开始滴定。
A.装入滴定液至零刻度以上
B.调整滴定液液面至零刻度或零刻度以下
C.排除气泡
D.用滴定液润洗2~3次
E.记录起始读数
(5)滴定终点时的现象为_______ 。
(6)若平均消耗 溶液V mL,则所得样品中
溶液V mL,则所得样品中 的纯度为
的纯度为_______ ×100%(用含字母的表达式表示)。
 、
、 ,某小组用粗硫酸铜制取较纯净的胆矾晶体并用碘量法测定其纯度,请回答下列问题:
,某小组用粗硫酸铜制取较纯净的胆矾晶体并用碘量法测定其纯度,请回答下列问题:Ⅰ.胆矾晶体(
 )的制备
)的制备配制硫酸铜溶液:将一定质量的粗硫酸铜置于盛有稀硫酸的烧杯中,加热并不断搅拌使可溶性部分充分溶解,停止加热。
除杂:往溶液中加入过量3%的
 溶液并加热,充分反应后再持续加热一段时间,冷却后调节溶液pH至3.5~4,过滤、洗涤,将滤液和洗涤液转移至蒸发皿中。
溶液并加热,充分反应后再持续加热一段时间,冷却后调节溶液pH至3.5~4,过滤、洗涤,将滤液和洗涤液转移至蒸发皿中。结晶:用
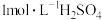 调节pH至1~2,然后经过一系列实验操作,最后经洗涤、干燥得到胆矾晶体。
调节pH至1~2,然后经过一系列实验操作,最后经洗涤、干燥得到胆矾晶体。(1)结合上述操作,除所给仪器外,配制硫酸铜溶液的过程中还需要的玻璃仪器有
(2)除杂过程中,加入
 反应的离子方程式
反应的离子方程式(3)结晶过程中,调节pH的目的是
Ⅱ.碘量法测定胆矾晶体的纯度:
称取胆矾晶体m g,加适量稀硫酸和水配成250mL溶液,每次取25.00mL,加入过量的KI溶液(杂质不参与反应),再加几滴淀粉溶液,用
 溶液滴定至终点
溶液滴定至终点(已知:
 ,
, )。
)。(4)有关滴定管的正确操作顺序为(填字母):
检漏→蒸馏水洗涤→→→→→→开始滴定。
A.装入滴定液至零刻度以上
B.调整滴定液液面至零刻度或零刻度以下
C.排除气泡
D.用滴定液润洗2~3次
E.记录起始读数
(5)滴定终点时的现象为
(6)若平均消耗
 溶液V mL,则所得样品中
溶液V mL,则所得样品中 的纯度为
的纯度为
您最近半年使用:0次
3 .  俗名绿矾,可用于制铁盐、氧化铁颜料、净水剂、消毒剂等。由硫铁矿烧渣(主要成分:
俗名绿矾,可用于制铁盐、氧化铁颜料、净水剂、消毒剂等。由硫铁矿烧渣(主要成分: 、
、 、FeO、
、FeO、 )制备绿矾流程如下:
)制备绿矾流程如下:

已知:① 难溶于水,能还原
难溶于水,能还原 ,硫元素被氧化成
,硫元素被氧化成 。
。
②金属离子生成氢氧化物沉淀的pH范围见下表:
(1)提高“酸浸”速率的措施有___________ (任写一点即可):写出滤渣Ⅰ与某种酸反应的化学方程式___________ ;滤渣Ⅱ经灼烧后可用于___________ (写出一种用途即可)。
(2)写出“还原”步骤中涉及反应的离子方程式___________ 。
(3)“除铝”需控制的pH范围是___________ 。
(4)“酸化”步骤中加入稀硫酸的目的是___________ 。操作Ⅲ为___________ ;“洗涤”时的试剂最好选用下列中的___________ (填代号)
A.热水 B.氯水 C.乙醇 D.饱和食盐水
(5)设计实验检验制得的绿矾晶体中是否含有 :
:___________ 。
 俗名绿矾,可用于制铁盐、氧化铁颜料、净水剂、消毒剂等。由硫铁矿烧渣(主要成分:
俗名绿矾,可用于制铁盐、氧化铁颜料、净水剂、消毒剂等。由硫铁矿烧渣(主要成分: 、
、 、FeO、
、FeO、 )制备绿矾流程如下:
)制备绿矾流程如下:
已知:①
 难溶于水,能还原
难溶于水,能还原 ,硫元素被氧化成
,硫元素被氧化成 。
。②金属离子生成氢氧化物沉淀的pH范围见下表:
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
 | 1.5 | 3.2 |
 | 3.0 | 5.0 |
 | 6.3 | 8.3 |
(1)提高“酸浸”速率的措施有
(2)写出“还原”步骤中涉及反应的离子方程式
(3)“除铝”需控制的pH范围是
(4)“酸化”步骤中加入稀硫酸的目的是
A.热水 B.氯水 C.乙醇 D.饱和食盐水
(5)设计实验检验制得的绿矾晶体中是否含有
 :
:
您最近半年使用:0次
4 . 以锌灰(含ZnO及少量PbO、CuO、Fe2O3、SiO2)和Fe2 (SO4)3为原料可以制备脱硫剂ZnFe2O4。该脱硫剂的制备硫化、再生过程可表示为
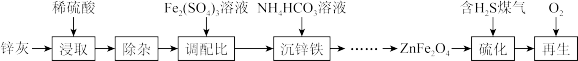
回答下列问题:
(1)“浸取”时为加快浸取速率,可以采取的措施有___________ (任写一条)。
(2)“除杂”包括加适量锌粉、过滤、加H2O2氧化等步骤。“加入H2O2氧化”的目的是___________ ,除Pb2+和Cu2+外,与锌粉反应的离子还有___________ (填离子符号)。
(3)“沉锌铁”时反应体系温度不能过高,可能的原因是___________ 。
(4)400 °C时,将一定比例H2、CO、CO2和H2S的混合气体以一定流速通过装有脱硫剂ZnFe2O4的硫化反应器。
①硫化过程中,ZnFe2O4与H2、H2S反应生成ZnS和FeS,其化学方程式为___________ 。
②硫化一段时间后,出口处检测到COS。研究表明ZnS参与了H2S与CO2生成COS的反应,但反应前后ZnS的质量不变, ZnS的作用是___________ ,生成COS的总反应化学方程式为___________ 。
(5)将硫化后的固体在V(N2) : V(O2) =95 : 5的混合气体中加热再生,固体质量随温度变化的曲线如图所示。在280~400 °C范围内,固体质量增加的主要原因可能是___________ 。


回答下列问题:
(1)“浸取”时为加快浸取速率,可以采取的措施有
(2)“除杂”包括加适量锌粉、过滤、加H2O2氧化等步骤。“加入H2O2氧化”的目的是
(3)“沉锌铁”时反应体系温度不能过高,可能的原因是
(4)400 °C时,将一定比例H2、CO、CO2和H2S的混合气体以一定流速通过装有脱硫剂ZnFe2O4的硫化反应器。
①硫化过程中,ZnFe2O4与H2、H2S反应生成ZnS和FeS,其化学方程式为
②硫化一段时间后,出口处检测到COS。研究表明ZnS参与了H2S与CO2生成COS的反应,但反应前后ZnS的质量不变, ZnS的作用是
(5)将硫化后的固体在V(N2) : V(O2) =95 : 5的混合气体中加热再生,固体质量随温度变化的曲线如图所示。在280~400 °C范围内,固体质量增加的主要原因可能是

您最近半年使用:0次
名校
5 . 碱式碳酸锰[Mn2(OH)2CO3]是一种不溶于水的固体,是制造其他含锰化合物的原料。工业上以方锰矿(主要成分为 MnO,还含有少量的 Fe3O4、Al2O3、CaO、SiO2)为原料制备碱式碳酸锰。
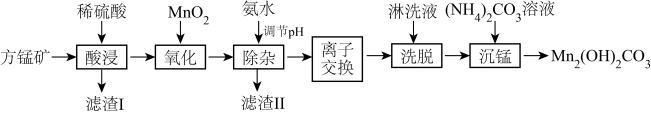
25℃时,相关物质的 Ksp如下表:
回答下列问题:
(1)“酸浸”时,滤渣I的成分是___________ (填化学式)。
(2)“氧化”时,该反应的离子方程式为___________ 。
(3)“除杂”时,使用氨水的目的是将 Fe3+和Al3+转化为沉淀而除去,则应调节溶液的pH≥______ ;若 A13+沉淀完全时,则溶液中 Fe3+的物质的量浓度为___________ mol·L-1(通常认为溶液中的离子浓度≤1×10-5mol·L-1沉淀完全)
(4)“离子交换”和“洗脱”时,发生反应:Mn2+ +2HR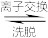 MnR2 +2H+(HR 是氢型交换树脂)。洗脱为了提高“洗脱”效率,淋洗液应为
MnR2 +2H+(HR 是氢型交换树脂)。洗脱为了提高“洗脱”效率,淋洗液应为___________ (填“硫酸”、“氢氧化钠溶液”或“蒸馏水”)。
(5)“沉锰”时,反应的离子方程式为___________ ,过滤、洗涤、干燥,得到Mn2(OH)2CO3,检验沉淀是否洗涤干净的操作是___________ 。
(6)为测定产品中锰的含量,取 a g 样品于烧杯中,加水溶解,加入足量的稀硫酸溶解,滴加过量的 0.1000 mol·L-1(NH4)2S2O8溶液将锰元素转化为 MnO ,充分反应后加热一段时间,冷却将烧杯中的溶液全部转移至 250mL 容量瓶中。取 25.00mL 于锥形瓶中,用0.1000mol·L-1FeSO4标准溶液滴定,达滴定终点时,消耗 FeSO4溶液的体积为 V mL。
,充分反应后加热一段时间,冷却将烧杯中的溶液全部转移至 250mL 容量瓶中。取 25.00mL 于锥形瓶中,用0.1000mol·L-1FeSO4标准溶液滴定,达滴定终点时,消耗 FeSO4溶液的体积为 V mL。
①滴定终点的现象是___________ 。
②该产品中锰的质量分数为___________ 。(用含 a、V 的式子表示)。

25℃时,相关物质的 Ksp如下表:
| 物质 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Ca(OH)2 |
| Ksp | 2×10-13 | 5×10-17 | 3×10-39 | 1×10-32 | 6×10-6 |
(1)“酸浸”时,滤渣I的成分是
(2)“氧化”时,该反应的离子方程式为
(3)“除杂”时,使用氨水的目的是将 Fe3+和Al3+转化为沉淀而除去,则应调节溶液的pH≥
(4)“离子交换”和“洗脱”时,发生反应:Mn2+ +2HR
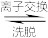 MnR2 +2H+(HR 是氢型交换树脂)。洗脱为了提高“洗脱”效率,淋洗液应为
MnR2 +2H+(HR 是氢型交换树脂)。洗脱为了提高“洗脱”效率,淋洗液应为(5)“沉锰”时,反应的离子方程式为
(6)为测定产品中锰的含量,取 a g 样品于烧杯中,加水溶解,加入足量的稀硫酸溶解,滴加过量的 0.1000 mol·L-1(NH4)2S2O8溶液将锰元素转化为 MnO
 ,充分反应后加热一段时间,冷却将烧杯中的溶液全部转移至 250mL 容量瓶中。取 25.00mL 于锥形瓶中,用0.1000mol·L-1FeSO4标准溶液滴定,达滴定终点时,消耗 FeSO4溶液的体积为 V mL。
,充分反应后加热一段时间,冷却将烧杯中的溶液全部转移至 250mL 容量瓶中。取 25.00mL 于锥形瓶中,用0.1000mol·L-1FeSO4标准溶液滴定,达滴定终点时,消耗 FeSO4溶液的体积为 V mL。①滴定终点的现象是
②该产品中锰的质量分数为
您最近半年使用:0次
2022-06-01更新
|
603次组卷
|
3卷引用:山西省太原市第五中学校2022届高三下学期二模理综化学试题
名校
解题方法
6 . 能够使CH3COONa溶液pH增大且水解程度也增大的条件是
| A.加水 | B.升温 | C.加压 | D.加CH3COONa固体 |
您最近半年使用:0次
2022-03-24更新
|
1144次组卷
|
7卷引用:山西省阳泉市第一中学校2022-2023学年高二上学期11月期中考试化学试题
山西省阳泉市第一中学校2022-2023学年高二上学期11月期中考试化学试题吉林省长春希望高中2021-2022学年高二上学期期末考试化学试题(已下线)3.3.2 影响盐类的水解的主要因素-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)吉林省吉林松花江中学2022-2023学年高二上学期1月期末考试化学试题黑龙江省鹤岗市第一中学2022-2023学年高二上学期11月期中考试化学试题福建省福州超德中学2023-2024学年高二上学期期末考试化学试题宁夏开元学校2023-2024学年高二学年下学期开学收心测试化学试题
名校
解题方法
7 . 常温下,下列有关电解质溶液的说法不正确 的是
A.向Na2CO3溶液中通入NH3,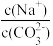 减小 减小 |
B.将0.1 mol·L-1的K2C2O4溶液从25 ℃升温至35 ℃,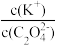 增大 增大 |
C.向0.1 mol·L-1的HF溶液中滴加NaOH溶液至中性, =1 =1 |
D.向0.1 mol·L-1的CH3COONa溶液中加入少量水,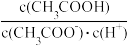 增大 增大 |
您最近半年使用:0次
2022-03-23更新
|
546次组卷
|
17卷引用:【全国百强校】山西省山西大学附属中学2019届高三上学期9月模块诊断化学试题
【全国百强校】山西省山西大学附属中学2019届高三上学期9月模块诊断化学试题广西防城港市2018届高三1月模拟考试理综化学试题安徽省长丰县双墩中学2018-2019学年高二上学期期末调研化学试题安徽省肥东县第二中学2019-2020学年高二上学期期中考试化学试题备考突破2020高三化学专题强化集训——盐类水解中的三大守恒的应用夯基提能2020届高三化学选择题对题专练 ——选修四化学反应原理——电离平衡常数及其影响因素专练 (2)【百强校】天津市静海区第一中学2020届高三下学期第七周周末训练化学试题天津市实验中学2020届高三下学期4月第一次测试化学试题广东省云浮市2018-2019学年高二上学期期末考试化学试题甘肃省白银市第十中学2019-2020学年高二上学期期中考试化学试题解题达人.化学选择题(2021全国卷)巩固小卷02河南省郑州市第四高级中学2021-2022学年高二下学期第二次调研考试化学试题黑龙江省大兴安岭呼玛县高级中学2021-2022学年高三上学期期末考试化学试题湖北省宜昌英杰学校2021-2022学年高三上学期10月月考化学试题安徽省桐城中学2022-2023学年高二上学期月考(1)化学试题河南省郑州市2021-2022学年高二上学期期末考试化学试题(已下线)第八章 水溶液中的离子反应与平衡 第49练 盐类的水解
8 . BiOCl是一种具有珠光泽的材料,利用金属Bi制备BiOCl的工艺流程如图:
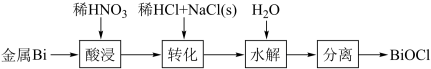
下列说法错误的是

下列说法错误的是
| A.酸浸工序中分次加入稀HNO3可降低反应剧烈程度 |
| B.转化工序中加入稀HCl可抑制生成BiONO3 |
| C.水解工序中加入少量CH3COONa(s)可提高Bi3+水解程度 |
| D.水解工序中加入少量NH4NO3(s)有利于BiOCl的生成 |
您最近半年使用:0次
2021-06-09更新
|
8431次组卷
|
33卷引用:山西省怀仁市2021-2022学年高二上学期期末调研化学试题
山西省怀仁市2021-2022学年高二上学期期末调研化学试题2021年新高考河北化学高考真题(已下线)考点14 铝及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点31 化学实验与工艺流程-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点14 铝及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)河北省衡水中学2021-2022学年高二上学期8月份线上调研化学试题湖南省邵阳邵东市第一中学2022届高三上学期第一次月考化学试题江西省乐平三中2021-2022高二上学期9月月考化学试题辽宁省东北育才学校2021-2022学年高二上学期期中考试化学试题2021年河北省高考化学试卷变式题1-9题(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)专题14 无机综合运用(选择题)-2022年高考化学二轮复习重点专题常考点突破练福建省龙岩第一中学2021-2022学年高二上学期第二次月考化学试题(实验班)(已下线)卷05 工艺流程型选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)卷04 小题仿真卷-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)押新高考卷03题 元素化合物的性质-备战2022年高考化学临考题号押题(新高考通版)(已下线)专题14 物质的反应和转化-三年(2020-2022)高考真题分项汇编(已下线)考点15 铝及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)河南省洛阳市新安县第一高级中学2022-2023学年高三上学期入学测试(实验小班)化学试题浙江省杭州高级中学2022-2023学年高三上学期模拟考试化学试题(已下线)专题14 工艺流程选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 专题14 溶液中的三大平衡及应用第四章 非金属及其化合物 第25讲 非金属及其化合物知识落实与拓展(已下线)素养卷08 微型化学工艺流程分析-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题10 物质的反应及转化(已下线)专题10 物质的反应及转化(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)河北省石家庄二中实验学校2023-2024学年高三上学期10月第二次调研考试化学试题(已下线)第4讲 盐类的水解湖北省恩施高中2023-2024学年高一下学期入学考试化学试题湖南省长沙市湖南师范大学附属中学2023-2024学年高三下学期第七次月考化学试题湖南省师范大学附属中学2023-2024学年高三下学期 月考化学试卷
解题方法
9 . 温度一定时,为了使 Na2S 溶液中  的比值变小,可采取的措施是:
的比值变小,可采取的措施是:
①加适量盐酸 ②加适量 NaOH(s) ③加适量 KOH(s) ④加适量 KHS(s) ⑤加水 ⑥通入适量 Cl2⑦加热
 的比值变小,可采取的措施是:
的比值变小,可采取的措施是:①加适量盐酸 ②加适量 NaOH(s) ③加适量 KOH(s) ④加适量 KHS(s) ⑤加水 ⑥通入适量 Cl2⑦加热
| A.②③④ | B.①②⑤⑥⑦ | C.②③ | D.③④ |
您最近半年使用:0次
10 . 下列说法正确的是
| A.强电解质溶液中不存在分子,弱电解质溶液中存在分子 |
| B.在其他外界条件不变的情况下,增大压强能增大活化分子百分数 |
C.反应 在室温下不能自发进行,说明该反应的 在室温下不能自发进行,说明该反应的 |
D.配制一定浓度 溶液时,将 溶液时,将 固体溶于少量浓盐酸,然后用水稀释到所需的浓度 固体溶于少量浓盐酸,然后用水稀释到所需的浓度 |
您最近半年使用:0次
2021-01-25更新
|
165次组卷
|
2卷引用:山西省太原市2020-2021学年高二上学期期末化学(理)试题



