2021高三·全国·专题练习
1 . (1)电解质在水中存在沉淀溶解平衡,是一种动态平衡____
(2)AgCl沉淀的生成和溶解不断进行,但速率相等____
(3)AgCl难溶于水,溶液中没有Ag+和Cl-_____
(4)升高温度,AgCl的溶解度不变____
(5)向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度不变____
(6)只有易溶电解质在溶液中才存在溶解平衡_____
(7)难溶电解质在溶液中只存在溶解平衡,不存在电离平衡_____
(8)溶解平衡只能通过电解质溶解于水时建立_____
(9)升高温度,沉淀溶解平衡一定正向移动____
(10)室温下,AgCl在水中的溶解度小于在食盐水中的溶解度____
(11)难溶电解质达到沉淀溶解平衡时,增加难溶电解质的量,平衡向溶解方向移动____
(12)向Na2SO4溶液中加入过量的BaCl2溶液,则SO 沉淀完全,溶液中只含Ba2+、Na+和Cl-,不含SO
沉淀完全,溶液中只含Ba2+、Na+和Cl-,不含SO
____
(13)饱和Na2CO3溶液与CaSO4固体反应:CO +CaSO4⇌CaCO3+SO
+CaSO4⇌CaCO3+SO
____
(2)AgCl沉淀的生成和溶解不断进行,但速率相等
(3)AgCl难溶于水,溶液中没有Ag+和Cl-
(4)升高温度,AgCl的溶解度不变
(5)向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度不变
(6)只有易溶电解质在溶液中才存在溶解平衡
(7)难溶电解质在溶液中只存在溶解平衡,不存在电离平衡
(8)溶解平衡只能通过电解质溶解于水时建立
(9)升高温度,沉淀溶解平衡一定正向移动
(10)室温下,AgCl在水中的溶解度小于在食盐水中的溶解度
(11)难溶电解质达到沉淀溶解平衡时,增加难溶电解质的量,平衡向溶解方向移动
(12)向Na2SO4溶液中加入过量的BaCl2溶液,则SO
 沉淀完全,溶液中只含Ba2+、Na+和Cl-,不含SO
沉淀完全,溶液中只含Ba2+、Na+和Cl-,不含SO
(13)饱和Na2CO3溶液与CaSO4固体反应:CO
 +CaSO4⇌CaCO3+SO
+CaSO4⇌CaCO3+SO
您最近一年使用:0次
解题方法
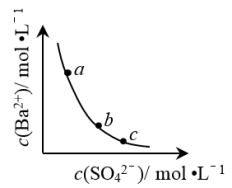
2 . 一定温度下,BaSO4(s)⇌Ba2+(aq)+ (aq)平衡体系中,c(Ba2+)和c(
(aq)平衡体系中,c(Ba2+)和c( )的关系如图所示。下列说法正确的是
)的关系如图所示。下列说法正确的是
 (aq)平衡体系中,c(Ba2+)和c(
(aq)平衡体系中,c(Ba2+)和c( )的关系如图所示。下列说法正确的是
)的关系如图所示。下列说法正确的是
| A.a、b、c三点对应的KW不相等 |
B.a、b、c三点对应c(Ba2+)•c( )的数值,a点最大 )的数值,a点最大 |
C.BaSO4在水中形成的饱和溶液,c(Ba2+)=c( ) ) |
| D.a点对应的溶液中加入BaSO4固体,c(Ba2+)沿曲线向b、c点方向变化 |
您最近一年使用:0次
名校
3 . 在CaCO3饱和溶液中,加入Na2CO3固体,达到平衡时
A.c(Ca2+)=c( ) ) |
B.c(Ca2+)=c( )= )= |
C.c(Ca2+)≠c( ),c(Ca2+)·c( ),c(Ca2+)·c( )=Ksp(CaCO3) )=Ksp(CaCO3) |
D.c(Ca2+)≠c( ),c(Ca2+)·c( ),c(Ca2+)·c( )≠Ksp(CaCO3) )≠Ksp(CaCO3) |
您最近一年使用:0次
2021-07-12更新
|
334次组卷
|
6卷引用:3.4.1 沉淀溶解平衡原理(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)
(已下线)3.4.1 沉淀溶解平衡原理(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)云南省马关县一中2020-2021学年高二下学期6月月考化学试题(已下线)期中试卷02-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)(已下线)第33练 沉淀溶解平衡-2023年高考化学一轮复习小题多维练(全国通用)云南省玉溪市江川区第一中学2021-2022学年高二下学期3月月考化学试题第三章 第四节 沉淀溶解平衡 第1课时 沉淀溶解平衡与溶度积
解题方法
4 . 下列离子方程式书写正确的是
A. 沉淀在水中的溶解: 沉淀在水中的溶解: |
B. 的电离: 的电离: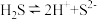 |
C. 的水解: 的水解: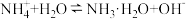 |
D.明矾净水原理: |
您最近一年使用:0次
解题方法
5 . 实验室由铁泥(主要成分为铁的氧化物,还含有少量 和CaO等)制备软磁性材料
和CaO等)制备软磁性材料 。其主要实验流程如下:
。其主要实验流程如下:

(1)酸浸:用一定浓度的 溶液浸取铁泥中的铁元素。若其他条件不变,实验中能加快铁元素浸出速率的措施有
溶液浸取铁泥中的铁元素。若其他条件不变,实验中能加快铁元素浸出速率的措施有_______ (写出一种方法),酸浸后的滤渣的主要成分是_______ 、_______ 。
(2)还原:向“酸浸”后的滤液中加入过量铁粉,使 完全转化为
完全转化为 。“还原”过程中发生的主要反应的离子方程式为
。“还原”过程中发生的主要反应的离子方程式为_______ ﹔检验 完全被还原的实验方案为
完全被还原的实验方案为_______ 。
(3)除杂:向“还原”后的滤液中加入 溶液,使
溶液,使 转化为
转化为 沉淀除去。若溶液的酸性较强,将会导致
沉淀除去。若溶液的酸性较强,将会导致 沉淀不完全,其原因是
沉淀不完全,其原因是_______ (从平衡移动的角度分析,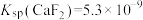 ,
,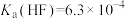 )。
)。
(4)沉铁:将提纯后的 溶液与氨水—
溶液与氨水— 混合溶液反应,生成
混合溶液反应,生成 沉淀。生成
沉淀。生成 沉淀的离子方程式为
沉淀的离子方程式为_______ 。
 和CaO等)制备软磁性材料
和CaO等)制备软磁性材料 。其主要实验流程如下:
。其主要实验流程如下:
(1)酸浸:用一定浓度的
 溶液浸取铁泥中的铁元素。若其他条件不变,实验中能加快铁元素浸出速率的措施有
溶液浸取铁泥中的铁元素。若其他条件不变,实验中能加快铁元素浸出速率的措施有(2)还原:向“酸浸”后的滤液中加入过量铁粉,使
 完全转化为
完全转化为 。“还原”过程中发生的主要反应的离子方程式为
。“还原”过程中发生的主要反应的离子方程式为 完全被还原的实验方案为
完全被还原的实验方案为(3)除杂:向“还原”后的滤液中加入
 溶液,使
溶液,使 转化为
转化为 沉淀除去。若溶液的酸性较强,将会导致
沉淀除去。若溶液的酸性较强,将会导致 沉淀不完全,其原因是
沉淀不完全,其原因是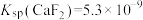 ,
,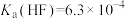 )。
)。(4)沉铁:将提纯后的
 溶液与氨水—
溶液与氨水— 混合溶液反应,生成
混合溶液反应,生成 沉淀。生成
沉淀。生成 沉淀的离子方程式为
沉淀的离子方程式为
您最近一年使用:0次
6 . 已知相同温度下, 。某温度下,饱和溶液中
。某温度下,饱和溶液中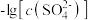 、
、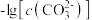 、与
、与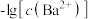 的关系如图所示。
的关系如图所示。
 。某温度下,饱和溶液中
。某温度下,饱和溶液中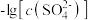 、
、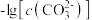 、与
、与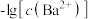 的关系如图所示。
的关系如图所示。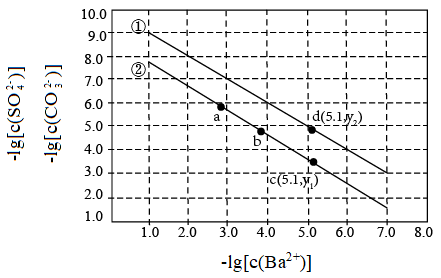
A.曲线①代表 的沉淀溶解曲线 的沉淀溶解曲线 |
B.该温度下 的 的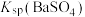 值为 值为 |
C.加适量 固体可使溶液由a点变到b点 固体可使溶液由a点变到b点 |
D. 时两溶液中 时两溶液中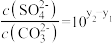 |
您最近一年使用:0次
2021-06-11更新
|
25675次组卷
|
71卷引用:第八章能力提升检测卷(精练)-2022年高考化学一轮复习讲练测
(已下线)第八章能力提升检测卷(精练)-2022年高考化学一轮复习讲练测(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第24讲 沉淀溶解平衡(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)2021年高考全国甲卷化学试题变式题(已下线)专题27 难溶电解质的溶解平衡(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练(已下线)专题12 水溶液中的离子平衡-备战2022年高考化学学霸纠错(全国通用)(已下线)第八单元 水溶液中的离子平衡(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)2021年高考全国甲卷化学真题重庆市缙云教育联盟2020-2021学年高二下学期期末质量检测化学试题湖南省邵阳邵东市第一中学2022届高三上学期第一次月考化学试题河北省石家庄市第一中学2021-2022学年高二上学期10月月考化学试卷辽宁省东北育才学校2021-2022学年高二上学期期中考试化学试题河北省石家庄市第二中学2022届高三上学期11月第三次考试化学试题(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版选修4)浙江省绍兴市诸暨中学2021-2022学年高二上学期期中考试(实验班)化学试题浙江省绍兴市诸暨中学2021-2022学年高二上学期期中考试(平行班)化学试题(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题13 水溶液中的离子平衡-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题07 电解质溶液—2022年高考化学二轮复习讲练测(全国版)-练习福建省三明第一中学2021-2022学年高二上学期第二次月考化学试题(已下线)卷11 溶液中的离子平衡-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)(已下线)卷09 水溶液中的离子平衡-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2022年高考化学临考题号押题(全国卷)(已下线)回归教材重难点07 图像数据和结果的分析-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)回归教材重难点04 水溶液中的离子平衡-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题6 Ksp专练(已下线)专题10水溶液中的离子平衡-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题10水溶液中的离子平衡-五年(2018~2022)高考真题汇编(全国卷)(已下线)考点29 沉淀溶解平衡-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第33练 沉淀溶解平衡-2023年高考化学一轮复习小题多维练(全国通用)(已下线)微专题39 水溶液中平衡图像的拓展与探析-备战2023年高考化学一轮复习考点微专题(已下线)第24讲 沉淀溶解平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)微专题42 四大平衡常数的计算与应用-备战2023年高考化学一轮复习考点微专题(已下线)专题06 水溶液中的离子平衡(讲)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题22 沉淀溶解平衡及图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 题型专攻4 电解质溶液各类图像的分析(已下线)第八章 水溶液中的离子反应与平衡 第53讲 沉淀溶解平衡图像的分析(已下线)题型142 有关沉淀溶解平衡图像(已下线)素养卷05 电解质溶液中微粒变化图像题-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)题型27 沉淀溶解平衡常数及其应用图象(已下线)专题16 水溶液中的离子平衡(已下线)专题16 水溶液中的离子平衡(已下线)专题09 水溶液中的离子平衡-2023年高考化学真题题源解密(新高考专用)(已下线)考点29 沉淀溶解平衡(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点4 沉淀溶解平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)云南省大理白族自治州实验中学2021-2022学年高二上学期10月月考化学试题山东省泰安市2021-2022学年高三下学期3月一模考试化学试题吉林省长春市2022届高三质量监测线上考试(三)理综化学试题(已下线)【奋进985】08-备战2022年高考化学名校进阶模拟卷(通用版)云南省丽江市第一高级中学2021-2022学年高二下学期4月月考化学试题河南省商丘市五校2021-2022学年高二下学期5月联考化学试题黑龙江省饶河县高级中学2021-2022学年上学期期末考试化学试题云南省玉溪市通海县第一中学2021-2022学年高二上学期期末考试化学试题第三章 综合拔高练江苏省海安市立发中学2022-2023学年高三上学期学情检测卷(二)化学试题辽宁省沈阳市五校协作体2022-2023学年高二上学期期中考试化学试题广东省华南师范大学附属中学2022-2023学年高二上学期阶段检测化学B卷试题吉林省长春市第二实验中学2022-2023学年高二上学期期末考试化学试题湖南省株洲市第二中学2022-2023学年高二上学期期中考试化学试题湖南省株洲九方中学2022-2023学年高二上学期期中考试化学试题湖南省株洲市第八中学2022-2023学年高二上学期期中考试化学试题湖南省岳阳市华容县普通高中2023届高三新高考适应性考试化学试题江西省赣州市重点中学九校联盟2022-2023学年高二下学期第一次月考化学试题黑龙江省齐齐哈尔市讷河市第二中学等3校2022-2023学年高二下学期开学考试化学试题微专题(12) 电解质溶液中的两类特殊图像微专题(九)——沉淀溶解平衡曲线广东省广州市真光中学2023-2024学年高二上学期12月月考化学试题山东省菏泽市鄄城县第一中学2023-2024学年高三上学期1月月考化学试题山东省青岛第一中学2023-2024学年高二上学期第二次月考化学试卷福建省福建师范大学附属中学2023-2024学年高三上学期开学考化学试题
解题方法
7 . 一定温度下,难溶电解质在水中存在沉淀溶解和生成的平衡,常用溶度积Ksp来表示溶解程度的大小,如Ksp(AgCl)=c(Ag+)·c(Cl—)。常温下用0.1000mol/L的AgNO3标准溶液(pH≈5)分别滴定20.00mL0.1000mol/L的NaCl溶液和NaBr溶液,混合溶液的pAg[定义为pAg=—lgc(Ag+)]与AgNO3溶液体积的变化关系如图所示。
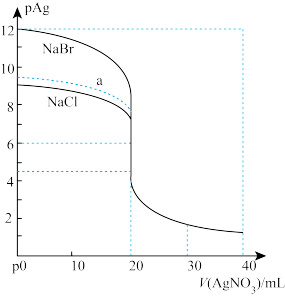
下列说法不正确的是

下列说法不正确的是
| A.Ksp(AgCl)>Ksp(AgBr) |
| B.当V(AgNO3溶液)=20mL时,NaBr溶液中:c(Ag+)+c(H+)=c(Br—)+c(OH—) |
C.当V(AgNO3溶液)=30mL时,NaCl溶液中:c(NO )>c(Na+)>c(Ag+)>c(Cl—)>c(H+) )>c(Na+)>c(Ag+)>c(Cl—)>c(H+) |
| D.相同实验条件下,若改用10.00mL0.2000mol/LNaCl溶液,则滴定曲线(滴定终点前)可能变为a |
您最近一年使用:0次
2021-06-02更新
|
883次组卷
|
6卷引用:第26讲 难溶电解质的溶解平衡(精练)-2022年高考化学一轮复习讲练测
(已下线)第26讲 难溶电解质的溶解平衡(精练)-2022年高考化学一轮复习讲练测(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)专题12 水溶液中的离子平衡-备战2022年高考化学学霸纠错(全国通用)浙江省名校新高考研究联盟(Z20联盟)2021届高三第三次联考化学试题(已下线)【浙江新东方】高三化学20210527-004【2021】【高三下】【模拟考】【Z20】【高中化学】【李鼎收集】(已下线)考点29 沉淀溶解平衡-备战2023年高考化学一轮复习考点帮(全国通用)
名校
解题方法
8 . 用0.1000mol·L-1AgNO3溶液滴定50.00mL0.0500mol·L-1KI溶液的滴定曲线如图所示。
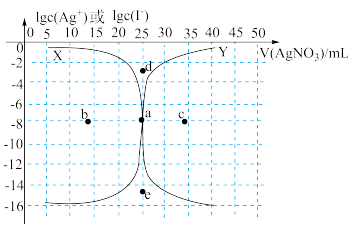
已知:Ksp(AgI)=4×10-16。下列有关描述正确的是

已知:Ksp(AgI)=4×10-16。下列有关描述正确的是
| A.曲线x代表lgc(Ag+)随v(AgNO3)变化而变化的曲线 |
| B.a点表示反应终点,其坐标是(25.00,-7.7) |
| C.相同实验条件下,若改为0.0500mol·L-1KCl溶液,反应终点由a向e方向移动 |
| D.相同实验条件下,若改为0.0500mol·L-1AgNO3溶液,反应终点a向b方向移动 |
您最近一年使用:0次
2021-05-31更新
|
732次组卷
|
4卷引用:第26讲 难溶电解质的溶解平衡(精练)-2022年高考化学一轮复习讲练测
(已下线)第26讲 难溶电解质的溶解平衡(精练)-2022年高考化学一轮复习讲练测四川省达州市普通高中2021届高三第二次诊断性测试理科综合化学试题河北省石家庄市第二中学2021-2022学年高三上学期九月第四次考试化学试题辽宁省实验中学2021-2022学年度高三上学期第三次阶段测试化学试题
9 . 常温下,用0.100mol•L-1的NH4SCN标准溶液滴定25.00mL未知浓度的AgNO3溶液,以NH4Fe(SO4)2•12H2O为指示剂,测得溶液中pSCN=-lgc(SCN)、pAg=‒lgc(Ag+)随加入NH4SCN溶液的体积变化如图所示。已知: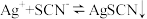 ,Ksp(Ag2CrO4)=1.0×10-12,Ksp(Ag2SO4)=1.4×10-5,Ksp(Ag2CO3)=8×10-12.回答下列问题:
,Ksp(Ag2CrO4)=1.0×10-12,Ksp(Ag2SO4)=1.4×10-5,Ksp(Ag2CO3)=8×10-12.回答下列问题:

(1)滴定终点的现象:_______ 。
(2)该温度下AgSCN溶度积常数Ksp=_______ 。
(3)为防止指示剂失效,溶液应维持____ (填“酸性”或“碱性”,),若用K2CrO4做指示剂,应控制其浓度不超过___ 。(假设c(Ag+)≤10-5mol·L-1,完全沉淀)
(4)当加入15.00mLNH4SCN溶液时,悬浊液中生成少量的Ag2SO4,则此时溶液中c( )=
)=___ 。
(5)滴定终点,再加入10mL0.005mol·L-1的Na2CO3溶液,__ (填“有”或“无”,)沉淀生成。
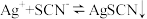 ,Ksp(Ag2CrO4)=1.0×10-12,Ksp(Ag2SO4)=1.4×10-5,Ksp(Ag2CO3)=8×10-12.回答下列问题:
,Ksp(Ag2CrO4)=1.0×10-12,Ksp(Ag2SO4)=1.4×10-5,Ksp(Ag2CO3)=8×10-12.回答下列问题:
(1)滴定终点的现象:
(2)该温度下AgSCN溶度积常数Ksp=
(3)为防止指示剂失效,溶液应维持
(4)当加入15.00mLNH4SCN溶液时,悬浊液中生成少量的Ag2SO4,则此时溶液中c(
 )=
)=(5)滴定终点,再加入10mL0.005mol·L-1的Na2CO3溶液,
您最近一年使用:0次
名校
解题方法
10 . 测定溶液中Cl-的浓度时,常用标准AgNO3溶液滴定,K2CrO4作指示剂。根据如下关于AgCl、Ag2CrO4的溶度积图,判断下列说法正确 的是
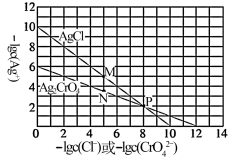

| A.P点时,二者的溶度积常数相同 |
| B.M点时,对AgCl溶液而言为饱和状态,对Ag2CrO4溶液而言为过饱和状态 |
C.向c(Cl-)=c( )=1×10-2mol·L-1的混合溶液中逐滴滴加1×10-3mol·L-1AgNO3溶液,振荡,先产生AgCl沉淀,当溶液中c(Cl-)降至1×10-5mol·L-1时,c( )=1×10-2mol·L-1的混合溶液中逐滴滴加1×10-3mol·L-1AgNO3溶液,振荡,先产生AgCl沉淀,当溶液中c(Cl-)降至1×10-5mol·L-1时,c( )=1×10-3.5mol·L-1 )=1×10-3.5mol·L-1 |
| D.当Cl-按化学计量比完全反应后,过量的一滴AgNO3溶液与K2CrO4反应沉淀颜色有明显变化。 |
您最近一年使用:0次
2021-05-28更新
|
1305次组卷
|
7卷引用:考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)
(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)河南省实验中学2021届高三5月第四次模拟考试理综化学试题内蒙古赤峰二中2021-2022学年高三上学期第一次月考化学试题(已下线)专题11 水溶液中的离子反应与平衡-2023年高考化学一轮复习小题多维练(全国通用)(已下线)题型40 沉淀滴定—直接滴定法、莫尔法湖南省永州市第四中学2022届高三第三次调研考试化学试题第三章 章末训练



