1 . 利用下列装置(夹持装置略)进行实验,能达到目的的是
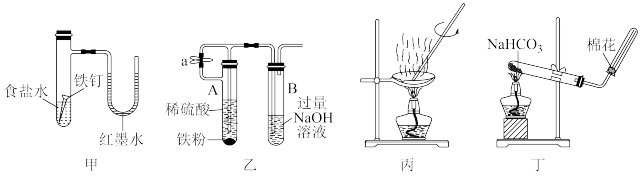

| A.装置甲验证铁的析氢腐蚀 |
| B.装置乙制备氢氧化亚铁 |
| C.装置丙蒸发氯化镁溶液,制备无水氯化镁 |
| D.装置丁制备并收集二氧化碳 |
您最近一年使用:0次
名校
2 . 利用下列实验装置不能完成相应实验的是
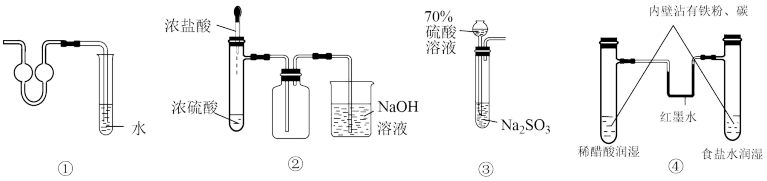

| A.装置①可用作少量氨气的尾气吸收装置 | B.装置②制取收集并吸收HCl |
| C.装置③亚硫酸钠与70%硫酸溶液制备SO2 | D.装置④模拟铁的腐蚀 |
您最近一年使用:0次
2022-02-27更新
|
441次组卷
|
4卷引用:辽宁省沈阳市第二中学2021-2022学年高三下学期学期初考试化学试题
辽宁省沈阳市第二中学2021-2022学年高三下学期学期初考试化学试题(已下线)押新高考卷05题 化学实验基础-备战2022年高考化学临考题号押题(新高考通版)辽宁省沈阳市第二中学2022-2023学年高三上学期12月阶段测试化学试题吉林省白山市抚松县第一中学2022-2023学年高三上学期期末考试化学试题
名校
解题方法
3 . 如图所示是原电池的装置图。请回答:

(1)若C为NaCl溶液,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为___________ ;反应进行一段时间后,向两电极附近溶液滴加酚酞试剂,___________ (填“A”或“B”)电极周围溶液显红色。
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(正极)极材料为___________ ,B(负极)极材料为___________ ,溶液C为___________ 。
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:

电池总反应为2CH3OH+3O2=2CO2+4H2O,则d电极是___________ (填“正极”或“负极”),c电极的反应方程式为___________ 。若线路中转移1mol电子,则上述CH3OH燃料电池消耗的O2在标准状况下的体积为___________ L。

(1)若C为NaCl溶液,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(正极)极材料为
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:

电池总反应为2CH3OH+3O2=2CO2+4H2O,则d电极是
您最近一年使用:0次
4 . 铁在地壳中的含量很高,铁及其化合物也是人们日常生活中应用广泛的一类物质。请根据实验回答下列问题:
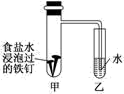
Ⅰ、将经过酸洗除锈的铁钉,用饱和食盐水浸泡后,放入如图所示装置中:
(1)发生的电化学腐蚀类型是___________ ,负极反应式为___________ 。
(2)过一段时间,乙试管中观察到的现象是___________
Ⅱ、实验室配置0.01mol•L﹣1FeCl2溶液时,需向溶液中滴加几滴稀盐酸,其目的是___________ ,还需要加入少量铁粉,其目的是___________ 。FeCl2溶液中离子浓度由大到小的顺序是___________ 。
Ⅲ、高铁酸盐是一种新型的净水剂,如高铁酸钾(K2FeO4),其净水过程中既表现出强氧化性,又表现了强吸附性,则K2FeO4与水反应的离子方程式为___________ 。
Ⅳ、工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)为原料制备高档颜料——铁红(Fe2O3),具体生产流程如下:

试回答下列问题:
(1)步骤1酸溶后的不溶物为___________ 。
(2)步骤Ⅳ中应选用___________ 试剂调节溶液的pH(填字母编号)。
A.稀硝酸 B.氢氧化钠溶液 C.高锰酸钾溶液 D.氨水
(3)检验步骤Ⅲ已经进行完全的试剂是___________ 。
(4)步骤Ⅴ中,FeCO3达到沉淀溶解平衡时,若室温下测得溶液的pH为9.5,c(Fe2+)=1×10—6mol/L。试判断所得的FeCO3中是否含有Fe(OH)2___________ (填“是”或“否”),请通过简单计算说明理由___________ (已知:Ksp[Fe(OH)2]=4.9×10—17)

Ⅰ、将经过酸洗除锈的铁钉,用饱和食盐水浸泡后,放入如图所示装置中:
(1)发生的电化学腐蚀类型是
(2)过一段时间,乙试管中观察到的现象是
Ⅱ、实验室配置0.01mol•L﹣1FeCl2溶液时,需向溶液中滴加几滴稀盐酸,其目的是
Ⅲ、高铁酸盐是一种新型的净水剂,如高铁酸钾(K2FeO4),其净水过程中既表现出强氧化性,又表现了强吸附性,则K2FeO4与水反应的离子方程式为
Ⅳ、工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)为原料制备高档颜料——铁红(Fe2O3),具体生产流程如下:

试回答下列问题:
(1)步骤1酸溶后的不溶物为
(2)步骤Ⅳ中应选用
A.稀硝酸 B.氢氧化钠溶液 C.高锰酸钾溶液 D.氨水
(3)检验步骤Ⅲ已经进行完全的试剂是
(4)步骤Ⅴ中,FeCO3达到沉淀溶解平衡时,若室温下测得溶液的pH为9.5,c(Fe2+)=1×10—6mol/L。试判断所得的FeCO3中是否含有Fe(OH)2
您最近一年使用:0次
名校
解题方法
5 . 下列电化学装置正确且能达到目的的是
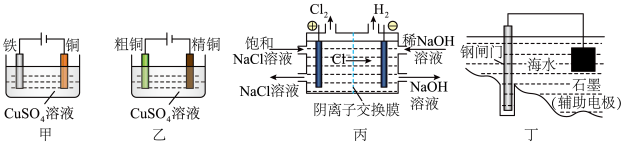

| A.用装置甲在铁制品表面镀铜 | B.用装置乙电解精炼铜 |
| C.用装置丙制备NaOH和氯气 | D.用装置丁保护钢闸门 |
您最近一年使用:0次
2020-07-21更新
|
553次组卷
|
10卷引用:江苏省苏州市2019-2020学年高二下学期学业质量阳光指标调研化学试题
江苏省苏州市2019-2020学年高二下学期学业质量阳光指标调研化学试题江苏省苏州市2019-2020学年高二下学期期末考试化学试题江苏省扬州市扬州中学2021届高三开学检测化学试题江苏省苏州外国语中学2020-2021学年高二下学期3月月考化学试题福建省仙游一中、莆田二中、莆田四中2020-2021学年高二上学期期末联考化学试题江苏省镇江中学2020-2021学年高二上学期期末考试化学试题河南省南阳市2022届高三上学期期中考试化学试题江苏省昆山中学2022-2023学年高一下学期5月月考化学试题江苏省苏州市苏州大学附属中学2023-2024学年高二上学期10月月考化学试题18 2024年苏州高新区吴县高级中学高二3月月考
6 . 关于下列各实验装置的叙述中,错误的是()
A. 装置可用于分离蔗糖和葡萄糖,且烧杯中的清水应多次更换 装置可用于分离蔗糖和葡萄糖,且烧杯中的清水应多次更换 |
B. 装置可用于制备少量Fe(OH)2沉淀,并保持较长时间白色 装置可用于制备少量Fe(OH)2沉淀,并保持较长时间白色 |
C. 装置可用从a处加水的方法检验的气密性,原理为液差法 装置可用从a处加水的方法检验的气密性,原理为液差法 |
D. 装置用于研究钢铁的吸氧腐蚀,一段时间后导管末端会进入一段水柱 装置用于研究钢铁的吸氧腐蚀,一段时间后导管末端会进入一段水柱 |
您最近一年使用:0次
7 . I.肼(N2H4)又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料。 已知在25℃、l0lkPA时,16gN2H4在氧气中完全燃烧生成氮气和H2O,放出热量312kJ。
(1)该条件下,N2H4完全燃烧的热化学方程式为______________
(2)传统制备肼的方法是以NAClO氧化NH3,制得肼的稀溶液,该反应的方程式为______________
II.钢铁工业是国家工业的基础。请回答钢铁腐蚀、防护过程中的有关问题。
(1)铁在潮湿的空气中容易被腐蚀,写出铁发生电化学腐蚀时,负极的电极反应式______________
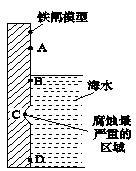
(2)下图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。图中A、B、C、D四个区域,生成铁锈最多的是_______ (填字母)
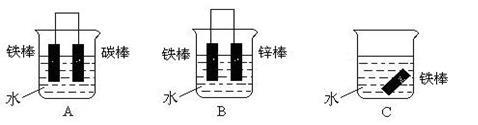
(3)下列各个装置中铁棒被腐蚀由难到易的顺序是______ (填字母)
(1)该条件下,N2H4完全燃烧的热化学方程式为
(2)传统制备肼的方法是以NAClO氧化NH3,制得肼的稀溶液,该反应的方程式为
II.钢铁工业是国家工业的基础。请回答钢铁腐蚀、防护过程中的有关问题。
(1)铁在潮湿的空气中容易被腐蚀,写出铁发生电化学腐蚀时,负极的电极反应式
(2)下图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。图中A、B、C、D四个区域,生成铁锈最多的是

(3)下列各个装置中铁棒被腐蚀由难到易的顺序是

您最近一年使用:0次
解题方法
8 . 某工程技术人员在检测维修高铁时发现,某段铁轨大面积锈蚀,周围大面积森林枯萎。经调查发现附近有一个水泥厂,生产水泥原料是煤矸石,煅烧煤矸石产生二氧化硫污染空气形成酸雨造成的。政府部门为了我国国民的人身安全果断关闭水泥厂。
(1)用化学方程式表示SO2形成硫酸型酸雨的反应: 。
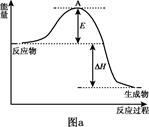

(2)已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=- 99 kJ/mol。2SO2+O2 2SO3反应过程的能量变化如图a所示。
2SO3反应过程的能量变化如图a所示。
①图a中ΔH= kJ/mol;该反应通常用V2O5作催化剂,加V2O5会使图a中A点降低,理由是 。
②L(L1、L2)、X可分别代表压强或温度。图b表示L一定时,SO2(g)的平衡转化率随X的变化关系。
a.X代表的物理量是 。
b.判断L1、L2的大小关系,并简述理由: 。
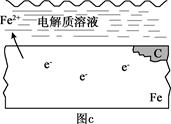
(3)钢铁锈蚀图示如图c所示:
① 用箭头画出图c中电子的运动方向
② 请你分析高铁铁轨锈蚀的原因是 。
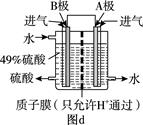
(4)我国的科技人员为了消除SO2的污染,利用原电池原理,变废为宝,设计由SO2和O2来制备硫酸,设计装置如图d所示,电极A、B为多孔的材料。
① A极为 (填“正极”或“负极”)。
② B极的电极反应式是 。
(1)用化学方程式表示SO2形成硫酸型酸雨的反应: 。


(2)已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=- 99 kJ/mol。2SO2+O2
 2SO3反应过程的能量变化如图a所示。
2SO3反应过程的能量变化如图a所示。①图a中ΔH= kJ/mol;该反应通常用V2O5作催化剂,加V2O5会使图a中A点降低,理由是 。
②L(L1、L2)、X可分别代表压强或温度。图b表示L一定时,SO2(g)的平衡转化率随X的变化关系。
a.X代表的物理量是 。
b.判断L1、L2的大小关系,并简述理由: 。
(3)钢铁锈蚀图示如图c所示:
① 用箭头画出图c中电子的运动方向
② 请你分析高铁铁轨锈蚀的原因是 。


(4)我国的科技人员为了消除SO2的污染,利用原电池原理,变废为宝,设计由SO2和O2来制备硫酸,设计装置如图d所示,电极A、B为多孔的材料。
① A极为 (填“正极”或“负极”)。
② B极的电极反应式是 。
您最近一年使用:0次



