名校
解题方法
1 . 短周期主族元素W、X、Y、Z原子序数依次增大,最外层电子数之和为15。W与Y可形成原子个数比为 的分子,且该分子含有18个电子。基态Z原子
的分子,且该分子含有18个电子。基态Z原子 轨道上有3个电子。下列说法正确的是
轨道上有3个电子。下列说法正确的是
 的分子,且该分子含有18个电子。基态Z原子
的分子,且该分子含有18个电子。基态Z原子 轨道上有3个电子。下列说法正确的是
轨道上有3个电子。下列说法正确的是A.原子半径: | B.Y的第一电离能比同周期相邻元素的大 |
C.氢化物的沸点: | D.Z元素最高价氧化物对应的水化物为强酸 |
您最近一年使用:0次
名校
解题方法
2 . 下列化学用语表述正确的是
A. 的电子式: 的电子式: | B.中子数为18的氧原子: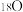 |
C.基态 原子的价电子排布式: 原子的价电子排布式: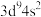 | D. 的空间构型:平面三角形 的空间构型:平面三角形 |
您最近一年使用:0次
名校
解题方法
3 . 氧化锌广泛应用于有机高分子材料、医药、食品等领域。以氧化锌烟灰(含 及少量
及少量 、
、 、
、 等)为原料制备氧化锌的工艺流程如下:
等)为原料制备氧化锌的工艺流程如下:

已知:用有机溶剂 从水溶液中萃取A时,
从水溶液中萃取A时,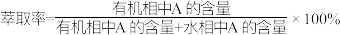
(1)为了提高酸浸效果,可采取的措施有______________________ (任写一点)。
(2)“滤渣1”的主要成分除了 还有
还有_________________________________ 。
(3)“沉铁”操作时不能用 代替
代替 ,原因是
,原因是_________________________________ 。
(4)若 、
、 时,用
时,用 萃取
萃取 溶液,
溶液, (水相)
(水相)
 (有机相)的平衡常数
(有机相)的平衡常数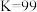 ,则用等体积的
,则用等体积的 一次性萃取
一次性萃取 溶液,
溶液, 萃取率为
萃取率为___________ (答案保留3位有效数字)
(5)“沉锌”时,可生成碱式碳酸锌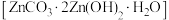 固体,请写出该反应的离子方程式
固体,请写出该反应的离子方程式_________________________________ 。
(6)锌可形成多种配合物。某种含锌配合物一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图1所示。请画出基态 的价电子排布图
的价电子排布图______________________ , 的配位数为
的配位数为___________ ;甘氨酸(如图2)易溶于水,原因是______________________ 。

 及少量
及少量 、
、 、
、 等)为原料制备氧化锌的工艺流程如下:
等)为原料制备氧化锌的工艺流程如下:
已知:用有机溶剂
 从水溶液中萃取A时,
从水溶液中萃取A时,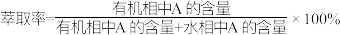
(1)为了提高酸浸效果,可采取的措施有
(2)“滤渣1”的主要成分除了
 还有
还有(3)“沉铁”操作时不能用
 代替
代替 ,原因是
,原因是(4)若
 、
、 时,用
时,用 萃取
萃取 溶液,
溶液, (水相)
(水相)
 (有机相)的平衡常数
(有机相)的平衡常数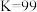 ,则用等体积的
,则用等体积的 一次性萃取
一次性萃取 溶液,
溶液, 萃取率为
萃取率为(5)“沉锌”时,可生成碱式碳酸锌
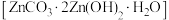 固体,请写出该反应的离子方程式
固体,请写出该反应的离子方程式(6)锌可形成多种配合物。某种含锌配合物一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图1所示。请画出基态
 的价电子排布图
的价电子排布图 的配位数为
的配位数为
您最近一年使用:0次
4 . 碳量子点(CDs)是一种尺寸小于10纳米,含有N、O等杂原子的新型碳基纳米材料,在紫外光照射下,产生荧光。居家利用香蕉皮等果蔬厨余物制备碳量子点的流程如图:

下列叙述不正确的是

下列叙述不正确的是
| A.碳量子点是碳的一种新型单质 |
| B.产生荧光与电子跃迁有关 |
| C.果蔬厨余物含C、H、O等元素 |
| D.所得滤液可产生丁达尔效应 |
您最近一年使用:0次
2023-11-10更新
|
546次组卷
|
3卷引用:广西南宁市第二中学2023-2024学年高一上学期12月测试化学试卷
广西南宁市第二中学2023-2024学年高一上学期12月测试化学试卷 辽宁省大连市金州高级中学2023-2024学年高三上学期期中考试化学试题(已下线)题型05 物质的性质与应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
5 . 化合物I是制备抗肿瘤药物阿法替尼的重要中间体,化合物I的一种合成路线如图。
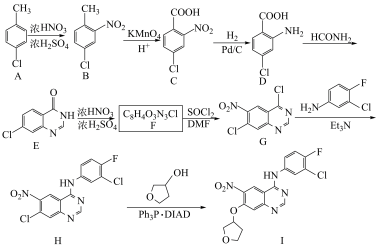
已知:RCH=NH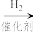 RCH2NH2
RCH2NH2
回答下列问题:
(1)C中含氧官能团的名称是______ 。
(2)A的化学名称为______ 。
(3)B中所含的第二周期元素第一电离能由大到小的顺序是______ 。
(4)F的结构简式为______ ,H→I的反应类型为______ 。
(5)G→H的化学方程式为______ 。
(6)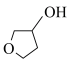 有多种同分异构体,符合下列条件的有
有多种同分异构体,符合下列条件的有______ 种(不考虑立体异构),其中核磁共振氢谱有3组峰,其峰面积比为6∶1∶1的结构简式为______ (写出一种)。
a.能发生银镜反应 b.不含醚键
(7)参考上述合成路线,以HOOCCH2NH2、HCONH2为原料合成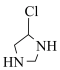 ,合成过程中无机试剂任选
,合成过程中无机试剂任选______ 。

已知:RCH=NH
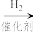 RCH2NH2
RCH2NH2回答下列问题:
(1)C中含氧官能团的名称是
(2)A的化学名称为
(3)B中所含的第二周期元素第一电离能由大到小的顺序是
(4)F的结构简式为
(5)G→H的化学方程式为
(6)
 有多种同分异构体,符合下列条件的有
有多种同分异构体,符合下列条件的有a.能发生银镜反应 b.不含醚键
(7)参考上述合成路线,以HOOCCH2NH2、HCONH2为原料合成
 ,合成过程中无机试剂任选
,合成过程中无机试剂任选
您最近一年使用:0次
2023-10-27更新
|
1054次组卷
|
4卷引用:广西南宁市2024届高三上学期毕业班摸底测试化学试题
广西南宁市2024届高三上学期毕业班摸底测试化学试题广西部分高中2024届高三第一次摸底测试化学试题(已下线)考点3 烃的衍生物的结构与性质(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)热点24 有机合成与推断综合题
6 . W、X、Y、Z是原子序数依次增大的短周期主族元素,其中Z元素基态原子L层电子数是电子层数的3倍。这四种元素组成的化合物(结构如图)可用于合成超分子聚合物。下列说法错误的是


| A.XZ2晶体属于共价晶体 | B.元素W、X、Y都可以与Z形成多种化合物 |
| C.电负性:Z>Y>X>W | D.超分子具有自组装和分子识别的特征 |
您最近一年使用:0次
2023-10-27更新
|
893次组卷
|
5卷引用:广西南宁市2024届高三上学期毕业班摸底测试化学试题
名校
解题方法
7 . 下列化学用语表达正确的是
| A.基态Cu+的价电子排布式:[Ar]3d10 |
B.NH3分子的球棍模型: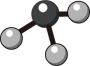 |
C.HClO的电子式: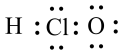 |
D.质量数为238、中子数为146的铀(U)原子: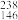 U U |
您最近一年使用:0次
2023-10-27更新
|
1463次组卷
|
9卷引用:广西南宁市2024届高三上学期毕业班摸底测试化学试题
广西南宁市2024届高三上学期毕业班摸底测试化学试题广西部分高中2024届高三第一次摸底测试化学试题新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高三上学期11月月考化学试题甘肃省兰州第一中学2023-2024学年高三上学期12月月考化学试题(已下线)选择题6-10(已下线)热点02 化学用语(已下线)专题01 基本概念-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)专题01 基本概念-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)山西省晋中市平遥县第二中学校2023-2024学年高三上学期适应性训练四理科综合试题
8 . TCCA是一种高效消毒剂,由原子序数依次增大的W、X、Y、Z四种元素构成,且位于两个不同短周期。W元素的K层电子数与其p能级上的电子数相等,基态Y原子s能级电子总数与p能级电子总数相等,其原子半径小于W原子,Z元素的原子半径为同周期主族元素最小。下列叙述正确的是
| A.电负性大小:X>Y>W |
| B.简单离子半径:Z>Y>X |
| C.Y的氢化物的沸点一定高于W的氢化物 |
| D.化合物WY2中,W的杂化方式为sp,为非极性分子 |
您最近一年使用:0次
2023-09-17更新
|
544次组卷
|
2卷引用:广西壮族自治区南宁三中、柳州高中2023-2024学年高三上学期第一次适应性考试化学试题
9 . Fe、Ni元素性质非常相似,属于铁系元素,得到广泛应用,请回答下列问题:
(1)Fe元素位于元素周期表的_______ 区(填分区)。
(2)基态 核外电子排布式为
核外电子排布式为_______ 。
(3)鉴定 的特征反应是将丁二酮肟加入
的特征反应是将丁二酮肟加入 盐溶液中,生成鲜红色的螯合物M,M结构如图所示:
盐溶液中,生成鲜红色的螯合物M,M结构如图所示:

①组成M的五种元素中,除H元素外,另外三种非金属元素第一电离能由大到小的顺序为_______ (填元素符号),其中C原子的杂化类型为_______ 。
②图中各微粒间不存在的作用力有_______ (填标号)。
a.配位键 b.极性键 c.非极性键 d.π键e.离子键 f.氢键
(4)无水三氯化铁( ,相对分子质量162.5)为棕黑色,共价性较强,熔点为307.6℃,沸点约为316℃,易升华,但是400℃以下的气态
,相对分子质量162.5)为棕黑色,共价性较强,熔点为307.6℃,沸点约为316℃,易升华,但是400℃以下的气态 的相对分子质量测定值约为325,可能的原因是
的相对分子质量测定值约为325,可能的原因是_______ 。
(5)一种铁氮化合物具有高磁导率,可用于制电子元件,其晶胞结构如图所示。

①该铁氮化合物的化学式为_______ 。
②在该晶胞结构的另一种表示中,N处于顶点位置,则铁处于_______ 位置。
③若该化合物密度为 ,用
,用 表示阿伏加德罗常数,则晶胞边长为
表示阿伏加德罗常数,则晶胞边长为_______ pm。
(1)Fe元素位于元素周期表的
(2)基态
 核外电子排布式为
核外电子排布式为(3)鉴定
 的特征反应是将丁二酮肟加入
的特征反应是将丁二酮肟加入 盐溶液中,生成鲜红色的螯合物M,M结构如图所示:
盐溶液中,生成鲜红色的螯合物M,M结构如图所示:
①组成M的五种元素中,除H元素外,另外三种非金属元素第一电离能由大到小的顺序为
②图中各微粒间不存在的作用力有
a.配位键 b.极性键 c.非极性键 d.π键e.离子键 f.氢键
(4)无水三氯化铁(
 ,相对分子质量162.5)为棕黑色,共价性较强,熔点为307.6℃,沸点约为316℃,易升华,但是400℃以下的气态
,相对分子质量162.5)为棕黑色,共价性较强,熔点为307.6℃,沸点约为316℃,易升华,但是400℃以下的气态 的相对分子质量测定值约为325,可能的原因是
的相对分子质量测定值约为325,可能的原因是(5)一种铁氮化合物具有高磁导率,可用于制电子元件,其晶胞结构如图所示。

①该铁氮化合物的化学式为
②在该晶胞结构的另一种表示中,N处于顶点位置,则铁处于
③若该化合物密度为
 ,用
,用 表示阿伏加德罗常数,则晶胞边长为
表示阿伏加德罗常数,则晶胞边长为
您最近一年使用:0次
名校
10 . 下列有关化学用语表示正确的是
A.氨基的电子式: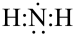 | B.基态铬原子的价层电子排布式:3d4 4s2 |
C.H2O 的 VSEPR 模型: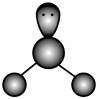 | D.葡萄糖的实验式:C6H12O6 |
您最近一年使用:0次
2023-07-10更新
|
227次组卷
|
2卷引用:广西南宁市第三中学2022-2023学年高二下学期期末考试化学试题



