1 . 四种元素的基态原子的核外电子排布式分别是:①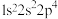 ,②
,②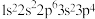 ,③
,③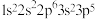 ,④
,④ ,下列说法不正确的是
,下列说法不正确的是
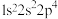 ,②
,②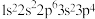 ,③
,③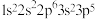 ,④
,④ ,下列说法不正确的是
,下列说法不正确的是| A.最高价含氧酸的酸性:②<③ | B.第一电离能:①>④ |
| C.①②③④都是p区元素 | D.电负性:①>② |
您最近一年使用:0次
2023-05-07更新
|
569次组卷
|
4卷引用:云南省保山市高(完)中C、D类学校2022-2023学年高二下学期6月份联考化学试题
云南省保山市高(完)中C、D类学校2022-2023学年高二下学期6月份联考化学试题北京市昌平区2023届高三下学期第二次统一练习化学试题(已下线)考点巩固卷05 物质结构 元素周期律(2大考点50题)-2024年高考化学一轮复习考点通关卷(新高考通用)北京市第五中学通州分校2023-2024学年高三上学期12月练习二化学试题
名校
2 . W、X、Y、Z是原子序数依次增大的4种短周期元素,其原子结构如表:
下列说法不正确的是
| 元素 | 原子结构 |
| W | 基态原子L层电子数是K层电子数的2倍 |
| X | 原子核外p电子数比s电子数少1 |
| Y | 原子的最外层2p轨道上有2个未成对电子 |
| Z | 原子核外的M层中只有两对成对电子 |
| A.原子半径:Z>X>Y |
| B.第一电离能:X>Y>W |
| C.W的最简单气态氢化物比X的最简单气态氢化物稳定 |
| D.ZY2和WY2在水中的溶解度较大的是ZY2 |
您最近一年使用:0次
2023-05-04更新
|
200次组卷
|
3卷引用:云南省丽江市2022-2023学年高二上学期期末考试化学试题
名校
解题方法
3 . 磷酸铁锂(LiFePO4)主要用做锂离子电池正极材料,下列说法中不正确 的是
| A.基态Li原子含有3种不同运动状态的电子 |
| B.Fe在第四周期第Ⅷ族,位于元素周期表ds区 |
| C.基态O原子核外电子占据的最高能级的电子云轮廓图为哑铃形 |
D.阴离子 的VSEPR模型为四面体形 的VSEPR模型为四面体形 |
您最近一年使用:0次
2023-04-26更新
|
203次组卷
|
3卷引用:云南师范大学附属中学2023-2024学年高二上学期10月月考化学试题
4 . 某种双核钴配合物阳离子的结构如图。X的第一电离能在第二周期主族元素中位居第二,Y的核外电子只有一种运动状态,Z的一种同素异形体是极性分子。下列说法错误的是
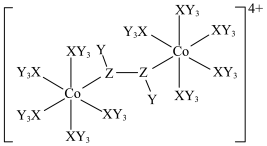
| A.简单氢化物的稳定性:Z>X |
| B.电负性:Z>X>Y |
| C.Co位于元素周期表ds区,在该阳离子中呈+2价 |
| D.从结构推测该配合物阳离子不稳定,且具有一定的氧化性 |
您最近一年使用:0次
2024-04-02更新
|
606次组卷
|
4卷引用:2024届东北三省三校高三下学期第二次联合模拟考试理综重组卷-高中化学
名校
解题方法
5 . 氢键对生命活动具有重要意义。DNA中四种碱基间的配对方式如下图(~代表糖苷键)。下列说法错误的是
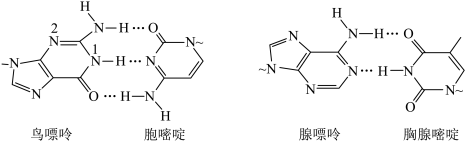

| A.基态氧原子核外的电子有5种不同的空间运动状态 |
| B.鸟嘌呤分子中2号N原子的杂化类型为sp2 |
| C.所涉及的四种元素电负性大小关系: H<C<O<N |
| D.氢键的强度较小,在DNA解旋和复制时容易断裂和形成 |
您最近一年使用:0次
2023-04-15更新
|
457次组卷
|
3卷引用:云南省昆明市云南民族大学附属高级中学2023-2024学年高三上学期期中考试理综化学试题
6 . 2022年诺贝尔化学奖授予美国科学家贝尔托齐、沙普利斯和丹麦科学家莫滕,以表彰他们在发展点击化学和生物正交化学方面的贡献。氯化亚铜是点击化学常用的催化剂,其晶胞结构如图所示,下列有关说法中错误的是

A.基态Cu+价层电子排布图为 |
| B.Cl原子核外电子的运动状态有17种 |
| C.该晶胞中含有4个Cu+利4个Cl- |
| D.Cu+周围等距离且最近的Cu+数为6个 |
您最近一年使用:0次
2024-03-15更新
|
309次组卷
|
3卷引用:云南省长水教育集团2023-2024学年高二下学期质量检测联考化学试题(二)
名校
解题方法
7 . 已知元素X简单气态氢化物和其最高价含氧酸可化合生成一种盐,基态Y原子最外层电子排布为nsnnpn+2。下列说法错误的是
| A.原子半径:X>Y | B.X、Y均属于p区元素 |
| C.X、Y的电负性:X>Y | D.X、Y的简单氢化物热稳定性:X<Y |
您最近一年使用:0次
2022-04-21更新
|
180次组卷
|
6卷引用:云南省巍山彝族回族自治县第二中学2021-2022学年高二下学期6月第三次月考化学试题
8 . 过渡金属及其化合物在生产生活中有着广泛应用。回答下列问题:
(1)过渡元素Co基态原子的核外电子排布式为_______ ;第四电离能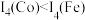 ,其原因是
,其原因是_______ 。
(2)Fe、Fe2+、Fe3+可以与CO、 、
、 、
、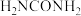 (尿素)等多种配体形成很多的配合物。
(尿素)等多种配体形成很多的配合物。
①配合物 的熔点为-20℃,沸点为103℃,可用于制备纯铁。
的熔点为-20℃,沸点为103℃,可用于制备纯铁。 的结构如图所示。下列关于
的结构如图所示。下列关于 说法不正确的是
说法不正确的是_______ (填序号)。
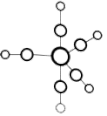
A. 是分子晶体
是分子晶体
B. 中Fe原子的配体与
中Fe原子的配体与 互为等电子体
互为等电子体
C. 中σ键与π键之比为1∶1
中σ键与π键之比为1∶1
D.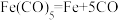 反应中没有新化学键生成
反应中没有新化学键生成
② 的电子式为
的电子式为_______ 。
③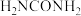 (尿素)中N原子的杂化方式为
(尿素)中N原子的杂化方式为_______ ,组成尿素的4种元素的第一电离能由大到小的顺序为_______ 。
(3)Ni和As形成某种晶体的晶胞图如图所示。其中,大球为Ni,小球为As,距离As最近的Ni构成正三支柱,其中晶胞下方As原子坐标为( ,
, ,
, )。
)。
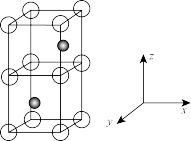
①Ni的配位数为_______ 。
②已知晶胞底面边长为apm,高为cpm,NA为阿伏加德罗常数。则晶胞密度为_______  。
。
(1)过渡元素Co基态原子的核外电子排布式为
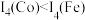 ,其原因是
,其原因是(2)Fe、Fe2+、Fe3+可以与CO、
 、
、 、
、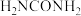 (尿素)等多种配体形成很多的配合物。
(尿素)等多种配体形成很多的配合物。①配合物
 的熔点为-20℃,沸点为103℃,可用于制备纯铁。
的熔点为-20℃,沸点为103℃,可用于制备纯铁。 的结构如图所示。下列关于
的结构如图所示。下列关于 说法不正确的是
说法不正确的是
A.
 是分子晶体
是分子晶体B.
 中Fe原子的配体与
中Fe原子的配体与 互为等电子体
互为等电子体C.
 中σ键与π键之比为1∶1
中σ键与π键之比为1∶1D.
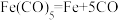 反应中没有新化学键生成
反应中没有新化学键生成②
 的电子式为
的电子式为③
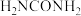 (尿素)中N原子的杂化方式为
(尿素)中N原子的杂化方式为(3)Ni和As形成某种晶体的晶胞图如图所示。其中,大球为Ni,小球为As,距离As最近的Ni构成正三支柱,其中晶胞下方As原子坐标为(
 ,
, ,
, )。
)。
①Ni的配位数为
②已知晶胞底面边长为apm,高为cpm,NA为阿伏加德罗常数。则晶胞密度为
 。
。
您最近一年使用:0次
名校
解题方法
9 . 铜盐中毒可用青霉胺解毒,解毒原理如下: 能与青霉胺形成环状络合物,其结构如图所示。该环状络合物无毒、易溶于水,可经尿液排出。下列说法错误的是
能与青霉胺形成环状络合物,其结构如图所示。该环状络合物无毒、易溶于水,可经尿液排出。下列说法错误的是
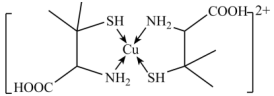
 能与青霉胺形成环状络合物,其结构如图所示。该环状络合物无毒、易溶于水,可经尿液排出。下列说法错误的是
能与青霉胺形成环状络合物,其结构如图所示。该环状络合物无毒、易溶于水,可经尿液排出。下列说法错误的是
A.比较硫化氢与氨气键角的大小: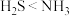 |
| B.第二周期主族元素中,第一电离能大于N的元素有1种 |
| C.该环状络合物易溶于水的主要原因是其与水可形成分子间氢键 |
| D.该环状络合物中,VSEPR模型为四面体或正四面体的非金属原子共有13个 |
您最近一年使用:0次
10 . 下列关于原子结构与元素周期表的说法正确的是
| A.电负性最大的元素位于周期表的左下角 |
| B.某基态原子的价电子排布式为4s24p1,该元素位于周期表第四周期第ⅢA族 |
| C.2s轨道在空间呈哑铃形 |
| D.第四能层最多可容纳16个电子 |
您最近一年使用:0次
2022-12-10更新
|
98次组卷
|
2卷引用:云南师范大学附属中学2023-2024学年高二上学期10月月考化学试题



