名校
解题方法
1 . 氨硼烷( )的分子结构和乙烷相似,是一种固体储氢材料。下列关于氨硼烷的说法,错误的是
)的分子结构和乙烷相似,是一种固体储氢材料。下列关于氨硼烷的说法,错误的是
 )的分子结构和乙烷相似,是一种固体储氢材料。下列关于氨硼烷的说法,错误的是
)的分子结构和乙烷相似,是一种固体储氢材料。下列关于氨硼烷的说法,错误的是A.第一电离能: |
| B.N和B元素都位于周期表的P区 |
| C.氨硼烷是极性分子 |
| D.氨硼烷中N原子和B原子之间形成了配位键 |
您最近一年使用:0次
2023-07-08更新
|
161次组卷
|
3卷引用:云南省玉溪市2022-2023学年高二下学期期末考试化学试题
云南省玉溪市2022-2023学年高二下学期期末考试化学试题云南省玉溪第三中学2022-2023学年高二下学期期末教学质量检测化学试题(已下线)专题01 物质的结构与性质-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(人教版2019)
2 . 铜是重要的战略资源,云南是我国铜资源储量较高的省份之一,回答下列问题:
(1)铜在周期表中位于第______ 族(填族序数),属于______ 区。
(2)铜可以形成多种配合物。
① 的核外电子排布式是
的核外电子排布式是______ ,过渡金属离子与水分子形成配合物时,若d轨道全空或全满时,化合物无颜色,否则有颜色。据此判断,
______ (填“有”或“无”)颜色。
② 可形成多种配合物,如
可形成多种配合物,如 ,若其中两个
,若其中两个 被
被 替换,得到的配合物只有两种结构,则
替换,得到的配合物只有两种结构,则 的空间构型是
的空间构型是______ , 中N原子的杂化方式是
中N原子的杂化方式是______ ,空间构型是______ 。
(3)铜与金等金属及合金可用于生产石墨烯的催化剂,如图是一种铜金合金的晶胞示意图:

①Cu原子的配位数是______ 。
②原子坐标参数,表示晶胞内部各原子的相对位置,其中原子坐标参数A为 ;B为
;B为 ;C为
;C为 。则D原子的坐标参数为
。则D原子的坐标参数为______ 。
(1)铜在周期表中位于第
(2)铜可以形成多种配合物。
①
 的核外电子排布式是
的核外电子排布式是
②
 可形成多种配合物,如
可形成多种配合物,如 ,若其中两个
,若其中两个 被
被 替换,得到的配合物只有两种结构,则
替换,得到的配合物只有两种结构,则 的空间构型是
的空间构型是 中N原子的杂化方式是
中N原子的杂化方式是(3)铜与金等金属及合金可用于生产石墨烯的催化剂,如图是一种铜金合金的晶胞示意图:

①Cu原子的配位数是
②原子坐标参数,表示晶胞内部各原子的相对位置,其中原子坐标参数A为
 ;B为
;B为 ;C为
;C为 。则D原子的坐标参数为
。则D原子的坐标参数为
您最近一年使用:0次
3 . 短周期主族元素X、Y、Z、Q、W原子序数依次增大,X的一种核素常用于测定文物的年代,Z的一种单质常用来消毒杀菌,Q最外层有2个电子,W和Y同族。下列说法不正确的是
| A.第一电离能:X>Y>Z | B.简单氢化物的沸点:Y>W |
| C.最高价氧化物对应水化物的酸性:Y>X | D.X、Y、Z的最简单氢化物的杂化方式均为 杂化 杂化 |
您最近一年使用:0次
解题方法
4 . 某元素基态原子价电子排布式为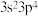 ,下列说法不正确的是
,下列说法不正确的是
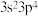 ,下列说法不正确的是
,下列说法不正确的是| A.该原子位于周期表p区 |
| B.该元素的最高正价为+4价 |
| C.该基态原子中存在两个未成对电子 |
| D.该元素最简单氢化物的空间构型是V形 |
您最近一年使用:0次
名校
5 .  的结构如图所示。下列说法正确的是
的结构如图所示。下列说法正确的是

 的结构如图所示。下列说法正确的是
的结构如图所示。下列说法正确的是
| A.O的第一电离能低于S |
B.相同条件下, 的稳定性比 的稳定性比 强 强 |
C.基态 的价层电子排布式为 的价层电子排布式为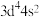 |
| D.该物质中存在的化学键类型有:离子键、共价键、氢键 |
您最近一年使用:0次
2023-07-06更新
|
534次组卷
|
3卷引用:云南省昆明市2022-2023学年高二下学期7月期末化学试题
6 . 短周期主族元素X、Y、Z、W原子序数依次增大,X的简单气态氢化物溶于水呈碱性,基态Y原子无未成对电子,Z的某种氧化物具有漂白性。下列说法正确的是
| A.电负性:W<Z<X |
B.原子半径: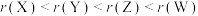 |
| C.最高价氧化物对应水化物的酸性:W<Z |
| D.Y的单质与X、Z、W的单质均能发生反应 |
您最近一年使用:0次
7 . 下列说法正确的是
 |  | 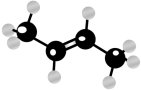 | 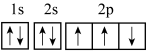 |
| A.基态锂原子最高能级的电子云轮廓图 | B. 分子的空间填充模型 分子的空间填充模型 | C.顺-2-丁烯的分子结构模型 | D.基态氮原子的电子排布图 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如下表:
下列叙述不正确的是
| 元素 | 相关信息 |
| X | X的基态原子L层电子数是K层电子数的2倍 |
| Y | Y的基态原子最外层电子排布式为:nsnnpn+2 |
| Z | Z存在质量数为23,中子数为12的核素 |
| W | W有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
| A.W基态原子价电子排布式为3d64s2 |
| B.Z所在周期中第一电离能最大的主族元素是Cl |
| C.X的电负性比Y的大 |
| D.XY2分子的空间结构是直线形 |
您最近一年使用:0次
9 . B、N、F、Ti、Fe、As、Se等元素及其化合物的研究对工农业生产意义重大,回答下列问题:
(1)写出Ti基态原子的电子排布式_____ 。
(2)基态Fe2+与Fe3+离子中未成对的电子数之比为_____ 。
(3)VIA族元素中O、S、Se的电负性由大到小的顺序为_____ 。
(4)BF3的空间构型为_____ ;其中B原子采用_____ 杂化,根据对角线规则,B的一些化学性质与元素_____ 的相似。
(5)元素As与N同族。As的氢化物的沸点比NH3的_____ (填“高”或“低”),其判断理由是_____ 。
(1)写出Ti基态原子的电子排布式
(2)基态Fe2+与Fe3+离子中未成对的电子数之比为
(3)VIA族元素中O、S、Se的电负性由大到小的顺序为
(4)BF3的空间构型为
(5)元素As与N同族。As的氢化物的沸点比NH3的
您最近一年使用:0次
2023-05-04更新
|
284次组卷
|
2卷引用:云南省丽江市2022-2023学年高二上学期期末考试化学试题
名校
10 . W、X、Y、Z是原子序数依次增大的4种短周期元素,其原子结构如表:
下列说法不正确的是
| 元素 | 原子结构 |
| W | 基态原子L层电子数是K层电子数的2倍 |
| X | 原子核外p电子数比s电子数少1 |
| Y | 原子的最外层2p轨道上有2个未成对电子 |
| Z | 原子核外的M层中只有两对成对电子 |
| A.原子半径:Z>X>Y |
| B.第一电离能:X>Y>W |
| C.W的最简单气态氢化物比X的最简单气态氢化物稳定 |
| D.ZY2和WY2在水中的溶解度较大的是ZY2 |
您最近一年使用:0次
2023-05-04更新
|
200次组卷
|
3卷引用:云南省丽江市2022-2023学年高二上学期期末考试化学试题



