1 . A、B、C是短周期ⅠA和ⅡA族元素的碳酸正盐,它们的质量分别为mA、mB、mC,与足量盐酸完全反应,消耗盐酸的物质的量分别为nA(HCl)、nB(HCl)、nC(HCl)。
已知:。mA=mB+mC,nA(HCl)=nB(HCl)+nC(HCl)。请填空:
(1)写出短周期ⅠA和ⅡA族元素形成的所有碳酸盐的名称:___ 。
(2)若以MA、MB和MC分别表示A、B、C的相对分子质量,试写出MA、MB和MC三者的相互关系式___ 。
(3)A的正确选择有___ 种,其化学式为:___ 。
已知:。mA=mB+mC,nA(HCl)=nB(HCl)+nC(HCl)。请填空:
(1)写出短周期ⅠA和ⅡA族元素形成的所有碳酸盐的名称:
(2)若以MA、MB和MC分别表示A、B、C的相对分子质量,试写出MA、MB和MC三者的相互关系式
(3)A的正确选择有
您最近一年使用:0次
名校
解题方法
2 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位置,结构和性质的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
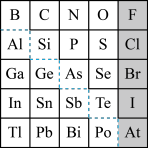
(l)Ge 的最高价氧化物对应水化物的化学式为_____ ,P、S、Cl元素对应的简单离子的还原性由强到弱的顺序为_____ 。(写离子符号)
(2)根据元素周期律,推断:
①阴影部分元素最高价氧化物对应水化物的酸性最强的是_____ 。(写化学式)
②H3AsO4、H2SeO4的酸性强弱:H3AsO4(填“> ”“< ”或“=” )_____ H2SeO4。
③镓的氯化物与氨水反应的化学方程式为_____
(3)用铝和金属氧化物反应制备金属单质是工业上较常用的方法。:如2A1+4BaO 3Ba↑ +BaO •A12O3,利用上述方法可制取Ba的主要原因是
3Ba↑ +BaO •A12O3,利用上述方法可制取Ba的主要原因是____________
a.高温时Al 的活泼性大于Ba b.高温有利于BaO 分解
c.高温时BaO• A12O3比A12O3稳定 d.Ba的沸点比Al 的低
(4)用铝热法还原下列氧化物,制得金属各l mol,消耗铝最少的是________ 。
a.MnO2 b.WO3 c.Cr2O3 d.Co3O4

(l)Ge 的最高价氧化物对应水化物的化学式为
(2)根据元素周期律,推断:
①阴影部分元素最高价氧化物对应水化物的酸性最强的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4(填“> ”“< ”或“=” )
③镓的氯化物与氨水反应的化学方程式为
(3)用铝和金属氧化物反应制备金属单质是工业上较常用的方法。:如2A1+4BaO
 3Ba↑ +BaO •A12O3,利用上述方法可制取Ba的主要原因是
3Ba↑ +BaO •A12O3,利用上述方法可制取Ba的主要原因是a.高温时Al 的活泼性大于Ba b.高温有利于BaO 分解
c.高温时BaO• A12O3比A12O3稳定 d.Ba的沸点比Al 的低
(4)用铝热法还原下列氧化物,制得金属各l mol,消耗铝最少的是
a.MnO2 b.WO3 c.Cr2O3 d.Co3O4
您最近一年使用:0次
18-19高一下·江西南昌·期中
解题方法
3 . 下图是周期表的一部分,回答下列问题:
(1)A的原子结构示意图是_________________ ;
(2)E在周期表的位置为_________________________ ;与E同族的下一周期元素的原子序数为___________ ;
(3)表中元素形成气态氢化物最稳定的是___________ (填化学式,下同),最高价氧化物对应水化物酸性最强的是________________ ;
(4)下列不能用来对比C和D金属性强弱的是_________
a.C单质的熔点比D低
b.C的阳离子的氧化性弱于D的阳离子的氧化性
c.C单质与水反应比D单质与水反应剧烈
d.C最高价氧化物对应水化物的碱性比D强
(5)元素A与H分别与H形成的18电子分子Q和W(常用作火箭燃料)可以发生氧化还原反应,生成H单质和A的另一种氢化物。请写出该反应的方程式:______________________ 。
| H | A | B | ||||||
| C | D | E | F | G | ||||
(2)E在周期表的位置为
(3)表中元素形成气态氢化物最稳定的是
(4)下列不能用来对比C和D金属性强弱的是
a.C单质的熔点比D低
b.C的阳离子的氧化性弱于D的阳离子的氧化性
c.C单质与水反应比D单质与水反应剧烈
d.C最高价氧化物对应水化物的碱性比D强
(5)元素A与H分别与H形成的18电子分子Q和W(常用作火箭燃料)可以发生氧化还原反应,生成H单质和A的另一种氢化物。请写出该反应的方程式:
您最近一年使用:0次
18-19高一下·江西南昌·期中
解题方法
4 . 某同学在研究前18号元素时发现,可以将它们排成如图所示的蜗牛形状,图中每个点代表一种元素,其中O点代表氢元素。下列说法中正确的是


| A.虚线相连的元素处于同一主族 |
| B.形成气态氢化物的稳定性:C>D |
| C.化合物BDA中既含离子键又含共价键且属于离子化合物 |
| D.C的氧化物能与B或D的最高价氧化物的水化物反应 |
您最近一年使用:0次
解题方法
5 . 如图是元素周期表中的前四周期,①~⑨为相应的元素,请从中选择合适的元素回答问题:
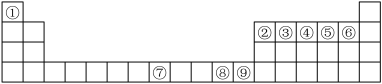
(1)根据元素原子的外围电子排布特征,元素周期表可划分为五个区域,⑨元素位于周期表的________ 区。
(2)④、⑥两元素形成的化合物的立体构型为________ ,其中心原子的杂化轨道类型为________ 。
(3)元素⑧的离子的氢氧化物不溶于水,但可溶于氨水中,该离子与NH3间结合的作用力为________ 。
(4)在周期表给出的9种元素中,电负性最大的元素基态原子的电子排布式为___________ 。
(5)在①与④形成的相对分子质量最小的化合物A中,元素④的杂化类型是____ ,写出与化合物A互为等电子体的一种阳离子______ (填离子符号)。
(6)关于元素①与元素⑤形成的1︰1的化合物,下列说法正确的是______ (填字母序号)。
A.该化合物中的所有原子都满足最外层8电子稳定结构
B.该化合物分子中σ键和π键数目比为1︰1
C.该化合物是由极性键和非极性键形成的极性分子
D.该化合物分子的空间构型为直线形
(7)元素⑦与CO可形成X(CO)5型化合物,该化合物常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断该化合物晶体属于________ 晶体(填晶体类型),化合物中⑦的化合价为:_______ 。根据等电子体理论,该化合物的配体的结构式为:_______ ,CaC2中,阴离子的电子式为: ____________________ 。

(1)根据元素原子的外围电子排布特征,元素周期表可划分为五个区域,⑨元素位于周期表的
(2)④、⑥两元素形成的化合物的立体构型为
(3)元素⑧的离子的氢氧化物不溶于水,但可溶于氨水中,该离子与NH3间结合的作用力为
(4)在周期表给出的9种元素中,电负性最大的元素基态原子的电子排布式为
(5)在①与④形成的相对分子质量最小的化合物A中,元素④的杂化类型是
(6)关于元素①与元素⑤形成的1︰1的化合物,下列说法正确的是
A.该化合物中的所有原子都满足最外层8电子稳定结构
B.该化合物分子中σ键和π键数目比为1︰1
C.该化合物是由极性键和非极性键形成的极性分子
D.该化合物分子的空间构型为直线形
(7)元素⑦与CO可形成X(CO)5型化合物,该化合物常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
您最近一年使用:0次
名校
解题方法
6 . 有X、Y、Z、W四种短周期主族元素,它们在周期表中的位置如图所示,已知Y是地壳中含量最高的金属元素,则下列说法中正确的是( )
| X | |||
| Y | Z | W |
| A.简单离子半径:Y>W |
| B.Y的最高价氧化物的水化物和X的最高价氧化物的水化物可反应 |
| C.X的简单氢化物比Z的简单氢化物更稳定、沸点更高 |
| D.非金属性:W>X |
您最近一年使用:0次
2019-12-31更新
|
559次组卷
|
3卷引用:华南师范大学附中2020届高三上学期第三次月考理综化学试题
解题方法
7 . W、X、Y、Z为原子序数依次递增的短周期主族元素,W的单质是同条件下密度最小的气体,X、Y、Z为同一周期紧邻元素,M、R为同一主族的元素,M的单质常温为液态,R的单质常温为固态,且易升华。回答下列问题:
(1)写出下列元素的名称:W___ ;M____ 。
(2)若X为形成化合物种类最多的元素,XZ(YW2)2为一种有机物,是目前使用量较大的化学肥料。XZ(YW2)2在碱性条件下能被MZ−氧化成单质Q(空气中的主要成分之一),X以酸根的形式存在。
①写出Q的化学式:___ ;X、Y、Z的简单氢化物的沸点由高到低的顺序为__ (写化学式)。
②上述反应的离子方程式为___ 。
(3)若Z为本周期中半径最小的元素,其最高价氧化物对应的水化物为强酸。
①请判断R2+ZO3-→RO3-+Z2是否能发生,__ (填“能”或“不能”)发生,其原因是____ 。
②请写出R2与含YO32-溶液反应的离子方程式为____ 。
(1)写出下列元素的名称:W
(2)若X为形成化合物种类最多的元素,XZ(YW2)2为一种有机物,是目前使用量较大的化学肥料。XZ(YW2)2在碱性条件下能被MZ−氧化成单质Q(空气中的主要成分之一),X以酸根的形式存在。
①写出Q的化学式:
②上述反应的离子方程式为
(3)若Z为本周期中半径最小的元素,其最高价氧化物对应的水化物为强酸。
①请判断R2+ZO3-→RO3-+Z2是否能发生,
②请写出R2与含YO32-溶液反应的离子方程式为
您最近一年使用:0次
2019-09-26更新
|
387次组卷
|
2卷引用:学科网2019年高三11月大联考(样卷)化学试题
13-14高一·全国·课时练习
名校
解题方法
8 . 下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
(1)④、⑤、⑥的原子半径由大到小的顺序是________ 。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是________ 。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:________ 。
(4)由表中两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)________ 。
A.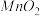 B.
B.
C. D.
D.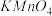
| 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
(4)由表中两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)
A.
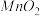 B.
B.
C.
 D.
D.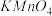
您最近一年使用:0次
2019-08-20更新
|
165次组卷
|
7卷引用:2014年高一化学人教版必修2 模块水平检测1练习卷
(已下线)2014年高一化学人教版必修2 模块水平检测1练习卷(已下线)2013-2014山东省淄博市高一下学期期末考试化学试卷2015-2016学年河北省秦皇岛市卢龙县高一下学期期中考试化学试卷2015-2016学年山西省长治一中高一平行班下期中化学试卷云南省峨山彝族自治县第一中学2017-2018学年高二上学期期末市统测模拟考化学试题百所名校联考-必修二模块综合检测山东省泰安市新泰市第二中学2019-2020学年高一下学期期中考试化学试题
名校
9 . X、Y、Z、W均为短周期主族元素,它们在周期表中的相对位置如图所示,下列说法中正确的是( )
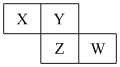

A.Y的价层电子排布式是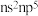 |
| B.四种元素所形成的最简单氢化物中,沸点最高的是可能Y的氢化物 |
| C.Y、Z之间可形成离子型化合物 |
| D.X、Z、W的最高价氧化物所对应的水化物不可能均是强酸 |
您最近一年使用:0次
2019-08-13更新
|
1538次组卷
|
5卷引用:新疆石河子第二中学2018-2019学年高二下学期第一次月考化学试题
10 . 下列说法正确的是
| A.氢原子的电子云图中小黑点的疏密表示电子在核外单位体积内出现机会的多少 |
| B.最外层电子数为ns2的元素都在元素周期表第2列 |
C.处于最低能量的原子叫做基态原子,1s22s22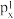 →1s22s22 →1s22s22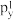 过程中形成的是发射光谱 过程中形成的是发射光谱 |
| D.已知某元素+3价离子的电子排布式为1s22s22p63s23p63d5,该元素位于周期表中的第四周期第VIII族位置,属于ds区 |
您最近一年使用:0次
2019-07-15更新
|
2342次组卷
|
7卷引用:宁夏银川一中2018-2019学年高二下学期期末考试化学试题



