1 . 元素周期表是学习和研究化学的重要工具。下列是元素周期表的部分信息:
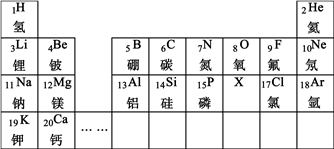
(1)地壳中含量最多的金属元素的原子序数是____________ 。
(2)分析上表规律,可推知,表中X的元素符号为____________ 。
(3)Ca在元素周期表中的位置为____________ 。
(4)写出一种由原子序数1、7、17三种元素组成化合物的化学式:__________ 。

(1)地壳中含量最多的金属元素的原子序数是
(2)分析上表规律,可推知,表中X的元素符号为
(3)Ca在元素周期表中的位置为
(4)写出一种由原子序数1、7、17三种元素组成化合物的化学式:
您最近一年使用:0次
2 . 下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
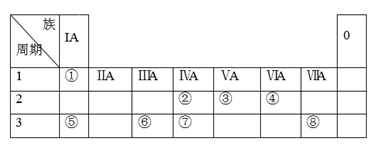
(1)①的元素符号为______ ;②的元素符号为______ ;③的元素符号为______ ;④的元素符号为______ ;⑤的元素符号为______ ;⑥的元素符号为______ ;⑦的元素符号为______ ;⑧的元素符号为_______ 。
(2)⑧的气态氢化物为_____________ (填化学式)。
(3)⑤对应的碱的化学式为__________ ;③的最高价含氧酸为___________ (填化学式)。
(4)⑤、⑥元素的金属性强弱依次为___________ (填“增大”、“减小”或“不变”)。

(1)①的元素符号为
(2)⑧的气态氢化物为
(3)⑤对应的碱的化学式为
(4)⑤、⑥元素的金属性强弱依次为
您最近一年使用:0次
名校
解题方法
3 . 近年来连续出现的铊中毒事件,给各科研单位及学校危险药品的管理敲响了警钟。铊的相关信息卡片如图所示:

(1)铊的原子序数为81,铊在元素周期表中位于第________ 周期第________ 族。
(2)若设铊的质量数为A,则铊原子中中子数和质子数之差为____________ 。
(3)下列推断正确的是________ 。
A.单质的还原性:Tl>Al B.原子半径:Al>Tl
C.碱性:Al(OH)3>Tl(OH)3 D.氧化性:Tl3+>Al3+
(4)铊(Tl)是某超导材料的组成元素之一。Tl3+与Ag在酸性介质中发生反应:
Tl3++2Ag===Tl++2Ag+。下列推断正确的是________ 。
A.Tl+最外层有1个电子 B.Tl能形成+3价和+1价的化合物
C.Tl3+的氧化性比Ag+弱 D.Tl+的还原性比Ag强

(1)铊的原子序数为81,铊在元素周期表中位于第
(2)若设铊的质量数为A,则铊原子中中子数和质子数之差为
(3)下列推断正确的是
A.单质的还原性:Tl>Al B.原子半径:Al>Tl
C.碱性:Al(OH)3>Tl(OH)3 D.氧化性:Tl3+>Al3+
(4)铊(Tl)是某超导材料的组成元素之一。Tl3+与Ag在酸性介质中发生反应:
Tl3++2Ag===Tl++2Ag+。下列推断正确的是
A.Tl+最外层有1个电子 B.Tl能形成+3价和+1价的化合物
C.Tl3+的氧化性比Ag+弱 D.Tl+的还原性比Ag强
您最近一年使用:0次
4 . 下面是元素周期表的一部分,参照元素①~⑧在表中的位置,请用化学用语回答下列问题:
(1)④、⑤、⑦的原子半径由大到小的顺序为(元素符号)___________ 。
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是(填化学式)___________ 。
(3)在①、④、⑤、⑧中的某些元素之间可形成既含离子键又含非极性共价键的离子化合物,写出其中一种化合物的电子式:__________ 。
(4)由②和④组成的化合物与⑤的同周期相邻主族元素的单质反应的化学方程式为:_____________ 。
(5)⑦单质与⑤的最高价氧化物的水化物反应的离子方程式为____________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)④、⑤、⑦的原子半径由大到小的顺序为(元素符号)
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是(填化学式)
(3)在①、④、⑤、⑧中的某些元素之间可形成既含离子键又含非极性共价键的离子化合物,写出其中一种化合物的电子式:
(4)由②和④组成的化合物与⑤的同周期相邻主族元素的单质反应的化学方程式为:
(5)⑦单质与⑤的最高价氧化物的水化物反应的离子方程式为
您最近一年使用:0次
名校
5 . 铁及其化合物之间的相互转化可用下式表示:
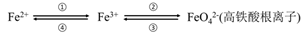
回答下列有关问题:
(1)铁元素在周期表中的位置是_____________ .
(2)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净,可选用的试剂是__________ --(选填序号).
A.Cl2 B.Fe C.HNO3 D.H2O2
(3)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺.精矿在阳极浸出的反应比较复杂,其中有一主要反应CuFeS2+4Fe3+=Cu2++5Fe2++2S(CuFeS2中S为-2价),下列说法正确的是_____ (选填序号).
A.从物质分类的角度看,黄铜矿属于合金
B.反应中,所有铁元素均被还原
C.反应中,CuFeS2 既作氧化剂又作还原剂
D.当转移1mol电子时,46g CuFeS2参加反应
(4)下述反应中,若FeSO4和O2的系数比为2:1,试配平下列方程式:_______FeSO4+_______K2O2→_______K2FeO4+_______K2O+ _______K2SO4+_______O2↑
_____________
(5)某同学将铁与水蒸气高温反应后的固体物质溶解在过量盐酸中,如何判断所得溶液中是否含有Fe3+?_____________________________________
(6)向含4 mol HNO3的稀溶液中逐渐加入铁粉至过量,假设生成的气体只有一种,请在坐标系中画出n(Fe2+)随n(Fe)变化的示意图,并在途中标出各点的坐标值。______________


回答下列有关问题:
(1)铁元素在周期表中的位置是
(2)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净,可选用的试剂是
A.Cl2 B.Fe C.HNO3 D.H2O2
(3)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺.精矿在阳极浸出的反应比较复杂,其中有一主要反应CuFeS2+4Fe3+=Cu2++5Fe2++2S(CuFeS2中S为-2价),下列说法正确的是
A.从物质分类的角度看,黄铜矿属于合金
B.反应中,所有铁元素均被还原
C.反应中,CuFeS2 既作氧化剂又作还原剂
D.当转移1mol电子时,46g CuFeS2参加反应
(4)下述反应中,若FeSO4和O2的系数比为2:1,试配平下列方程式:_______FeSO4+_______K2O2→_______K2FeO4+_______K2O+ _______K2SO4+_______O2↑
(5)某同学将铁与水蒸气高温反应后的固体物质溶解在过量盐酸中,如何判断所得溶液中是否含有Fe3+?
(6)向含4 mol HNO3的稀溶液中逐渐加入铁粉至过量,假设生成的气体只有一种,请在坐标系中画出n(Fe2+)随n(Fe)变化的示意图,并在途中标出各点的坐标值。

您最近一年使用:0次
2017-11-02更新
|
287次组卷
|
3卷引用:二轮复习测试专项 专题05 氧化还原反应
名校
6 . 短周期元素 a~g 在表中的位置如右表,请回答下列问题:
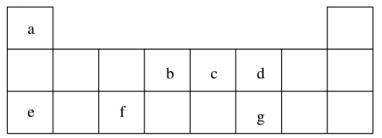
(1)d、e元素常见离子的半径由大到小的顺序为(用化学式表示)__________ ;b、c两元素非金属性较强的是(写元素符号)_________ ,写出能证明这一结论的一个化学方程式_____________ 。
(2)下列有关说法正确的是( )
A.e在 d2 中燃烧,生成e2d
B.加热熔化eda时不可用Al2O3坩埚,可用瓷坩埚
C.将 gd2 通入溴水中,溴水褪色,体现了gd2 的漂白性
D.将打磨过的 f 置于酒精灯上点燃,观察到f 熔化但未见液滴滴落
(3)上述元素可组成盐 R:ca4f(gd4)2和盐S:ca4agd4。
①相同条件下,0.1 mol·L-1盐R中 c(ca4+)_______ (填“=”、 “>”或“<”)0.1 mol·L-1盐S中c(ca4+)。
②R常用作净水剂,其原理为(用离子方程式表示)______________ 。
③向盛有 10 mL 1 mol·L-1盐S溶液的烧杯中滴加1 mol·L-1 NaOH溶液至中性,则反应后各离子浓度由大到小的排列顺序是_____________ 。
④向盛有 10 mL 1 mol·L-1盐R溶液的烧杯中滴加 1 mol·L-1NaOH溶液 32 mL后,继续滴加至35 mL,写出此时段(32 mL~35 mL)间发生的离子方程式:_____________ 。

(1)d、e元素常见离子的半径由大到小的顺序为(用化学式表示)
(2)下列有关说法正确的是
A.e在 d2 中燃烧,生成e2d
B.加热熔化eda时不可用Al2O3坩埚,可用瓷坩埚
C.将 gd2 通入溴水中,溴水褪色,体现了gd2 的漂白性
D.将打磨过的 f 置于酒精灯上点燃,观察到f 熔化但未见液滴滴落
(3)上述元素可组成盐 R:ca4f(gd4)2和盐S:ca4agd4。
①相同条件下,0.1 mol·L-1盐R中 c(ca4+)
②R常用作净水剂,其原理为(用离子方程式表示)
③向盛有 10 mL 1 mol·L-1盐S溶液的烧杯中滴加1 mol·L-1 NaOH溶液至中性,则反应后各离子浓度由大到小的排列顺序是
④向盛有 10 mL 1 mol·L-1盐R溶液的烧杯中滴加 1 mol·L-1NaOH溶液 32 mL后,继续滴加至35 mL,写出此时段(32 mL~35 mL)间发生的离子方程式:
您最近一年使用:0次
2017-10-21更新
|
707次组卷
|
3卷引用:2019年秋高三化学复习强化练习—— 硫及其化合物
7 . 下表标出的是元素周期表的一部分元素,用元素符号回答下列问题:
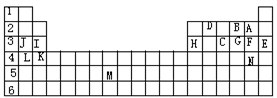
(1)表中用字母标出的14种元素中,化学性质最不活泼的是________ ,主族元素中金属性最强的是_______ ,非金属性最强是_____ ,常温下单质为液态的非金属元素是______ ;M所在的族是_________ 。
(2)C气态氢化物的化学式分别为_____________ ,A、B、C的气态氢化物中最稳定的是_______ 。
(3)第三周期中原子半径最小的是____________ 。

(1)表中用字母标出的14种元素中,化学性质最不活泼的是
(2)C气态氢化物的化学式分别为
(3)第三周期中原子半径最小的是
您最近一年使用:0次
名校
8 . 硼及硼的化合物有着广泛的用途。请回答下列问题:
(1)硼在元素周期表中的位置为____________ ,硼元素有两种天然同位素10B和11B,硼元素的近似相对原子质量为10.8,则两种同位素原子的原子个数之比为_____________ 。
(2)单质硼(B)在一定条件下与NaOH溶液反应生成NaBO2和一种气体,请写出该反应的化学方程式__________________________ 。
(3)硼酸(H3BO3)是一种白色片状晶体,微溶于水,对人体的受伤组织有着和缓的防腐消毒作用。硼酸是一元弱酸,室温时0.1mol/L硼酸的pH为5,计算硼酸的电离常数数K=____________ 。
氟硼酸(HBF4)是一种强酸,仅以离子状态存在于水中,请写出BF4-的电子式____________ 。
(4)B2H6是硼的一种气态氢化物,因组成与乙烷(C2H6)相似而被称为乙硼烷。
①经测定B2H6中B原子最外层也满足8电子结构,由此推测B2H6与C2H6分子结构____________ (填“相同”或“不相同”)。
②B2H6可由BF3与NaBH4在一定条件下反应制得,写出该反应的化学方程式_____________ 。
③B2H6是强还原剂,它与水反应生成H3BO3和H2。若有0.1mol B2H6与水完全反应,则产生H2在标准状况下的体积为____________ L。
(1)硼在元素周期表中的位置为
(2)单质硼(B)在一定条件下与NaOH溶液反应生成NaBO2和一种气体,请写出该反应的化学方程式
(3)硼酸(H3BO3)是一种白色片状晶体,微溶于水,对人体的受伤组织有着和缓的防腐消毒作用。硼酸是一元弱酸,室温时0.1mol/L硼酸的pH为5,计算硼酸的电离常数数K=
氟硼酸(HBF4)是一种强酸,仅以离子状态存在于水中,请写出BF4-的电子式
(4)B2H6是硼的一种气态氢化物,因组成与乙烷(C2H6)相似而被称为乙硼烷。
①经测定B2H6中B原子最外层也满足8电子结构,由此推测B2H6与C2H6分子结构
②B2H6可由BF3与NaBH4在一定条件下反应制得,写出该反应的化学方程式
③B2H6是强还原剂,它与水反应生成H3BO3和H2。若有0.1mol B2H6与水完全反应,则产生H2在标准状况下的体积为
您最近一年使用:0次
2017-05-07更新
|
803次组卷
|
3卷引用:2020届高三化学二轮选修大题必练—— 物质结构与性质大题练
真题
名校
9 . Q、R、T、W四种短周期元素在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
(1)T的原子结构示意图为_______ 。
(2)元素的非金属性为(原子的得电子能力):Q_______ W(填“强于”或“弱于”)。
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为_______ 。
(4)原子序数比R多1的元素的一种氢化物A能分解为其另一种氢化物B,写出A的电子式_____ 。
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是___ 。
(6)在298K下,Q、T的单质各1mol完全燃烧,分别放出热量aKJ和bKJ。又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3molQ的单质,则该反应在298K下的△H =_______ kJ/mol(注:题中所设单质均为最稳定单质)
Q | R | ||
T | W |
(1)T的原子结构示意图为
(2)元素的非金属性为(原子的得电子能力):Q
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为
(4)原子序数比R多1的元素的一种氢化物A能分解为其另一种氢化物B,写出A的电子式
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是
(6)在298K下,Q、T的单质各1mol完全燃烧,分别放出热量aKJ和bKJ。又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3molQ的单质,则该反应在298K下的△H =
您最近一年使用:0次
2016-12-08更新
|
1277次组卷
|
5卷引用:山西省实验中学2020届高三化学复习针对性试题集(三)



