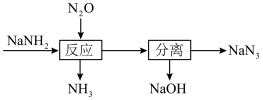
1 . 叠氮化钠(NaN3)可用于汽车安全气囊的产气药。一种由氨基化钠(NaNH2)制备NaN3的工艺流程如下:
(1)生产NaNH2的化学方程式为2Na+ 2NH3(液)= 2NaNH2+ H2↑。
①钠元素位于周期表第___________ 周期___________ 族。
②NaNH2中氮元素的化合价为___________ .
(2) NaOH的电子式为___________ , 流程中“反应”的化学方程式为___________ 。
(3) NaN3晶体属于_____________ (填 “离子”、“分子”或“原子”)晶体,NaN3在撞击时能发生分解反应生成两种单质。计算理论上65gNaN3完全分解,释放出标准状况下的气体体积_________ (写出计算过程)。

(1)生产NaNH2的化学方程式为2Na+ 2NH3(液)= 2NaNH2+ H2↑。
①钠元素位于周期表第
②NaNH2中氮元素的化合价为
(2) NaOH的电子式为
(3) NaN3晶体属于
您最近一年使用:0次
2 . 硫是人类认识最早的元素之一,含硫物质在现代生产和生活中发挥着重要作用。
(l)我国化学家姜雪峰因其在绿色有机硫化学领域的杰出贡献被遴选为“全球青年化学家元素周期表硫元素代表”。
①硫元素在元素周期表中的位置是____ 。
②乙硫醇(CH3CH2SH)是一种含硫有机物,其分子中S-H的极性小于CH3CH2OH分子中O-H的极性,请从原子结构角度解释其原因:____ 。
(2)自然界的硫循环过程如下图所示。
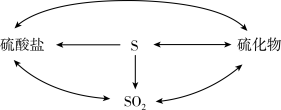
①上图所涉及的含硫物质中,能使品红溶液褪色的是____ 。
②降解石油(主要成分为CxHy)的过程中,在细菌催化作用下,石油与硫酸盐反应转化为碳酸氢盐,硫酸盐做____ (填“氧化剂”或“还原剂”)。
③煤炭中的硫化物主要为FeS2(S为-1价)。在潮湿的环境中,FeS2可在氧化亚铁硫杆菌(T.f)的作用下被空气氧化为Fe2(SO4)3,该反应的化学方程式为____ 。
(l)我国化学家姜雪峰因其在绿色有机硫化学领域的杰出贡献被遴选为“全球青年化学家元素周期表硫元素代表”。
①硫元素在元素周期表中的位置是
②乙硫醇(CH3CH2SH)是一种含硫有机物,其分子中S-H的极性小于CH3CH2OH分子中O-H的极性,请从原子结构角度解释其原因:
(2)自然界的硫循环过程如下图所示。

①上图所涉及的含硫物质中,能使品红溶液褪色的是
②降解石油(主要成分为CxHy)的过程中,在细菌催化作用下,石油与硫酸盐反应转化为碳酸氢盐,硫酸盐做
③煤炭中的硫化物主要为FeS2(S为-1价)。在潮湿的环境中,FeS2可在氧化亚铁硫杆菌(T.f)的作用下被空气氧化为Fe2(SO4)3,该反应的化学方程式为
您最近一年使用:0次
名校
3 . 已知元素aA、bB、cC、dD、eE的原子结构示意图分别为
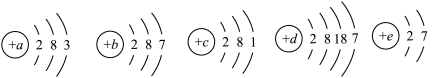
请回答下列问题:
(1)属于同周期的元素是________ (填元素符号,下同),属于同主族的元素是________ 。
(2)金属性最强的元素是________ ,非金属性最强的元素是________ 。
(3)上述元素中最高价氧化物对应的水化物碱性最强的是________ (填化学式)。

请回答下列问题:
(1)属于同周期的元素是
(2)金属性最强的元素是
(3)上述元素中最高价氧化物对应的水化物碱性最强的是
您最近一年使用:0次
2020-02-04更新
|
203次组卷
|
5卷引用:第03天 原子核外电子排布——《每日一题·2018快乐暑假》高二化学
(已下线)第03天 原子核外电子排布——《每日一题·2018快乐暑假》高二化学湖北省宜昌市示范高中协作体2016-2017学年高一下学期期中联考化学试题山西省大同市第三中学2017-2018学年高一下学期4月月考化学试题2019—2020学年人教版必修2第一章 第一节《元素周期表》第2课时《元素的性质与原子结构》(跟踪训练)(已下线)4.1.2 原子结构与元素的性质练习(2)——《高中新教材同步备课》(人教版 必修第一册)
名校
解题方法
4 . 氟及其化合物在生产生活中被广泛使用,造福人类。
(1)氟在元素周期表中的位置是___________ 。
(2)氢氟酸具有刻蚀玻璃的特性,写出该反应的化学方程式____________ 。已知25℃时,氢氟酸的电离平衡常数Ka=3.6×10-4,若将0.01 mol·L-1的HF溶液与pH=12的NaOH溶液等体积混合,则溶液中离子浓度由大到小的顺序为_____ 。
(3)次氟酸(HOF)由科学家在1971年首次制得,次氟酸的电子式为_______ 。
(4)四氟肼(N2F4)用作高能燃料的氧化剂,1 mol N2F4分子中含有的共价键数目是________ NA。N2F4气体可用Fe3+氧化二氟胺(HNF2)制得,写出该反应的离子方程式______________ 。
(5)六氟化铀(UF6)是铀的稳定气态化合物,用作核燃料,由U3O8制取UF6的三步反应原理如下:
①U3O8+H2 →UO2+H2O (未配平) ②UO2+4HF=UF4+2H2O ③UF4+ F2 = UF6
则下列说法正确的是_____________ 。
A.反应①②③都是氧化还原反应
B.反应③中U元素被氧化
C.反应①中氧化剂和还原剂的物质的量之比为2:1
(6)六氟磷酸锂(LiPF6)是锂离子电池广泛使用的电解质。LiPF6与极少量水反应可生成POF3等三种含氟化合物,写出该反应的化学方程式:________ 。
(1)氟在元素周期表中的位置是
(2)氢氟酸具有刻蚀玻璃的特性,写出该反应的化学方程式
(3)次氟酸(HOF)由科学家在1971年首次制得,次氟酸的电子式为
(4)四氟肼(N2F4)用作高能燃料的氧化剂,1 mol N2F4分子中含有的共价键数目是
(5)六氟化铀(UF6)是铀的稳定气态化合物,用作核燃料,由U3O8制取UF6的三步反应原理如下:
①U3O8+H2 →UO2+H2O (未配平) ②UO2+4HF=UF4+2H2O ③UF4+ F2 = UF6
则下列说法正确的是
A.反应①②③都是氧化还原反应
B.反应③中U元素被氧化
C.反应①中氧化剂和还原剂的物质的量之比为2:1
(6)六氟磷酸锂(LiPF6)是锂离子电池广泛使用的电解质。LiPF6与极少量水反应可生成POF3等三种含氟化合物,写出该反应的化学方程式:
您最近一年使用:0次
2020-01-23更新
|
243次组卷
|
4卷引用:2020届高三《新题速递·化学》2月第01期(考点01-06)
(已下线)2020届高三《新题速递·化学》2月第01期(考点01-06)(已下线)考点05 元素周期表和元素周期律-2020年高考化学命题预测与模拟试题分类精编福建省宁德市2019-2020学年高三上学期期末质量检测理综化学试题河南省郑州市第一中学2021届高三上学期开学测试化学试题
名校
5 . 砷(As)是第四周期ⅤA族元素,可以形成As2S3、H3AsO3、H3AsO4等化合物,用途广泛。完成下列填空:
(1)砷原子核外有____ 个电子层,最外层有_____ 个电子。
(2)将砷与ⅤA族所有短周期元素的原子半径,按从小到大的顺序排列_____ (用元素符号表示)
(3)溴位于ⅦA族且与砷同周期,比较溴、砷最高价氧化物对应水化物酸性的强弱:_____ 强于____ (填物质的化学式)
(4)周期表中,铝和砷都在金属和非金属过渡线附近。若向AlCl3溶液中逐滴加入NaOH溶液,先生成沉淀,然后沉淀逐渐消失,请用电离平衡移动的原理解释沉淀会消失的原因______ 。
(1)砷原子核外有
(2)将砷与ⅤA族所有短周期元素的原子半径,按从小到大的顺序排列
(3)溴位于ⅦA族且与砷同周期,比较溴、砷最高价氧化物对应水化物酸性的强弱:
(4)周期表中,铝和砷都在金属和非金属过渡线附近。若向AlCl3溶液中逐滴加入NaOH溶液,先生成沉淀,然后沉淀逐渐消失,请用电离平衡移动的原理解释沉淀会消失的原因
您最近一年使用:0次
6 . 砷(As)是第四周期VA族元素,可以形成As2S3、H3AsO3、H3AsO4等化合物,用途广泛。
完成下列填空:
(1)砷原子核外有__ 个电子层,最外层有__ 个电子,写出砷原子最外层电子的轨道表示式:__ 。
(2)将砷与VA族所有短周期元素的原子半径,按从小到大的顺序排列:__ (用元素符号表示)。
(3)溴位于VIIA族且与砷同周期,比较溴、砷最高价氧化物对应水化物酸性的强弱:__ 强于__ (填物质的化学式)。
(4)周期表中,铝和砷都在金属和非金属过渡线附近,举一例说明铝元素具有非金属性:__ 。
(5)已知:稀Na3AsO3溶液、稀碘水和稀NaOH溶液混合,发生如下反应:AsO33-(aq)+I2(aq)+2OH- AsO43-(aq)+2I-(aq)+H2O(l),溶液中c(AsO43-)与反应时间(t)的关系如图所示。
AsO43-(aq)+2I-(aq)+H2O(l),溶液中c(AsO43-)与反应时间(t)的关系如图所示。
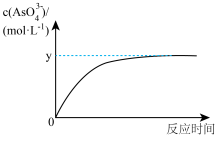
①写出该反应平衡常数的表达式K=___ 。
②不能判断反应达到平衡状态的是___ (选填编号)。
A.溶液的pH不再变化
B.v(I-)=2v(AsO33-)
C.c(AsO33-)/c(I-)不再变化
D.c(I-)=2ymol·L-1
完成下列填空:
(1)砷原子核外有
(2)将砷与VA族所有短周期元素的原子半径,按从小到大的顺序排列:
(3)溴位于VIIA族且与砷同周期,比较溴、砷最高价氧化物对应水化物酸性的强弱:
(4)周期表中,铝和砷都在金属和非金属过渡线附近,举一例说明铝元素具有非金属性:
(5)已知:稀Na3AsO3溶液、稀碘水和稀NaOH溶液混合,发生如下反应:AsO33-(aq)+I2(aq)+2OH-
 AsO43-(aq)+2I-(aq)+H2O(l),溶液中c(AsO43-)与反应时间(t)的关系如图所示。
AsO43-(aq)+2I-(aq)+H2O(l),溶液中c(AsO43-)与反应时间(t)的关系如图所示。
①写出该反应平衡常数的表达式K=
②不能判断反应达到平衡状态的是
A.溶液的pH不再变化
B.v(I-)=2v(AsO33-)
C.c(AsO33-)/c(I-)不再变化
D.c(I-)=2ymol·L-1
您最近一年使用:0次
2019-11-08更新
|
164次组卷
|
3卷引用:专题35 磷、砷及其化合物-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
(已下线)专题35 磷、砷及其化合物-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)上海市杨浦区2017-2018学年度高三第一学期高中等级考模拟调研化学试题上海市民星中学2019—2020学年高三上学期期中考试化学试题
7 . 按要求完成下列填空
(1)某原子的激发态原子的电子排布式为1s22s22p63s23p34s1,则该原子基态原子的电子排布式为______________________ ;元素符号为_________ ;其最高价氧化物对应的水化物的化学式是__________ 。
(2)某原子的电子排布式为 [Ne]3s23p1,则该原子的元素符号为______ ,最高正价为______ ,该原子位于元素周期表第_____ 周期第_____ 族,位于元素周期表______ 区。
(3)某原子位于元素周期表第3周期第IA族,则该原子序数为________ ,位于元素周期表______ 区,电子排布式为________________________ 。
(1)某原子的激发态原子的电子排布式为1s22s22p63s23p34s1,则该原子基态原子的电子排布式为
(2)某原子的电子排布式为 [Ne]3s23p1,则该原子的元素符号为
(3)某原子位于元素周期表第3周期第IA族,则该原子序数为
您最近一年使用:0次
2019-08-13更新
|
677次组卷
|
4卷引用:第1.2.1讲 原子结构与元素周期表-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)
(已下线)第1.2.1讲 原子结构与元素周期表-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)新疆疏勒八一中2018-2019学年高二4月月考化学试题(人教版2019)选择性必修2 第一章 原子结构与性质 第二节 原子结构与元素的性质 课时1 原子结构与元素周期表鲁科版2019选择性必修2第1章 原子结构与元素性质 第2节 原子结构与元素周期表 第2课时 核外电子排布与元素周期表
名校
8 . 几种主族元素在周期表中的位置如下

根据上表回答下列问题:
(1)⑥元素的氢化物是_________ (填化学式)
(2)①③⑦三种元素原子半径由大到小的顺序是_________ (填元素符号)。
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为_________ ,该元素在周期表中的位置是__________________ 。
(4)①②③三种元素氧化物对应水化物碱性最强的是_________ (填化学式),①与水反应的化学方程式为_________ 。
(5)⑦非金属性强于⑧,从原子结构的角度解释其原因:_________ 。下列表述中能证明这一事实的是_________ (填序号)
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物的水化物的酸性强于⑧最高价氧化物的水化物的酸性
c.⑦能将⑧从其钠盐溶液中置换出来
(6)④与⑤元素形成的分子可能是_________ (填字母序号)


根据上表回答下列问题:
(1)⑥元素的氢化物是
(2)①③⑦三种元素原子半径由大到小的顺序是
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为
(4)①②③三种元素氧化物对应水化物碱性最强的是
(5)⑦非金属性强于⑧,从原子结构的角度解释其原因:
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物的水化物的酸性强于⑧最高价氧化物的水化物的酸性
c.⑦能将⑧从其钠盐溶液中置换出来
(6)④与⑤元素形成的分子可能是

您最近一年使用:0次
9 . 下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,在这些元素中,化学性质最不活泼的是_____________ (填具体元素符号,下同)。
(2)在最高价氧化物的水化物中,酸性最强的化合物是_________ ,碱性最强的化合物是_________ 。
(3)最高价氧化物是两性氧化物的元素是_________ 。
(4)元素④与⑥形成的化合物属于_____________ (填“共价”或“离子”)化合物。
(5)①与⑦形成的化合物的化学式__________________ 。
(6)写出⑥的原子结构示意图_____________ 。
| 主族 周期 | I A | IIA | IIIA | IVA | V A | VIA | VIIA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(1)在这些元素中,在这些元素中,化学性质最不活泼的是
(2)在最高价氧化物的水化物中,酸性最强的化合物是
(3)最高价氧化物是两性氧化物的元素是
(4)元素④与⑥形成的化合物属于
(5)①与⑦形成的化合物的化学式
(6)写出⑥的原子结构示意图
您最近一年使用:0次
2019-05-29更新
|
125次组卷
|
3卷引用:2019年6月8日 《每日一题》 必修2 周末培优
(已下线)2019年6月8日 《每日一题》 必修2 周末培优【市级联考】山东省威海市2018-2019学年高一下学期期中考试化学试题甘肃省庆阳市第六中学2021-2022学年高二上学期第一次月考化学(文)试题
10 . 下表为元素周期表的一部分,表中序号分别代表某一元素。请回答下列问题。
(1)①~⑩中,最活泼的金属元素是________ (写元素符号,下同),最不活泼的元素是________ 。
(2)①⑧的简单离子,其半径更大的是________ (写离子符号)。
(3)⑧⑨的气态氢化物,更稳定的是____________ (填化学式)。
(4)元素的非金属性:⑥________ ⑦(填“>”或“<”)。
(5)①~⑨的最高价氧化物的水化物中:酸性最强的是____________ (填化学式);碱性最强的是__________ (填化学式),该碱与⑤的最高价氧化物的水化物反应的离子方程式为__________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑦ | ⑧ | ⑩ | |||||
| 3 | ① | ② | ⑤ | ⑥ | ⑨ | |||
| 4 | ② | ④ |
(2)①⑧的简单离子,其半径更大的是
(3)⑧⑨的气态氢化物,更稳定的是
(4)元素的非金属性:⑥
(5)①~⑨的最高价氧化物的水化物中:酸性最强的是
您最近一年使用:0次
2019-04-24更新
|
120次组卷
|
4卷引用:5.1.4 元素周期表的应用(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)
(已下线)5.1.4 元素周期表的应用(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)福建省德化县第一中学、永安市第一中学、漳平市第一中学2017--2018学年高一年第一次联考(4月)化学试题甘肃省武威市第五中学2018-2019学年高一下学期第一次月考化学试题湖南省邵阳市新邵县2021-2022学年高一上学期期末质量检测化学试题



