名校
1 . 已知某些元素在周期表中的位置如图所示,下列说法不正确的是

| A.元素②和⑤位于同一区 |
| B.s区(除元素①外)、d区和ds区的元素都是金属元素 |
| C.与元素④具有相同最外层电子数的元素只可能处于ds区 |
D.元素③的基态原子中,价层电子的轨道表示式为: |
您最近一年使用:0次
2023-06-07更新
|
94次组卷
|
2卷引用:广东省茂名市信宜市2022-2023学年高二下学期4月期中考试化学试题
解题方法
2 . 化学用语是化学科目中的基础性语言,下列化学用语的使用正确的是
A.丙炔的结构简式: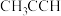 | B.葡萄糖的某种环状结构: |
| C.Cr位于元素周期表的ds区 | D. 分子的球棍模型: 分子的球棍模型: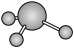 |
您最近一年使用:0次
2023-06-02更新
|
83次组卷
|
4卷引用:河南省驻马店市2022-2023学年高二下学期5月月考化学试题
名校
3 . 元素周期表和周期律体现了对元素的科学分类方法,以及结构决定性质的化学观念,下列说法正确的是
| A.门捷列夫编制的第一张元素周期表是按原子序数递增的顺序编排的 |
| B.在金属与非金属分界线附近可以寻找优良催化剂和耐高温的合金材料 |
| C.某元素的原子最外层只有一个电子,它跟卤素原子结合时,所形成的化学键一定是离子键 |
| D.化学键是相邻离子或原子间的一种强作用力,既包括静电吸引力,又包括静电排斥力 |
您最近一年使用:0次
4 . 人类赖以生存的大千世界是由众多物质组成的,而数量如此庞大的物质却仅由百余种化学元素组成。我们要探索元素性质的递变规律,理解原子是如何通过相互作用构建物质。
(1)下列说法不正确的是__________
(2)下列说法正确的是___________
(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)4,Ni(CO)4呈正四面体形,Ni(CO)4易溶于下列物质中的__________
(4)氯原子最外层电子的原子轨道有___________ 种不同的伸展方向。
(5)写出与氯同周期,有3个未成对电子的基态原子的价电子轨道表示式为:___________ 。
(6)元素周期表中与氧元素相邻,且第一电离能比氧大的元素是___________ (填元素符号),它们与氧元素电负性由大到小的顺序为___________ 。
(7)根据价层电子对互斥理论判断下列问题:H2S中心原子的杂化方式为___________ 杂化,VSEPR构型为___________ ,分子的立体构型为___________ 。
(8)海洋元素中的氯、溴、碘统称为海水中的卤素资源,它们的化学性质既有相似性,也体现其递变性,用原子结构理论解释原因___________ 。
(1)下列说法不正确的是__________
A. 键是原子轨道以“肩并肩”方式相互重叠而形成的 键是原子轨道以“肩并肩”方式相互重叠而形成的 |
B.2个原子形成的多重共价键中,只能有一个是 键,而 键,而 键可以是一个或多个 键可以是一个或多个 |
C.s电子与s电子间形成的键是 键,p电子与p电子间形成的键是 键,p电子与p电子间形成的键是 键 键 |
| D.共价键一定有原子轨道的重叠 |
| A.氢原子的电子云图中小黑点的疏密表示电子在核外单位体积内出现机会的多少 |
| B.最外层电子数为ns2的元素都在元素周期表第2列 |
C.处于最低能量的原子叫做基态原子,1s22s22p →1s22s22p →1s22s22p 过程中形成的是发射光谱 过程中形成的是发射光谱 |
| D.已知某元素+3价基态离子的核外电子排布式为1s22s22p63s23p63d5,该元素位于周期表中的第四周期ⅥB族位置,属于d区 |
| A.水 | B.CCl4 | C.苯 | D.NiSO4溶液 |
(5)写出与氯同周期,有3个未成对电子的基态原子的价电子轨道表示式为:
(6)元素周期表中与氧元素相邻,且第一电离能比氧大的元素是
(7)根据价层电子对互斥理论判断下列问题:H2S中心原子的杂化方式为
(8)海洋元素中的氯、溴、碘统称为海水中的卤素资源,它们的化学性质既有相似性,也体现其递变性,用原子结构理论解释原因
您最近一年使用:0次
5 . 化学与生活密切相关。下列叙述正确的是
| A.冬奥场馆建筑应用了新材料碲化镉发电玻璃,碲和镉均属于过渡元素 |
| B.“天宫课堂”实验:常温下乙酸钠过饱和溶液结晶成温热“冰球”的过程属于吸热反应 |
| C.食品包装袋中常用的干燥剂有生石灰、还原铁粉、硅胶等 |
| D.干冰可用在舞台上制造“云雾” |
您最近一年使用:0次
6 . 硫酸四氨合铜 可用于织物媒染剂、消毒剂,下列关于硫酸四氨合铜的说不正确的是
可用于织物媒染剂、消毒剂,下列关于硫酸四氨合铜的说不正确的是
 可用于织物媒染剂、消毒剂,下列关于硫酸四氨合铜的说不正确的是
可用于织物媒染剂、消毒剂,下列关于硫酸四氨合铜的说不正确的是| A.硫酸四氨合铜难溶于乙醇 | B.Cu元素位于周期表的ds区 |
C.硫酸四氨合铜中的铜离子为 杂化 杂化 | D.N-H键电子云轮廓图: |
您最近一年使用:0次
解题方法
7 . 下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
(1)③的原子结构示意图为_______ ;
(2)元素①~⑧中金属性最强的是_______ (填元素符号);
(3)元素①~⑧中最高价氧化物对应的水化物酸性最强的是_______ (填化学式);
(4)⑤、⑥元素的金属性强弱依次_______ (填“增大”“减少”或“不变”)。
| 周期 | 族 | |||||||
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)元素①~⑧中金属性最强的是
(3)元素①~⑧中最高价氧化物对应的水化物酸性最强的是
(4)⑤、⑥元素的金属性强弱依次
您最近一年使用:0次
名校
8 . 中国传统文化博大精深,蕴含着丰富的化学知识。下列说法错误的是
| A.“烟花巷陌,依约丹青屏障”中烟花绽放出的绚丽色彩跟原子核外电子跃迁有关 |
| B.KNO3 和Na2SO4 均属于离子晶体 |
| C.《淮南万毕术》中记载:“曾青得铁则化为铜”,铁位于元素周期表的第四周期第Ⅷ 族 |
D.《石灰吟》中记载“要留清白在人间”其中Ca2+ 的结构示意图为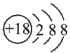 |
您最近一年使用:0次
9 . 下列说法正确的是
A.已知非金属性:Cl>S,则酸性 |
| B.在周期表里,元素所在的族序数一定等于基态原子的最外层电子数 |
C.基态原子的价电子排布式为 的元素位于ds区 的元素位于ds区 |
| D.最外层只有三个电子的元素,一定是ⅢA族元素 |
您最近一年使用:0次
名校
10 . 甲、乙两元素原子的L层电子数都是其他层电子总数的2倍。下列推论正确的是
| A.甲与乙处于同一周期 | B.甲与乙处于同一主族 |
| C.甲与乙都位于元素周期表的p区 | D.甲与乙的最高价氧化物晶体类型不同 |
您最近一年使用:0次
2023-05-24更新
|
23次组卷
|
2卷引用:四川省广元市苍溪中学校2022-2023学年高二下学期5月期中考试化学试题



