名校
1 . 回答下列问题:
(1)无机化合物甲、乙分别由三种元素组成。组成甲、乙化合物的元素原子的特征排布都可表示如下:asa、bsbbpb、csccp2c甲是一种溶解度较小的盐类化合物。由此可知甲、乙的化学式分别是___________ 、___________ 。
(2)根据周期表对角线规则,金属铍与铝的单质及其化合物性质相似,又已知氯化铝的熔、沸点较低,易升化。氢氧化铍与氢氧化镁可用___________ 鉴别,其离子方程式是___________ 。
(3)已知砷(As)元素原子的最外层电子排布是 4s24p3,砷酸钠在酸性条件下能把碘化钾氧化为单质碘,同时生成亚砷酸钠(Na3AsO3)和水,该反应的离子方程式为___________ 。
(1)无机化合物甲、乙分别由三种元素组成。组成甲、乙化合物的元素原子的特征排布都可表示如下:asa、bsbbpb、csccp2c甲是一种溶解度较小的盐类化合物。由此可知甲、乙的化学式分别是
(2)根据周期表对角线规则,金属铍与铝的单质及其化合物性质相似,又已知氯化铝的熔、沸点较低,易升化。氢氧化铍与氢氧化镁可用
(3)已知砷(As)元素原子的最外层电子排布是 4s24p3,砷酸钠在酸性条件下能把碘化钾氧化为单质碘,同时生成亚砷酸钠(Na3AsO3)和水,该反应的离子方程式为
您最近一年使用:0次
解题方法
2 . 按要求填空:
(1)基态Si原子中,电子占据的能量最高的电子层符号为_______ ,该电子层具有的原子轨道数为_______ ,具有的电子数为_______
(2)基态N原子中,核外电子占据_______ 个电子层,_______ 个原子轨道,共有_______ 种运动状态;电子占据的能量最高的原子轨道的形状为_______ 。
(1)基态Si原子中,电子占据的能量最高的电子层符号为
(2)基态N原子中,核外电子占据
您最近一年使用:0次
2022-08-22更新
|
242次组卷
|
2卷引用:专题2 原子结构与元素性质 第一单元 原子核外电子的运动 第1课时 人类对原子结构的认识 原子核外电子的运动特征
名校
3 . A、B两元素。A元素的M层电子数与K层电子数相等;B元素原子的M层电子数等于其L层电子数的一半。则A为_______ ,B为_______ 。
您最近一年使用:0次
名校
4 . 合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为___________ ,占据最高能级电子的电子云轮廓图为___________ 形。
②NH3分子中,与N原子相连的H显正电性。N、H电负性大小顺序为___________ 。
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是___________ 。
②比较Mg、Ca第一电离能的大小:___________ 。O的第一电离能小于N,原因是___________ 。
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
结合数据说明Mg的常见化合价为+2价的原因:___________ 。
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为___________ ,铁在元素周期表中的位置___________ 。
②比较Li+与H-的半径大小关系:r(Li+)___________ r(H-)(填“>”或“<”)。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为
②NH3分子中,与N原子相连的H显正电性。N、H电负性大小顺序为
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②比较Mg、Ca第一电离能的大小:
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
| 元素 | Na | Mg | Al |
| 电离能(kJ/mol) | 496 | 738 | 578 |
| 4562 | 1451 | 1817 | |
| 6912 | 7733 | 2745 | |
| 9543 | 10540 | 11575 |
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为
②比较Li+与H-的半径大小关系:r(Li+)
您最近一年使用:0次
2022-03-15更新
|
804次组卷
|
4卷引用:北京师范大学附属中学2021-2022学年高二上学期期末考试化学试题
5 . 1913年,玻尔提出氢原子模型,电子在线性轨道上绕核运行,然而到了1926年,玻尔建立的线性轨道模型被量子力学推翻。量子力学指出,一定空间运动状态的电子并不在玻尔假定的线性轨道上运行,而在核外空间各处都可能出现,但出现的概率不同,即只能用统计的观点指出它在原子核外空间某处出现机会的多少。下图为多电子原子在核外空间出现的概率图:
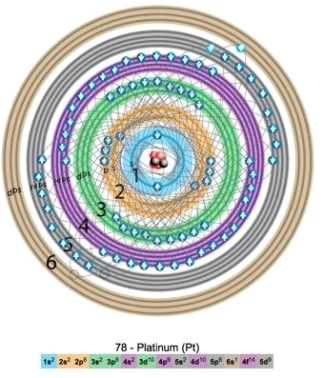
问题:仔细观察图片,你有什么发现?___________

问题:仔细观察图片,你有什么发现?
您最近一年使用:0次
6 . 核外电子排布规律
(1)能量最低原理
电子总是尽可能先从内层排起,当一层充满后再填充下一层,即按___________ 顺序排列。
(2)电子层最多容纳的电子数
①第n层最多容纳___________ 个电子,K、L、M、N层最多容纳的电子数依次为2、8、18、32。
②K层为最外层时最多容纳的电子数为2,除K层外,其他各层为最外层时,最多容纳的电子数为___________ 。
③K层为次外层时,所排电子数为2,除K层外,其他各层为次外层时,最多容纳的电子数为___________ 。
(1)能量最低原理
电子总是尽可能先从内层排起,当一层充满后再填充下一层,即按
(2)电子层最多容纳的电子数
①第n层最多容纳
②K层为最外层时最多容纳的电子数为2,除K层外,其他各层为最外层时,最多容纳的电子数为
③K层为次外层时,所排电子数为2,除K层外,其他各层为次外层时,最多容纳的电子数为
您最近一年使用:0次
解题方法
7 . 硅铝合金广泛应用于航空、交通、建筑、汽车等行业。
完成下列填空:
(1)硅原子的结构示意图为___________ ;比较硅铝的原子半径:r(Si)___________ r(Al)(选填:“>”、“<”或“=”)。硅铝合金中的铝与氢氧化钠溶液反应的化学方程式为___________ 。
(2)氟化铝和氯化铝的熔点分别为1040 和194
和194 ,它们熔点差异大的原因可能是
,它们熔点差异大的原因可能是___________ 。
(3)门捷列夫准确预测了铝、硅下一周期的同主族元素(当时并未被发现)的性质,并将他们分别命名为“类铝”和“类硅”。你据此推断类铝的最外层电子排布式为___________ ,推断的依据是___________ 。
(4)制备硅铝合金时,在高温真空炉中发生如下反应:
 ;
;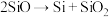 ;
;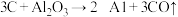
上述反应的最终还原产物为___________ ;当有1mol C参加反应时,转移的电子数目为___________ 。
完成下列填空:
(1)硅原子的结构示意图为
(2)氟化铝和氯化铝的熔点分别为1040
 和194
和194 ,它们熔点差异大的原因可能是
,它们熔点差异大的原因可能是(3)门捷列夫准确预测了铝、硅下一周期的同主族元素(当时并未被发现)的性质,并将他们分别命名为“类铝”和“类硅”。你据此推断类铝的最外层电子排布式为
(4)制备硅铝合金时,在高温真空炉中发生如下反应:
 ;
;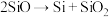 ;
;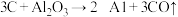
上述反应的最终还原产物为
您最近一年使用:0次
2021-04-20更新
|
416次组卷
|
3卷引用:上海市浦东新区2021届高三二模化学试题
上海市浦东新区2021届高三二模化学试题(已下线)第15讲 原子结构 化学键(练)-2023年高考化学一轮复习讲练测(全国通用)上海市奉贤区致远高级中学2021-2022学年高二上学期期末教学评估(等级考)化学试题
名校
8 . (1)下列状态的镁中,电离最外层一个电子所需能量最大的是_____________ .
A.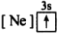 B.
B.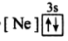 C.
C.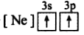 D.
D.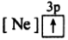
(2) 成为阳离子时首先失去
成为阳离子时首先失去____________ 轨道电子, 的价层电子排布式为
的价层电子排布式为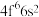 ,
,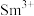 价层电子排布式为
价层电子排布式为____________ .比较离子半径:
____________ (填“大于”“小于”或“等于”) .
.
(3)在周期表中,与 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是___________ ,该元素基态原子核外 层电子的自旋
层电子的自旋___________ (填“相同”或“相反”). 中,电负性最高的元素是
中,电负性最高的元素是___________ .
(4) 基态核外电子排布式为
基态核外电子排布式为___________ .
A.
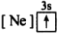 B.
B.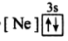 C.
C. D.
D.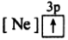
(2)
 成为阳离子时首先失去
成为阳离子时首先失去 的价层电子排布式为
的价层电子排布式为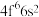 ,
,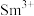 价层电子排布式为
价层电子排布式为
 .
.(3)在周期表中,与
 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是 层电子的自旋
层电子的自旋 中,电负性最高的元素是
中,电负性最高的元素是(4)
 基态核外电子排布式为
基态核外电子排布式为
您最近一年使用:0次
2021-02-01更新
|
1080次组卷
|
4卷引用:鲁科版2019选择性必修2第1章 原子结构与元素性质 第1章学科素养提升
9 . 氢气的生产、存储是氢能应用的核心。目前较成熟的生产、存储路线之一为:利用CH3OH和H2O在某Cu/Zn-Al催化剂存在下生产H2, H2与Mg在一定条件下制得储氢物质X。
回答问题: .
(1) Al在周期表中的位置______________ 。基态Zn的价层电子排布式___________ 。
(2)水分了中氧原子的杂化轨道类型_______________ 。
(3)键能是衡量共价键稳定性的参数之一。 CH3OH键参数中有_________ 种键能数据。CH3OH可以与水以任意比例互溶的原因是___________________ 。
(4) X的晶胞结构如图所示(晶胞参数:α =β =γ=90º,a=b=450.25 pm),密度为1.4g cm-3, H-的配位数为______________ , X的储氢质量分数是______________ ,c= ___________ pm (列出计算式即可)。
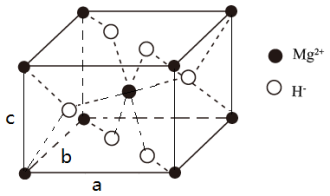
回答问题: .
(1) Al在周期表中的位置
(2)水分了中氧原子的杂化轨道类型
(3)键能是衡量共价键稳定性的参数之一。 CH3OH键参数中有
(4) X的晶胞结构如图所示(晶胞参数:α =β =γ=90º,a=b=450.25 pm),密度为1.4g cm-3, H-的配位数为

您最近一年使用:0次
2020-10-12更新
|
4091次组卷
|
5卷引用:2020年海南省高考化学试卷(新高考)
2020年海南省高考化学试卷(新高考)(已下线)难点10 物质结构与性质综合题-2021年高考化学【热点·重点·难点】专练(新高考)(已下线)专题13 物质结构与性质—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)2020年海南卷化学高考真题变式题15-19北京市第一六一中学2021-2022学年高三上学期期中考试化学试题
名校
解题方法
10 . 根据要求填空:
(1)A元素原子的M层电子数是其电子总数的 ,则其原子结构示意图为
,则其原子结构示意图为__ ;其简单离子的电子式为___ 。
(2)下列图示表示同种元素的是___ ;化学性质相似的是___ ;属于离子的是__ 。
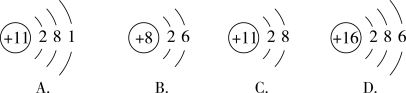
(3)已知Mm+与Nn-具有相同的电子层结构,若N的核电荷数为a,M的质量数为A,则M的中子数为__ ,两者形成的化合物的化学式可能为__ 。
(1)A元素原子的M层电子数是其电子总数的
 ,则其原子结构示意图为
,则其原子结构示意图为(2)下列图示表示同种元素的是
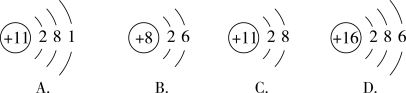
(3)已知Mm+与Nn-具有相同的电子层结构,若N的核电荷数为a,M的质量数为A,则M的中子数为
您最近一年使用:0次



