名校
1 . 普鲁士蓝的化学式为 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A.该物质中 与 与 数目之比为 数目之比为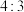 |
B. 该物质中含 该物质中含 数目为 数目为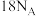 |
| C.该物质中只存在共价键和配位键,不存在离子键 |
D. 的核外电子排布式为 的核外电子排布式为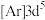 |
您最近一年使用:0次
2021-05-21更新
|
345次组卷
|
4卷引用:山东省潍坊市四县市(安丘,诸城,五莲,兰山)2021届高考模拟化学试题
解题方法
2 . 下列说法错误的是
| A.非金属单质中一定不含离子键,一定只含共价键 |
| B.化学键是相邻原子之间的强相互作用 |
| C.酸雨后钢铁易发生析氢腐蚀,日常铁锅存留盐液时易发生吸氧腐蚀 |
| D.电热水器有镁棒防止内胆腐蚀是牺牲阳极保护法 |
您最近一年使用:0次
名校
3 . 三硫化磷(P4S3)是黄绿色针状晶体,易燃、有毒,分子结构之一如图所示。已知其燃烧时P被氧化为P4O10,下列有关P4S3的说法中不正确的是


| A.P4S3中既含离子键又含共价键 |
| B.P4S3属于共价化合物 |
| C.1molP4S3分子中含有9mol共价键 |
D.P4S3充分燃烧的化学方程式为P4S3+8O2 P4O10+3SO2 P4O10+3SO2 |
您最近一年使用:0次
2022-09-25更新
|
100次组卷
|
2卷引用:山东省菏泽市单县第五中学2021-2022学年高一下学期第一次段考化学(A)试题
解题方法
4 . 胍(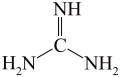 )是一元强碱,分子构型为平面型,其盐酸盐(
)是一元强碱,分子构型为平面型,其盐酸盐(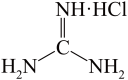 )是核酸检测液的主要成分。下列说法错误的是
)是核酸检测液的主要成分。下列说法错误的是
 )是一元强碱,分子构型为平面型,其盐酸盐(
)是一元强碱,分子构型为平面型,其盐酸盐( )是核酸检测液的主要成分。下列说法错误的是
)是核酸检测液的主要成分。下列说法错误的是| A.胍中C、N杂化方式均为sp2 | B.胍具有很强的吸湿性 |
| C.胍的熔点低于胍盐 | D.胍盐中含有的化学键均为极性键 |
您最近一年使用:0次
名校
解题方法
5 . 全氮阴离子盐是一种新型超高能含能材料,全氮阴离子化学式为N ,某种全氮阴离子盐结构如图。下列有关说法正确的是
,某种全氮阴离子盐结构如图。下列有关说法正确的是
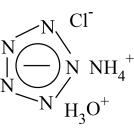
 ,某种全氮阴离子盐结构如图。下列有关说法正确的是
,某种全氮阴离子盐结构如图。下列有关说法正确的是
| A.该全氮阴离子盐属于有机物 |
B.N 的摩尔质量为71g/mol 的摩尔质量为71g/mol |
C.每个 N 含有26个电子 含有26个电子 |
| D.该全氮阴离子盐既含共价键又含离子键 |
您最近一年使用:0次
解题方法
6 . 下列物质中,含有非极性共价键的是
| A.KOH | B.H2S | C.Na2O2 | D.MgCl2 |
您最近一年使用:0次
2021-01-28更新
|
234次组卷
|
2卷引用:山东省济宁市2020-2021学年高一上学期质量检测化学试题
7 . 下列说法正确的是
| A.离子化合物中,一个阴离子可同时与多个阳离子之间有静电作用 |
| B.离子化合物中的阳离子中都只含金属元素,阴离子中都不含金属元素 |
| C.通过化学变化可以实现16O与18O间的相互转化 |
| D.溶于水可以导电的化合物一定是离子化合物 |
您最近一年使用:0次
名校
8 . 下面是同学们熟悉的物质:
①O2 ②H2O2 ③MgCl2 ④H2SO4 ⑤Na2CO3⑥NH4Cl ⑦CO2 ⑧Ne ⑨Na2O2 ⑩NaOH
(1)这些物质中,只含有共价键的是__________________________________ (填序号,下同);只含有离子键的是___________________________ ;既含有极性共价键又含有离子键的是_____________________________ ;既含有非极性共价键又含有离子键的是________________________ 不存在化学键的是_________________________________ 。
属于共价化合物的是_________________________________ ;
(2)写出下列物质的结构式
①O2_______________ ②H2O2_______________ ⑦CO2_______________
(3)写出下列物质的电子式
⑥NH4Cl______________ ⑨Na2O2 _______________ ⑩NaOH_______________
(4)用电子式表示下列物质的形成
①O2_______________________________________________________________
③MgCl2____________________________________________________________
①O2 ②H2O2 ③MgCl2 ④H2SO4 ⑤Na2CO3⑥NH4Cl ⑦CO2 ⑧Ne ⑨Na2O2 ⑩NaOH
(1)这些物质中,只含有共价键的是
属于共价化合物的是
(2)写出下列物质的结构式
①O2
(3)写出下列物质的电子式
⑥NH4Cl
(4)用电子式表示下列物质的形成
①O2
③MgCl2
您最近一年使用:0次
2019-12-29更新
|
512次组卷
|
2卷引用:山东省临沂市沂水县第一中学2019—2020学年高一上学期12月份月考化学试题
9 . 某种含铜的催化剂 可用于汽车尾气脱氮,催化机理如图所示。下列说法错误的是
可用于汽车尾气脱氮,催化机理如图所示。下列说法错误的是
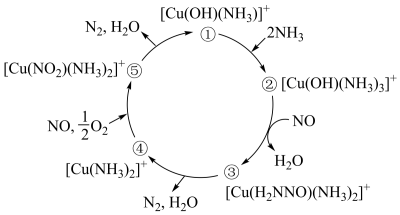
 可用于汽车尾气脱氮,催化机理如图所示。下列说法错误的是
可用于汽车尾气脱氮,催化机理如图所示。下列说法错误的是
| A.每一步骤只存在铜和氮元素之间的电子转移 |
B.该催化循环中 的成键数目发生了变化 的成键数目发生了变化 |
| C.反应过程中存在非极性键的断裂和形成 |
D.总反应的化学方程式为 |
您最近一年使用:0次
解题方法
10 . 我国采用的Cu2O/TiO2–NaBiO3光催化氧化技术能深度净化工业含有机物的废水。回答下列问题:
(1)钛(Ti)的基态原子M能层中能量不同的电子有_____________ 种。
(2)该技术能有效将含有机物废水中的农药、醇、油等降解为水、二氧化碳、硝酸根离子等小分子。
①H2O、CH3OH、 分子中O-H键的极性最强的是
分子中O-H键的极性最强的是_____________ 。
②C、N、O三种元素的电负性由大到小的顺序是_____________ 。
(3)将少量无水硫酸铜溶解在水中,形成蓝色溶液,再加入过量氨水,溶液变为深蓝色。深蓝色离子的结构如图所示,lmol该离子中所含σ键为_____________ mol(包括配位键);向深蓝色溶液中缓慢加入乙醇,得到深蓝色晶体,加热该晶体先失去组分b的原因是_____________ 。
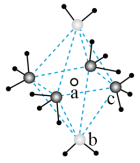
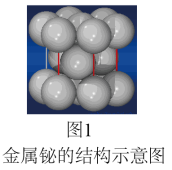
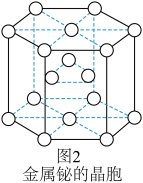
(4)铋合金具有凝固时不收缩的特性,用于铸造高精度铸型。金属铋的结构示意图如图1所示,其晶胞结构如图2所示。若铋原子的半径为rpm,则该晶体的密度为_____________ g•cm-3 (用含r和NA数学表达式表示)。
(1)钛(Ti)的基态原子M能层中能量不同的电子有
(2)该技术能有效将含有机物废水中的农药、醇、油等降解为水、二氧化碳、硝酸根离子等小分子。
①H2O、CH3OH、
 分子中O-H键的极性最强的是
分子中O-H键的极性最强的是②C、N、O三种元素的电负性由大到小的顺序是
(3)将少量无水硫酸铜溶解在水中,形成蓝色溶液,再加入过量氨水,溶液变为深蓝色。深蓝色离子的结构如图所示,lmol该离子中所含σ键为

(4)铋合金具有凝固时不收缩的特性,用于铸造高精度铸型。金属铋的结构示意图如图1所示,其晶胞结构如图2所示。若铋原子的半径为rpm,则该晶体的密度为


您最近一年使用:0次



