解题方法
1 . 下列说法错误的是
| A.“雪花六出”体现了晶体的自范性 |
| B.防撞气囊中的NaN3是一种含有共价键的离子化合物 |
| C.钛镁合金的导电性和导热性是通过自由电子定向移动实现的 |
| D.冠醚(18-冠-6)的空穴与K+尺寸适配,两者能通过弱相互作用形成超分子 |
您最近一年使用:0次
名校
2 . 下列分子的结构式、化学键类型、空间构型的说法均正确的有
| 分子化学式 | 结构式 | 化学键类型 | 空间构型 | |
| A | HClO | H—Cl—O | 极性键 | 直线形 |
| B | CO2 | O=C=O | 极性键 | 直线形 |
| C | H2O | H—O—H | 非极性键 | 直线形 |
| D | CH4 | H—H—C—H—H | 非极性键 | 正方形 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 下列说法正确的有
| A.硫酸氢钠晶体加热至熔融态破坏了离子键 |
| B.干冰升华破坏了共价键 |
| C.冰融化破坏了氢键和离子键 |
| D.氯化氢溶于水破坏了离子键 |
您最近一年使用:0次
名校
解题方法
4 . 下列说法正确的有
| A.强酸都是离子化合物 |
| B.共价化合物一定不含离子键 |
| C.离子化合物中一定含有金属元素 |
| D.含有金属元素的一定是离子化合物 |
您最近一年使用:0次
名校
解题方法
5 . 下列说法中正确的是
①非金属元素不可能形成离子化合物 ②位于第四周期第VA族的元素为非金属元素
③可用质谱法区分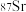 和
和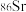 ④金属晶体的导电性、导热性均与自由电子有关
④金属晶体的导电性、导热性均与自由电子有关
⑤分子晶体中一定存在共价键 ⑥金刚石与石墨中的C―C―C夹角都为120°
⑦NaCl晶体中,阴离子周围紧邻的阳离子数为6
⑧NaClO和NaCl均为离子化合物,它们所含的化学键类型完全相同
①非金属元素不可能形成离子化合物 ②位于第四周期第VA族的元素为非金属元素
③可用质谱法区分
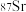 和
和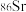 ④金属晶体的导电性、导热性均与自由电子有关
④金属晶体的导电性、导热性均与自由电子有关⑤分子晶体中一定存在共价键 ⑥金刚石与石墨中的C―C―C夹角都为120°
⑦NaCl晶体中,阴离子周围紧邻的阳离子数为6
⑧NaClO和NaCl均为离子化合物,它们所含的化学键类型完全相同
| A.①③④⑥ | B.②③④⑦ | C.②③④⑤ | D.②③④⑧ |
您最近一年使用:0次
2024-02-22更新
|
297次组卷
|
2卷引用:山东省青岛市2023-2024学年高二上学期1月期末化学试题
名校
解题方法
6 . 短周期元素形成的一种麻醉剂的结构式如图所示,其中X、Y、Z、W、E原子序数依次增大,且分布于三个短周期,下列说法正确的是
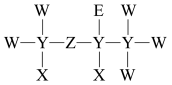
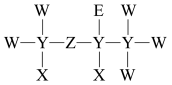
| A.氮元素和X可以形成既含离子键又含共价键的化合物 |
| B.五种元素中,W的非金属性最强,其最高价含氧酸的酸性最强 |
| C.E的含氧酸中,E的价态越高,其氧化性越强 |
| D.X和Z组成的二元化合物一定只含由极性键 |
您最近一年使用:0次
名校
解题方法
7 . 随着原子序数的递增,7种短周期元素A~G的最高正价或最低负价与原子序数的关系如图。
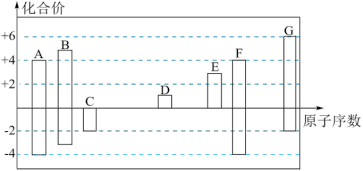
回答下列问题:
(1)写出中子数为8的A元素的一种核素的化学符号_______ 。
(2)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为_______ 。
(3)E元素最高价氧化物对应水化物与氢氧化钠溶液反应的离子方程式为_______ 。
(4)元素A与G形成的电子总数为38的分子的结构式为_______ 。
(5)元素C与D按原子个数比1:1形成的化合物的电子式为_______ ,所含有化学键类型有_______ 。
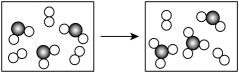
(6)如图表示由C、G元素组成的两种气体分子在一定条件下的密闭容器中充分反应的转化关系,请写出该转化过程的化学方程式:_______ 。

回答下列问题:
(1)写出中子数为8的A元素的一种核素的化学符号
(2)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为
(3)E元素最高价氧化物对应水化物与氢氧化钠溶液反应的离子方程式为
(4)元素A与G形成的电子总数为38的分子的结构式为
(5)元素C与D按原子个数比1:1形成的化合物的电子式为
(6)如图表示由C、G元素组成的两种气体分子在一定条件下的密闭容器中充分反应的转化关系,请写出该转化过程的化学方程式:

您最近一年使用:0次
解题方法
8 . 人体必需的一些元素在周期表中的分布情况如下:
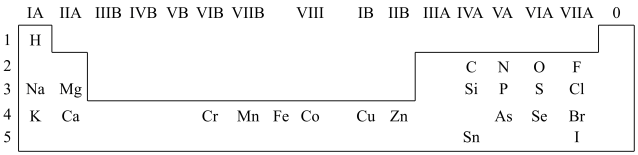
(1)请在上图中画出金属与非金属的分界线______ 。
(2)Na与O形成的原子个数比为1:1的化合物所含的化学键类型为______ 。
(3)锡(Sn)与C为同一主族元素,Sn原子比C原子多三个电子层,则Sn的原子序数为______ 。
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是______ (填字母)。
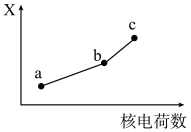
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是______(填字母)。
(6)某小组为探究 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:
资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
实验②观察到的现象是______ ,甲同学根据此现象得出结论:氧化性 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,其理由是
,其理由是______ 。试从原子结构的角度解释卤素单质的氧化性递变规律:同一主族元素从上到下,______ ,因此,元素的非金属性逐渐减弱,对应的单质的氧化性逐渐减弱。

(1)请在上图中画出金属与非金属的分界线
(2)Na与O形成的原子个数比为1:1的化合物所含的化学键类型为
(3)锡(Sn)与C为同一主族元素,Sn原子比C原子多三个电子层,则Sn的原子序数为
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是
| A | B | C | D |
| HCl | H₂O | CO₂ | CH₄ |
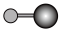 | 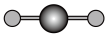 | 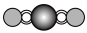 | 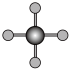 |
| 直线形 | 直线形 | 直线形 | 平面正方形 |
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是______(填字母)。

| A.若a、b、c表示碱金属元素,则X表示对应单质的密度 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示第ⅥA族元素,则X表示对应氢化物的稳定性 |
| D.若a、b、c表示第ⅡA族元素,则X表示最高价氧化物对应水化物的碱性 |
(6)某小组为探究
 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
| 序号 | 实验① | 实验② |
| 实验操作 |  |  |
| 现象 | 溶液变为黄色 |
 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,其理由是
,其理由是
您最近一年使用:0次
名校
9 . 利用“价类二维图”研究物质的性质是化学研究的重要手段。如图是氯元素的化合价与部分物质类别的对应关系。下列说法正确的是


| A.D中含有的化学键类型只有离子键 |
| B.将E溶液滴入碳酸氢钠溶液中,有大量气泡产生 |
| C.A、B、C均属于电解质 |
| D.C的酸性和氧化性均强于E |
您最近一年使用:0次
解题方法
10 . 现有下列六种物质:
① ②过氧化钠 ③
②过氧化钠 ③ ④
④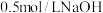 溶液 ⑤碳酸氢钠 ⑥
溶液 ⑤碳酸氢钠 ⑥ 。请根据上述物质回答下列问题:
。请根据上述物质回答下列问题:
(1)在上述物质中属于酸性氧化物的有___________ (填①~⑥序号)。
(2)含有 氧原子的②与足量①反应,产生的气体在标准状况下的体积为
氧原子的②与足量①反应,产生的气体在标准状况下的体积为___________ L。
(3)写出⑥在水溶液中的电离方程式___________ 。
(4)②所含化学键类型为___________ 。
(5)某同学帮助水质检测站配制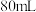 ④以备使用。
④以备使用。
①该同学应用托盘天平称取 固体
固体___________ g。
②配制过程所需的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、___________ 。
③定容时仰视刻度线,则所配制的溶液的浓度会___________ (填“偏高”、“偏低”、“不变”)。
(6)④和⑤的溶液混合,发生反应的离子方程式为___________ 。
①
 ②过氧化钠 ③
②过氧化钠 ③ ④
④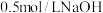 溶液 ⑤碳酸氢钠 ⑥
溶液 ⑤碳酸氢钠 ⑥ 。请根据上述物质回答下列问题:
。请根据上述物质回答下列问题:(1)在上述物质中属于酸性氧化物的有
(2)含有
 氧原子的②与足量①反应,产生的气体在标准状况下的体积为
氧原子的②与足量①反应,产生的气体在标准状况下的体积为(3)写出⑥在水溶液中的电离方程式
(4)②所含化学键类型为
(5)某同学帮助水质检测站配制
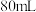 ④以备使用。
④以备使用。①该同学应用托盘天平称取
 固体
固体②配制过程所需的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、
③定容时仰视刻度线,则所配制的溶液的浓度会
(6)④和⑤的溶液混合,发生反应的离子方程式为
您最近一年使用:0次



