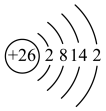
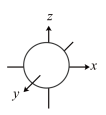
1 . 下列图示或化学用语表示正确的是
|
|
|
|
| A.NaCl的电子式 | B.基态47Ag的价层电子轨道表示式 | C.Fe2+的结构示意图 | D.px轨道的电子云轮廓图 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 按要求回答下列问题:
(1)基态K原子中,核外电子占据最高能层的符号是___ ,占据该能层电子的电子云轮廓图形状____ 。
(2)Fe成为阳离子时首先失去_______ 轨道电子,写出Fe2+简化核外电子排布_______ 。
(3)P位于元素周期表中第三周期_______ 族,基态P原子核外未成对电子有_______ 个。
(1)基态K原子中,核外电子占据最高能层的符号是
(2)Fe成为阳离子时首先失去
(3)P位于元素周期表中第三周期
您最近半年使用:0次
3 . 现有六种元素,其中A、B、C、D、E为短周期主族元素,F为第4周期元素,它们的原子序数依次增大。请根据下列相关信息回答问题。
(1)B元素基态原子具有___________ 种运动状态不同的电子,能量最高的电子,其电子云在空间有___________ 个伸 展方向。
(2)根据上述信息,画出C元素基态原子的轨道表示式___________ 。
(3)F在元素周期表中属于___________ 区元素。
(4)写出DA3的电子式:___________ (用元素符号表示)。
| 元素 | 相关信息 |
| A | 元素的原子核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 元素原子的核外p电子数比s电子数少1 |
| C | 元素的第一至第四电离能分别是I1=738 kJ/mol、I2=1451 kJ/mol、I3= 7733 kJ/mol、I4= 10540 kJ/mol |
| D | 原子核外填充电子的所有p轨道全满或半满 |
| E | 元素的主族序数与周期序数的差为3 |
| F | 在元素周期表的第6列 |
(2)根据上述信息,画出C元素基态原子的轨道表示式
(3)F在元素周期表中属于
(4)写出DA3的电子式:
您最近半年使用:0次
4 . 聚氮化硫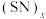 是重要的超导材料,目前已成为全球材料行业研究的热点。
是重要的超导材料,目前已成为全球材料行业研究的热点。
(1)基态S原子的原子核外能量最高的电子电子云轮廓图为___________ 形。
(2)下列电子排布图能表示氮原子的最低能量状态的是___________。
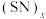 是重要的超导材料,目前已成为全球材料行业研究的热点。
是重要的超导材料,目前已成为全球材料行业研究的热点。(1)基态S原子的原子核外能量最高的电子电子云轮廓图为
(2)下列电子排布图能表示氮原子的最低能量状态的是___________。
A. | B.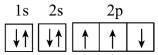 |
C.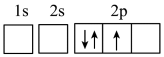 | D. |
您最近半年使用:0次
5 . 硅原子核外电子运动状态为___________ 种;基态Si原子,若其电子排布式表示为 违背了
违背了___________ 。
 违背了
违背了
您最近半年使用:0次
解题方法
6 . 氧化二氯(Cl2O)是净化饮用水的一种有效的净水剂,制备反应为 ,下列说法错误的是
,下列说法错误的是
 ,下列说法错误的是
,下列说法错误的是A.Cl2O的结构式为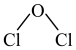 | B.键角 |
C. 中心原子的杂化方式为 中心原子的杂化方式为 | D.Cl2的电子云轮廓图为 |
您最近半年使用:0次
7 . 下列关于电子云或原子轨道的叙述中,正确的是
| A.电子云图中的小黑点越密,表示原子核外单位体积内的电子越多 |
| B.原子轨道是电子运动的轨迹 |
| C.原子轨道表示电子在空间各处出现的概率 |
| D.电子云用小黑点的疏密程度来表示电子在原子核外单位体积内出现概率的大小 |
您最近半年使用:0次
解题方法
8 . 氨硼烷 含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。氨硼烷在催化剂作用下水解放出氢气:
含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。氨硼烷在催化剂作用下水解放出氢气: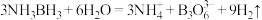 ,
, 的结构如图。下列说法正确的是
的结构如图。下列说法正确的是
 含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。氨硼烷在催化剂作用下水解放出氢气:
含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。氨硼烷在催化剂作用下水解放出氢气: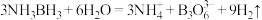 ,
, 的结构如图。下列说法正确的是
的结构如图。下列说法正确的是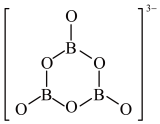
| A.基态B原子电子占据最高能级的电子云轮廓图为球形 |
| B.第一电离能:O>N>B |
| C.原子半径:N>B>H |
D. 中各原子均在同一平面内 中各原子均在同一平面内 |
您最近半年使用:0次
名校
解题方法
9 . 2023年6月,科学家首次合成含铍-铍能的固态化合物,相关成果发表于《科学》杂质。该分子入选2023年最“炫”分子榜单,其结构如图所示,回答下列问题: 原子最外层电子的电子云轮廓图为
原子最外层电子的电子云轮廓图为_____ (填序号)。
A.球形 B.哑铃形
(2)下列电子排布式分别代表铍微粒,其中失去1个电子所需能量最多的是_____。
(3)“固态双铍化合物的化学式为_____ ,它不含_____ (填标号)。
A.极性键 B.非极性键 C.金属键 D. 键
键
(4)卤化铍的熔点如表所示:
① 中
中 原子的杂化方式为
原子的杂化方式为_____ ;
②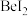
_____ (填“能”或“不能)溶于四氯化碳:
③ 、
、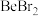 、
、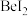 的熔点依次升高的原因是
的熔点依次升高的原因是_____ 。
(5) 易形成配离子
易形成配离子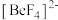 ,其中心阳离子的配位数为
,其中心阳离子的配位数为_____ ,配体是_____ (填化学符号),配离子的空间构型为_____ 。
(6)离子晶体中稳定配位多面体的理论半径比如表所示:
已知铍离子、氧离子的半径分别为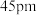 、
、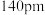 ,
, 的配位多面体是
的配位多面体是_____ 。
(7)Be的某种氧化物晶体是制备氟硼铍酸钾晶体的原料之一,其晶胞结构如图所示。这种氧化物的化学式为_____ ;设晶胞参数为 ,用
,用 表示阿伏加德罗参数的值,则
表示阿伏加德罗参数的值,则 晶体的密度为
晶体的密度为_____  (用含a和
(用含a和 的式子表示)。
的式子表示)。
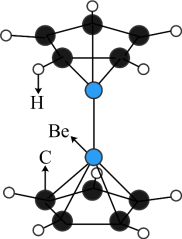
 原子最外层电子的电子云轮廓图为
原子最外层电子的电子云轮廓图为A.球形 B.哑铃形
(2)下列电子排布式分别代表铍微粒,其中失去1个电子所需能量最多的是_____。
A.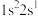 | B. | C.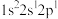 | D. |
(3)“固态双铍化合物的化学式为
A.极性键 B.非极性键 C.金属键 D.
 键
键(4)卤化铍的熔点如表所示:
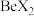 | 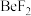 |  | 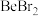 | 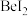 |
熔点/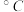 | 552 | 399 | 488 | 510 |
 中
中 原子的杂化方式为
原子的杂化方式为②
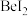
③
 、
、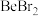 、
、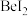 的熔点依次升高的原因是
的熔点依次升高的原因是(5)
 易形成配离子
易形成配离子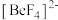 ,其中心阳离子的配位数为
,其中心阳离子的配位数为(6)离子晶体中稳定配位多面体的理论半径比如表所示:
| 配位多面体 | 配位数 | 半径比(r+/r-) |
| 平面三角形 | 3 | 0.15~0.225 |
| 四面体 | 4 | 0.225~0.414 |
| 八面体 | 6 | 0.414~0.732 |
| 立方体 | 8 | 0.732~1.000 |
| 立方八面体 | 12 | 1.000 |
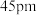 、
、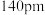 ,
, 的配位多面体是
的配位多面体是(7)Be的某种氧化物晶体是制备氟硼铍酸钾晶体的原料之一,其晶胞结构如图所示。这种氧化物的化学式为
 ,用
,用 表示阿伏加德罗参数的值,则
表示阿伏加德罗参数的值,则 晶体的密度为
晶体的密度为 (用含a和
(用含a和 的式子表示)。
的式子表示)。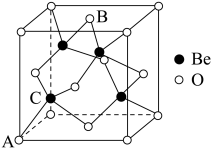
您最近半年使用:0次
名校
解题方法
10 . 下列化学用语正确的是
A. 的VSEPR模型: 的VSEPR模型: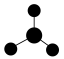 |
B.乙烯的球棍模型为: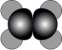 |
C.乙醚的键线式为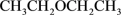 |
D.镁原子最外层电子的电子云轮廊图: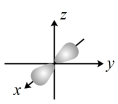 |
您最近半年使用:0次