解题方法
1 . 回答下列问题。
(1)氮元素在元素周期表中的位置是第___________ 周期,第___________ 族。
(2) 是元素周期表中第
是元素周期表中第___________ 号元素。
(3) 的M能层电子排布式是
的M能层电子排布式是___________ ,价层电子排布图是___________ ,原子结构示意图是___________ 。
(1)氮元素在元素周期表中的位置是第
(2)
 是元素周期表中第
是元素周期表中第(3)
 的M能层电子排布式是
的M能层电子排布式是
您最近一年使用:0次
2 . 下列关于价电子排布3s23p4的描述正确的是
| A.它的元素符号为O |
| B.它的核外电子排布式为1s22s22p63s23p4 |
| C.可以与H2化合生成液态化合物 |
D.其电子排布图为 |
您最近一年使用:0次
2024-04-13更新
|
211次组卷
|
44卷引用:宁夏回族自治区青铜峡市高级中学2018-2019学年高二上学期期末考试化学试题
宁夏回族自治区青铜峡市高级中学2018-2019学年高二上学期期末考试化学试题宁夏青铜峡市高级中学2021-2022学年高二上学期期末考试化学试题(已下线)吉林一中2009--2010学年度下学期期末考试第一次质量检测高二化学试卷宁夏育才中学2016-2017学年高二下学期期中考试化学试题【全国校级联考】新疆昌吉市教育共同体四校2017-2018学年高二下学期期末联考化学试题宁夏回族自治区银川市长庆高级中学2018-2019学年高二下学期第二次月考化学试题福建省长泰县第一中学2018-2019学年高二下学期期末考试化学试题新疆新源县第二中学2019-2020学年高二下学期期末考试化学试题宁夏石嘴山市平罗中学2021-2022学年高二上学期期中考试化学试题宁夏吴忠市吴忠中学2022-2023学年高三上学期阶段性测试 化学试题江西省南昌市八一中学2022-2023学年高二上学期1月期末考试化学试题(已下线)2011-2012学年福建省厦门一中高二上学期期中考试化学试卷(已下线)2012届浙江省杭州高中高三第二次月考化学试卷(已下线)2011-2012学年内蒙古包头三十三中高二下学期期中考试化学试卷(已下线)2011-2012学年河南许昌鄢陵一高高二下学期期中考试化学试卷(已下线)2012-2013学年山东省淄博市沂源一中高二下学期期中模块检测化学卷(已下线)2012-2013学年山东省济南一中高二下学期期中考试理科化学试卷(已下线)2013-2014学年福建省厦门一中高二上学期期中考试化学试卷2013-2014山东省即墨市高二下学期期中考试化学试卷2015-2016学年西藏日喀则一中高二10月月考化学试卷2015-2016学年贵州省思南中学高二下第二次月考化学试卷江苏省盘湾中学、陈洋中学2017-2018学年高二上学期期中联考(选修)化学试题2016-2017学年高中化学选修3(人教版)模块综合测评云南省武定县第一中学2018-2019学年高二上学期12月份考试化学试题云南省昭通水田新区中学2018-2019学年高二上学期12月月考化学试题新疆维吾尔自治区北京大学附属中学新疆分校2018-2019学年高二下学期期中考试化学试题新疆石河子第二中学2018-2019学年高二下学期第一次月考化学试题河南省林州市第一中学2019-2020学年高二3月线上调研考试化学试题江苏省盐城市伍佑中学2019-2020学年高二下学期第一次阶段考试化学试题湖北省武汉市黄陂区第六中学2019-2020学年高二下学期三月线上考试化学试题甘肃省静宁县第一中学2019-2020学年高二下学期期中考试(第二次月考)化学试题(普通班)广西防城港市防城中学2019-2020学年高二下学期期中考试化学试题湖北省仙桃市汉江中学2018-2019学年高二下学期期中考试化学试题(已下线)考点33 原子结构与性质-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)课时54 原子结构与性质-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点46 原子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)黑龙江省牡丹江市海林市朝鲜族中学2021-2022学年高二下学期第一次月考化学试题河北省保定高碑店市崇德实验中学2022-2023学年高三上学期10月月考化学试题重庆市西南大学附属中学校2022-2023学年高二上学期开学定时训练化学试题(广延班)(已下线)考点41 原子结构与性质(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第01讲 原子结构-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)(已下线)选择题6-10(已下线)第一章章节专项提升贵州省遵义市桐梓县荣兴高级中学2023-2024学年高二下学期第一次(3月)月考化学试题
名校
3 . 中国近代化学启蒙者徐寿首次把“Nitrogen”译成中文时曾写成“淡气”,意指它“冲淡”了空气中的氧气。含氮化合物种类繁多,用途广泛,根据信息回答下列问题。
(1)GaN是第三代半导体材料,基态Ga的电子排布式为_______ ,GaN晶体为共价键空间网状结构,熔点1700℃,晶体类型为_______ 。
(2)硫酸四氨合铂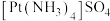 在工业上用于镀铂,Pt的配位数为
在工业上用于镀铂,Pt的配位数为_______ ,其阴离子的空间构型为_______ 。
(3)氨缩脲与胆矾溶液反应得到如下图所示的紫色离子,离子中碳原子、氮原子的杂化类型分别是_______ 、_______ 。O的第二电离能比N第二电离能更大,解释其原因是_______ 。 气体常用作天然气的警报剂。
气体常用作天然气的警报剂。 与其同分异构体
与其同分异构体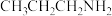 相比较,熔点较高的是
相比较,熔点较高的是_______ 。 易与
易与 形成三甲胺正离子,反应中形成的化学键属于
形成三甲胺正离子,反应中形成的化学键属于_______ 。
A.氢键 B.极性键 C.π键 D.配位键
(5)某铁氮化合物晶体的晶胞结构如图所示。_______ 。
②若晶胞中距离最近的两个铁原子距离为apm,阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为_______  (列出计算式即可)。
(列出计算式即可)。
(1)GaN是第三代半导体材料,基态Ga的电子排布式为
(2)硫酸四氨合铂
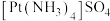 在工业上用于镀铂,Pt的配位数为
在工业上用于镀铂,Pt的配位数为(3)氨缩脲与胆矾溶液反应得到如下图所示的紫色离子,离子中碳原子、氮原子的杂化类型分别是

 气体常用作天然气的警报剂。
气体常用作天然气的警报剂。 与其同分异构体
与其同分异构体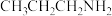 相比较,熔点较高的是
相比较,熔点较高的是 易与
易与 形成三甲胺正离子,反应中形成的化学键属于
形成三甲胺正离子,反应中形成的化学键属于A.氢键 B.极性键 C.π键 D.配位键
(5)某铁氮化合物晶体的晶胞结构如图所示。

②若晶胞中距离最近的两个铁原子距离为apm,阿伏加德罗常数的值为
 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
2024-03-10更新
|
139次组卷
|
2卷引用:宁夏回族自治区石嘴山市第三中学2023-2024学年高三上学期期末考试理综试题-高中化学
名校
解题方法
4 . 艾姆斯实验室已制造出包含钙、钾、铁和砷以及少量镍的CaK(Fe1-xNix)4As4新型化合物材料。回答下列问题:
(1)基态镍原子的外围电子排布式为___________ 。
(2)在稀氨水介质中,Ni2+与丁二酮肟(分子式为C4H8N2O2)反应可生成鲜红色沉淀,其分子结构如下图所示,该结构中碳原子的杂化方式为___________ ;其中碳、氮、氧三种元素第一电离能由大到小的顺序为___________ (用元素符号表示)。
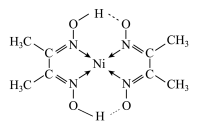
(3)铁、镍易与CO作用形成羰基配合物Fe(CO)5、Ni(CO)4;1mol Fe(CO)5分子中含有σ 键数目为___________ ;已知Ni(CO)4分子为正四面体构型,下列溶剂能够溶解Ni(CO)4的是___________ (填字母)。
a.四氯化碳 b.苯 c.水 d.液氨
(4)K3AsO3可用于碘的微量分析,AsO 的立体构型为
的立体构型为___________ ,写出一种与其互为等电子体的分子___________ (填化学式)。
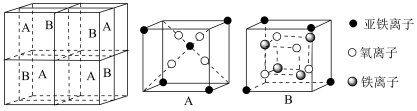
(5)某种离子型铁的氧化物晶胞如图所示,它由A、B方块组成。则该化合物中Fe2+、Fe3+、O2-的个数比为___________ (填最简整数比);已知该晶体的密度dg/cm3,阿伏加德罗常数的值为NA,则晶胞参数为___________ nm(用含d和NA的代数式表示)。
(1)基态镍原子的外围电子排布式为
(2)在稀氨水介质中,Ni2+与丁二酮肟(分子式为C4H8N2O2)反应可生成鲜红色沉淀,其分子结构如下图所示,该结构中碳原子的杂化方式为

(3)铁、镍易与CO作用形成羰基配合物Fe(CO)5、Ni(CO)4;1mol Fe(CO)5分子中含有σ 键数目为
a.四氯化碳 b.苯 c.水 d.液氨
(4)K3AsO3可用于碘的微量分析,AsO
 的立体构型为
的立体构型为(5)某种离子型铁的氧化物晶胞如图所示,它由A、B方块组成。则该化合物中Fe2+、Fe3+、O2-的个数比为

您最近一年使用:0次
2024-02-13更新
|
125次组卷
|
2卷引用:宁夏银川市育才中学2023-2024学年高三上学期1月期末理科综合化学试题
解题方法
5 . 根据所学化学知识回答下列问题:
(1)基态Cr原子的价电子排布式为______ ;基态S原子电子占据最高能级的电子云轮廓图为______ 形。
(2)稳定性:
____  (填“>”或“<”)。
(填“>”或“<”)。
(3)水是生命之源,通常水加热至100℃时变为水蒸气,破坏的粒子间的相互作用包含___________ ,加热至2000℃会缓慢分解为 和
和 时破坏的粒子间的相互作用是
时破坏的粒子间的相互作用是___________ 。
(4)硼砂中阴离子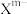 (含B、O、H三种元素)的球棍模型如图所示,则在
(含B、O、H三种元素)的球棍模型如图所示,则在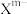 中,2号硼原子的杂化类型为
中,2号硼原子的杂化类型为______ ;4号硼原子是否参与形成配位键?_____ (填“是”或“否”)。

(5) 和过量NaF作用可生成
和过量NaF作用可生成 ,
, 的空间结构为
的空间结构为______ 。
(1)基态Cr原子的价电子排布式为
(2)稳定性:

 (填“>”或“<”)。
(填“>”或“<”)。(3)水是生命之源,通常水加热至100℃时变为水蒸气,破坏的粒子间的相互作用包含
 和
和 时破坏的粒子间的相互作用是
时破坏的粒子间的相互作用是(4)硼砂中阴离子
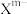 (含B、O、H三种元素)的球棍模型如图所示,则在
(含B、O、H三种元素)的球棍模型如图所示,则在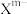 中,2号硼原子的杂化类型为
中,2号硼原子的杂化类型为
(5)
 和过量NaF作用可生成
和过量NaF作用可生成 ,
, 的空间结构为
的空间结构为
您最近一年使用:0次
6 . NaBiO3(铋酸钠,浅黄色不溶于冷水的固体)是分析化学常用试剂。工业上以辉铋矿粉[主要成分是Bi2S3,含少量SiO2、Cu2S、FeS2 等杂质]为原料制备铋酸钠的流程如下:

请回答下列问题:
(1)浸渣的主要成分___________ ;Cu在周期表中的位置是第四周期,___________ 族;基态Cu+的电子排布式是___________ 。
(2)检验“酸浸”液中是否含Fe2+,可选择K3[Fe(CN)6]溶液。能证明不存在Fe2+的实验现象是___________ 。
(3)“除铁”时需调节溶液的pH为3.7,这时溶液中的Fe3+已沉淀完全。从平衡原理解释加入CuO如何除去Fe3+___________ ;从沉淀溶解平衡角度计算Fe(OH)3的溶度积常数Ksp[Fe(OH)3]=___________
(4)已知Ksp[Cu(OH)2]=2.0×10-20,Cu2+(aq)+4NH3·H2O(aq) [Cu(NH3)4]2+(aq)+4H2O(l)的平衡常数K1=2.0×1013。Cu(OH)2(s)+4 NH3·H2O(aq)
[Cu(NH3)4]2+(aq)+4H2O(l)的平衡常数K1=2.0×1013。Cu(OH)2(s)+4 NH3·H2O(aq) [Cu(NH3)4]+(ag)+2OH-(aq)+ 4H2O(l)的平衡常数K2=
[Cu(NH3)4]+(ag)+2OH-(aq)+ 4H2O(l)的平衡常数K2=___________ 。
(5)写出“氧化”步骤对应的离子方程式:___________
(6)探究NaBiO3的性质:
结合上述实验及所学知识,在酸性条件下, 、NaBiO3、Cl2中氧化性最强的是
、NaBiO3、Cl2中氧化性最强的是___________ (填化学式),这些物质中元素基态原子中未成对电子数最多的是___________ (填元素名称)。

请回答下列问题:
(1)浸渣的主要成分
(2)检验“酸浸”液中是否含Fe2+,可选择K3[Fe(CN)6]溶液。能证明不存在Fe2+的实验现象是
(3)“除铁”时需调节溶液的pH为3.7,这时溶液中的Fe3+已沉淀完全。从平衡原理解释加入CuO如何除去Fe3+
(4)已知Ksp[Cu(OH)2]=2.0×10-20,Cu2+(aq)+4NH3·H2O(aq)
 [Cu(NH3)4]2+(aq)+4H2O(l)的平衡常数K1=2.0×1013。Cu(OH)2(s)+4 NH3·H2O(aq)
[Cu(NH3)4]2+(aq)+4H2O(l)的平衡常数K1=2.0×1013。Cu(OH)2(s)+4 NH3·H2O(aq) [Cu(NH3)4]+(ag)+2OH-(aq)+ 4H2O(l)的平衡常数K2=
[Cu(NH3)4]+(ag)+2OH-(aq)+ 4H2O(l)的平衡常数K2=(5)写出“氧化”步骤对应的离子方程式:
(6)探究NaBiO3的性质:
| 实验 | 操作 | 现象 |
| Ⅰ | 取少量NaBiO3粉末于试管中,加入浓盐酸,振荡;用镊子夹一块湿润的淀粉KI试纸放置在试管口上方 | 浅黄色固体溶解,产生黄绿色气体,试纸变蓝 |
| Ⅱ | 在稀硫酸酸化的MnSO4溶液中加入NaBiO3粉末,振荡 | 无色溶液变紫红色溶液 |
 、NaBiO3、Cl2中氧化性最强的是
、NaBiO3、Cl2中氧化性最强的是
您最近一年使用:0次
名校
解题方法
7 . 下列表示物质结构的化学用语或模型正确的是
A.Se的原子结构示意图: |
B.基态铬原子的价电子排布式: |
C.基态氧原子的轨道表示式: |
| D.Fe3+的价电子排布式:3d5 |
您最近一年使用:0次
名校
8 . 下表列出了九种元素在元素周期表中的位置。
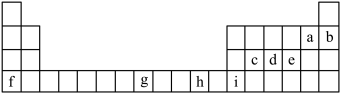
(1)这九种元素电负性最大的是_______ ,第一电离能最小的元素是_______ (均用元素符号填空)。
(2)这九种元素中最外层电子排布为4s1的元素为_______ (用元素符号填空)。
(3)c、d、e三种元素第一电离能由大到小的顺序是_______ ,电负性由大到小的顺序是_______ (均用元素符号填空)。
(4)写出g元素原子的价层电子轨道表达式_______ ,i元素原子基态电子排布式_______ 。

(1)这九种元素电负性最大的是
(2)这九种元素中最外层电子排布为4s1的元素为
(3)c、d、e三种元素第一电离能由大到小的顺序是
(4)写出g元素原子的价层电子轨道表达式
您最近一年使用:0次
9 . 下列有关基态微粒的电子排布式正确的是
A. | B.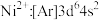 |
C.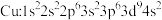 | D.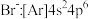 |
您最近一年使用:0次
2023-12-26更新
|
255次组卷
|
5卷引用:宁夏开元学校2023-2024学年高二上学期期末考试化学试题
名校
解题方法
10 . 下列化学用语表示不正确的是
A.Mg2+的结构示意图: |
B.基态氧原子的轨道表示式: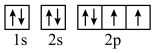 |
| C.S2-的电子排布式:1s22s22p63s23p6 |
| D.基态铬原子(24Cr)的价层电子排布式:3d44s2 |
您最近一年使用:0次
2023-12-25更新
|
301次组卷
|
2卷引用:宁夏开元学校2023-2024学年高二上学期期末考试化学试题



