名校
1 . C、Be、Cl、Fe等元素及其化合物有重要的应用。
(1)查表得知,Be的电负性是1.5,Cl的电负性是3.0,则BeCl2应为________ (填离子或共价)化合物;根据铍元素和铝元素在周期表中的位置,推测BeCl2应与_________ (填MgCl2或AlCl3)化学性质更相似。
(2)上述四种元素的原子中,未成对电子数最多的元素是_________________ 。
(3)①试根据原子核外电子排布所遵循的原理解释Fe2+具有较的强还原性,易被氧化为Fe3+的原因___________________ 。②当然Fe3+也有氧化性,在印刷行业中就用氯化铁溶液腐蚀铜板,写出离子方程式___________________ 。
(4)一定条件下,C元素可形成多种晶体。下图1是其中某种晶体的一个晶胞,该晶胞中含有________ 个C原子。
(5)下图2为金属铁某种晶体的晶胞结构,已知铁的摩尔质量是56g•mol-1,该晶体的密度为ag•cm-3,NA为阿伏加德罗常数的值,则该晶胞的体积为_________ cm3。

(1)查表得知,Be的电负性是1.5,Cl的电负性是3.0,则BeCl2应为
(2)上述四种元素的原子中,未成对电子数最多的元素是
(3)①试根据原子核外电子排布所遵循的原理解释Fe2+具有较的强还原性,易被氧化为Fe3+的原因
(4)一定条件下,C元素可形成多种晶体。下图1是其中某种晶体的一个晶胞,该晶胞中含有
(5)下图2为金属铁某种晶体的晶胞结构,已知铁的摩尔质量是56g•mol-1,该晶体的密度为ag•cm-3,NA为阿伏加德罗常数的值,则该晶胞的体积为

您最近一年使用:0次
2016-12-09更新
|
299次组卷
|
2卷引用:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷
名校
解题方法
2 . 碘酸钾(KIO3)是重要的食品添加剂。可用Cl2氧化I2制取HIO3,再用KOH中和HIO3制取KIO3。其中,制取碘酸(HIO3)的实验装置示意图和有关资料如下:

回答下列问题:
(1)装置A中发生反应的化学方程式为___________________________________ 。
(2)装置B的名称为_____________ ,I2和Cl2在水中的溶解度小于在CCl4中的溶解度,原因是___________________________________________________________ 。
(3)KIO3晶体中,基态 K 原子核外电子占据的最高能层的符号是________ ,占据该能层电子的电子云轮廓图形状为__________ ;碘元素在周期表中的位置为___________ ,IO3-中心原子I的杂化类型为_____________ 。
(4)HIO3分子中三种元素电负性由大到小的顺序为___________ ,其电离方程式为______ 。

| HIO3 | ①白色固体,能溶于水,难溶于四氯化碳 ②Ka=0.169mol/L |
| KIO3 | ①白色固体,能溶于水,难溶于乙醇 ②碱性条件下易发生反应: ClO-+IO3-=IO4-+Cl- |
(1)装置A中发生反应的化学方程式为
(2)装置B的名称为
(3)KIO3晶体中,基态 K 原子核外电子占据的最高能层的符号是
(4)HIO3分子中三种元素电负性由大到小的顺序为
您最近一年使用:0次
9-10高二下·江苏泰州·期末
名校
解题方法
3 . 对Na、Mg、Al的有关性质的叙述正确的是:
| A.碱性:NaOH< Mg(OH)2< Al(OH)3 | B.第一电离能:Na< Mg <Al |
| C.还原性:Na> Mg >Al | D.电负性:Na> Mg >Al |
您最近一年使用:0次
2020-11-12更新
|
573次组卷
|
63卷引用:2015-2016学年福建省泉州市晋江市平山中学高二上期末化学试卷
2015-2016学年福建省泉州市晋江市平山中学高二上期末化学试卷福建省福州市八县(市)协作校2016-2017学年高二下学期期末考试化学试题福建省福州市八县协作校2016-2017学年高二下学期期末化学试题福建省福州三中2017-2018学年高二上学期期末考试化学试题福建省泉州市泉港区第一中学2018-2019学年高二下学期期末考试化学试题福建省永春美岭中学2021-2022学年高二下学期期中测试化学试题(已下线)09—10年泰州中学高二下学期期末考试化学卷(已下线)2013-2014宁夏银川一中高二下学期期末考试化学试卷2014-2015学年宁夏宁大附中高二上学期期中考试化学试卷2014-2015宁夏银川市唐徕回民中学高二下学期3月月考化学试卷2014-2015吉林省吉林市第五十五中学高二下学期期中考试化学试卷2014-2015学年陕西省宝鸡中学高二下学期期末化学试卷A2014-2015学年吉林省汪清县第六中学高二下学期期末考试化学试卷2015-2016学年宁夏六盘山中学高二下第一次月考化学卷2015-2016学年山西太原五中高二下3月第二次周练化学卷2015-2016学年陕西西藏民族学院附中高二4月月考化学卷2015-2016学年山东省淄博市高青一中高二4月月考化学试卷2015-2016学年山西省右玉一中高二5月月考化学试卷2015-2016学年吉林东北师大附属实验高二下期末化学试卷2015-2016学年吉林梅河口五中高二下期末化学试卷2015-2016吉林东北师大附属实验学校净月实验学校高二下期末化学卷2015-2016学年山西省朔州市右玉一中高二下5月月考化学试卷2016-2017学年四川省阆中中学高二上教学质检化学试卷2016-2017学年宁夏吴忠中学高二下学期第一次月考化学试卷2016-2017学年宁夏育才中学孔德校区高二下学期第一次(3月)月考化学试卷安徽省蚌埠市第二中学2016-2017学年高二下学期期中考试化学试题河北省馆陶县第一中学2016-2017学年高二下学期期中考试化学试题湖北省孝感市七校教学联盟2016-2017学年高二下学期期末考试化学试题新疆呼图壁县第一中学2016-2017学年高二下学期期末考试化学试题河北省深州中学2016-2017学年高二下学期期末考试化学试题内蒙古包头市第三十三中学2016-2017学年高二下学期期末考试化学试题吉林省辽源五中2017-2018学年高二下学期第一次月考化学试题云南省玉溪市易门中学2017-2018学年高二上学期期中考试化学试题云南省玉溪市通海三中2018-2019学年高二上学期10月考试化学试题甘肃省玉门市第一中学2018-2019学年高二上学期期中考试化学试题山东省泰安市宁阳一中2018-2019学年高二上学期阶段性考试三(12月)化学试题贵州省剑河县第二高级中学2018-2019学年高二上学期12月份考试化学试题黑龙江省鸡西市鸡东县第二中学2018-2019学年高二5月月考化学试题新疆兵团八师一四三团一中2018-2019学年高二下学期期中考试化学试题新疆石河子第二中学2018-2019学年高二下学期第一次月考化学试题黑龙江省哈尔滨市第三中学校2019-2020学年高二上学期期末考试化学试题黑龙江省哈尔滨市第三中学2019-2020学年高二上学期第一模块(期末)考试化学试题吉林省延边市长白山第一高级中学2019-2020学年高二下学期验收考试化学试卷吉林省长春市第二十九中学2019-2020学年高二上学期期末考试化学试题安徽省安庆市太湖县太湖中学2019-2020学年高二下学期3月线上考试化学试题新疆乌鲁木齐市第四中学2019-2020学年高二下学期期末考试化学试题广西防城港市防城中学2019-2020学年高二下学期期中考试化学试题四川省平昌县驷马中学2020-2021学年高二上学期九月月考化学试题江苏省东台创新高级中学2019-2020学年高二下学期4月份月检测化学试题山东省淄博市般阳中学2020-2021学年高二上学期期中考试化学试题四川省乐山十校2020-2021学年高二上学期半期联考化学试题宁夏青铜峡市高级中学2020-2021学年高二下学期第一次月考化学试题河南省宏力学校2018-2019学年高二下学期期中考试化学试题内蒙古集宁新世纪中学2020-2021学年高二下学期期末考试化学试题广西蒙山县第一中学2018-2019学年高二下学期第二次月考化学试题新疆博尔塔拉蒙古自治州蒙古中学2020-2021学年高二下学期期中考试化学试题 四川省绵阳第一中学2022-2023学年高二上学期9月教学质量监测理科化学试题新疆乌鲁木齐市第101中学2021-2022学年高二下学期期末考试化学试题四川省乐山市沫若中学2022-2023学年高二上学期第一次月考化学试题云南省广南县二中2021-2022年学年高二下学期开学考试化学试题河南省焦作市2022-2023学年第四中学高二下学期3月月考 化学试卷新疆阿克苏市实验中学2022-2023学年高二下学期第一次月考化学试题2020届高三化学二轮物质结构题型专攻——原子结构与性质【基础专练】
名校
解题方法
4 . 维生素C的结构简式如图所示,下列关于维生素C的说法错误的是
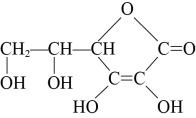

A.分子式为 |
| B.其分子中含有2种官能团 |
| C.能使酸性高锰酸钾溶液褪色,故维生素C具有还原性 |
D.维生素C分子中元素电负性大小: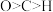 |
您最近一年使用:0次
5 . 日光灯中用到的某种荧光粉的主要成分为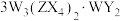 。已知:X、Y、Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对电子数之比为2∶1∶3。下列说法正确的是
。已知:X、Y、Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对电子数之比为2∶1∶3。下列说法正确的是
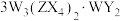 。已知:X、Y、Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对电子数之比为2∶1∶3。下列说法正确的是
。已知:X、Y、Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对电子数之比为2∶1∶3。下列说法正确的是| A.电负性:X>Y>Z>W |
| B.原子半径:X<Y<Z |
| C.Y和W的单质都能与水反应生成气体 |
| D.Z元素最高价氧化物对应的水化物具有强氧化性 |
您最近一年使用:0次
解题方法
6 . W、X、Y、Z是原子序数依次增大的短周期主族元素,原子序数总和为25,由这四种元素形成的某化合物的结构如图所示。下列说法错误的是


A.电负性大小: |
| B.该化合物具有强氧化性,可用于消毒杀菌 |
| C.该化合物含离子键、共价键、配位键 |
| D.该化合物中所有原子最外层均满足8个电子稳定结构 |
您最近一年使用:0次
解题方法
7 . 用“>”、“<”、“=”填空
(1)第一电离能:P_______ S;
(2)酸性:H3PO4_______ H2SO4;
(3)稳定性:H2O_______ H2S
(4)微粒半径:S_______ S2-
(5)碱性:KOH_______ NaOH
(6)元素的电负性:S_______ Cl。
(1)第一电离能:P
(2)酸性:H3PO4
(3)稳定性:H2O
(4)微粒半径:S
(5)碱性:KOH
(6)元素的电负性:S
您最近一年使用:0次
名校
解题方法
8 . 下列叙述正确的是
| A.某元素原子核外电子总数是最外层电子数的5倍,则其最高正价为+7 |
| B.钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能 |
| C.通过比较氯的化合价即可确定氧化性:高氯酸>次氯酸 |
| D.元素电负性大的原子第一电离能也一定大 |
您最近一年使用:0次
名校
解题方法
9 . 短周期主族元素X、Y、Z、W的原子序数依次增加,K、L、M均是由这些元素组成的氧化物,甲、乙分别是元素Y、W的单质,甲是常见的固体,乙是常见的气体。K是红棕色气体,丙的浓溶液具有强氧化性,上述物质的转化关系如图所示。下列说法不正确的是( )


| A.Y、Z、W三种元素电负性:W>Z>Y |
| B.Y、Z、W三种元素第一电离能:Z>W>Y |
| C.L的沸点一定比X、Y组成的化合物沸点高 |
| D.由X、Y、Z、W构成的化合物中只能含有共价键 |
您最近一年使用:0次
2020-06-24更新
|
556次组卷
|
6卷引用:福建省建瓯市芝华中学2019-2020学年高二下学期居家学习检测化学试题
名校
解题方法
10 . 物质世界的神奇莫测,常常超乎人们的想象。掌握晶体的结构与性质之间的关系,也许能使你想象的翅膀变得更有力。请回答下列问题:
(1) 是目前市场上流行的补锌剂。写出
是目前市场上流行的补锌剂。写出 基态电子排布式:
基态电子排布式:___________ 。
(2)已知高温下 比
比 更稳定,试从铜原子核外电子变化角度解释其原因:
更稳定,试从铜原子核外电子变化角度解释其原因:___________ 。
(3)镍能与类卤素 反应生成
反应生成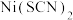 。
。 中硫原子的杂化方式是
中硫原子的杂化方式是___________ , 键和
键和 键数目之比为
键数目之比为___________ ;类卤素 对应的酸有两种,理论上硫氰酸(HSCN)的沸点低于异硫氰酸(HNCS)的沸点,其原因是
对应的酸有两种,理论上硫氰酸(HSCN)的沸点低于异硫氰酸(HNCS)的沸点,其原因是___________ 。
(4)氮化硼(BN)晶体存在两种结构,六方氮化硼的结构与石墨类似,可做润滑剂;立方氮化硼的结构与金刚石类似,可作研磨剂。六方氮化硼的晶体类型为___________ 。
(5) 中所含元素的电负性由大到小的顺序为
中所含元素的电负性由大到小的顺序为___________ ,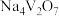 晶体中存在的相互作用有
晶体中存在的相互作用有___________ (填标号)。
a.离子键 B.共价键 C.金属键 D.氢键 E.范德华力
(6) 的结构如图所示,已知键角
的结构如图所示,已知键角 为
为 ,
, 为
为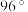 ,则
,则 的原因主要是
的原因主要是___________ 。

(7)酸性:
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(8)已知 可形成配位数为6,颜色不同的两种配合物晶体,一种为紫色,另一为绿色。两种晶体的组成皆为
可形成配位数为6,颜色不同的两种配合物晶体,一种为紫色,另一为绿色。两种晶体的组成皆为 。为测定这两种晶体的化学式,设计了如下实验:
。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入 溶液,均产生白色沉淀;
溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现绿色晶体的水溶液得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的 。绿色晶体配合物的化学式为
。绿色晶体配合物的化学式为___________ 。
(9) 的晶胞如图所示。
的晶胞如图所示。
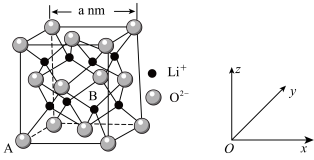
①已知A的坐标为(0,0,0),B的坐标为___________ 。
②设阿伏加德罗常数的值为 ,则
,则 晶体的密度为
晶体的密度为___________  (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
(1)
 是目前市场上流行的补锌剂。写出
是目前市场上流行的补锌剂。写出 基态电子排布式:
基态电子排布式:(2)已知高温下
 比
比 更稳定,试从铜原子核外电子变化角度解释其原因:
更稳定,试从铜原子核外电子变化角度解释其原因:(3)镍能与类卤素
 反应生成
反应生成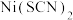 。
。 中硫原子的杂化方式是
中硫原子的杂化方式是 键和
键和 键数目之比为
键数目之比为 对应的酸有两种,理论上硫氰酸(HSCN)的沸点低于异硫氰酸(HNCS)的沸点,其原因是
对应的酸有两种,理论上硫氰酸(HSCN)的沸点低于异硫氰酸(HNCS)的沸点,其原因是(4)氮化硼(BN)晶体存在两种结构,六方氮化硼的结构与石墨类似,可做润滑剂;立方氮化硼的结构与金刚石类似,可作研磨剂。六方氮化硼的晶体类型为
(5)
 中所含元素的电负性由大到小的顺序为
中所含元素的电负性由大到小的顺序为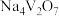 晶体中存在的相互作用有
晶体中存在的相互作用有a.离子键 B.共价键 C.金属键 D.氢键 E.范德华力
(6)
 的结构如图所示,已知键角
的结构如图所示,已知键角 为
为 ,
, 为
为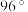 ,则
,则 的原因主要是
的原因主要是
(7)酸性:

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(8)已知
 可形成配位数为6,颜色不同的两种配合物晶体,一种为紫色,另一为绿色。两种晶体的组成皆为
可形成配位数为6,颜色不同的两种配合物晶体,一种为紫色,另一为绿色。两种晶体的组成皆为 。为测定这两种晶体的化学式,设计了如下实验:
。为测定这两种晶体的化学式,设计了如下实验:a.分别取等质量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入
 溶液,均产生白色沉淀;
溶液,均产生白色沉淀;c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现绿色晶体的水溶液得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的
 。绿色晶体配合物的化学式为
。绿色晶体配合物的化学式为(9)
 的晶胞如图所示。
的晶胞如图所示。
①已知A的坐标为(0,0,0),B的坐标为
②设阿伏加德罗常数的值为
 ,则
,则 晶体的密度为
晶体的密度为 (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次



