1 . 物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
| 选项 | 性质差异 | 结构因素 |
| A | 正戊烷的沸点高于新戊烷 | 正戊烷分子极性大于新戊烷,范德华力强 |
| B | 金刚石的熔点高于 | 金刚石为共价晶体, 为分子晶体 为分子晶体 |
| C | 三氟乙酸的 大于三氯乙酸的 大于三氯乙酸的 |  电负性大于 电负性大于 ,三氟乙酸 ,三氟乙酸 键极性强 键极性强 |
| D |  在水中的溶解度大于CO 在水中的溶解度大于CO |  为非极性分子, 为非极性分子, 为极性分子 为极性分子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . Zn、Fe、Cu、Cr等过渡金属的原子或离子易通过配位键形成配合物或配离子。回答下列问题:
I.一种比率光声探针M与 配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:
配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:

(1)H、C、N、F四种元素电负性由小到大的顺序为_______ , 中键角F-B-F
中键角F-B-F_______ M中键角F-B-F(填“>”、“<”或“=”)。
(2)As与N为同一主族元素,有机酸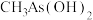 的沸点比
的沸点比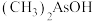 高的原因是
高的原因是_______ 。
(3)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列物质中,属于顺磁性物质的是_______。
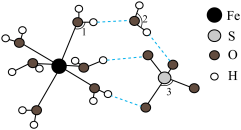
Ⅱ. 的结构如下图所示。
的结构如下图所示。
(4)与Fe最外层电子数相同且同周期的元素有_______ 种。
(5)图示 结构中键角1、2、3由大到小的顺序是
结构中键角1、2、3由大到小的顺序是_______ (填序号)。
Ⅲ.一种立方钙钛矿型晶体 有两种晶胞结构,其俯视图如下(重叠处仅画出大的微粒),La的配位数均是12。
有两种晶胞结构,其俯视图如下(重叠处仅画出大的微粒),La的配位数均是12。
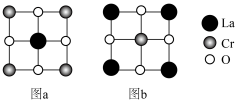
(6)图a的晶胞参数为xpm,则O与O的最小核间距为_______ pm;图b晶胞中O的位置为_______ (填“体心”“顶点”“面心”“棱心”)。
(7)晶胞经掺杂后能提高红外辐射效率。由图a晶胞堆叠形成的2×2×2超晶胞中一个La原子被Sr代替,则掺杂后晶体化学式为_______ 。
I.一种比率光声探针M与
 配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:
配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:
(1)H、C、N、F四种元素电负性由小到大的顺序为
 中键角F-B-F
中键角F-B-F(2)As与N为同一主族元素,有机酸
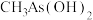 的沸点比
的沸点比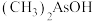 高的原因是
高的原因是(3)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列物质中,属于顺磁性物质的是_______。
A. | B. |
C. | D.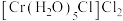 |
Ⅱ.
 的结构如下图所示。
的结构如下图所示。
(4)与Fe最外层电子数相同且同周期的元素有
(5)图示
 结构中键角1、2、3由大到小的顺序是
结构中键角1、2、3由大到小的顺序是Ⅲ.一种立方钙钛矿型晶体
 有两种晶胞结构,其俯视图如下(重叠处仅画出大的微粒),La的配位数均是12。
有两种晶胞结构,其俯视图如下(重叠处仅画出大的微粒),La的配位数均是12。
(6)图a的晶胞参数为xpm,则O与O的最小核间距为
(7)晶胞经掺杂后能提高红外辐射效率。由图a晶胞堆叠形成的2×2×2超晶胞中一个La原子被Sr代替,则掺杂后晶体化学式为
您最近一年使用:0次
名校
3 . 过渡元素镍(Ni)、铬(Cr)都是重要的合金元素,他们的配合物在科技生活中都有很重要的应用,例如我国科学家合成铬的化合物通过烷基铝和[ph3C]+[B(C6F5)4]-活化后,对乙烯聚合表现出较好的催化活性。合成铬的化合物过程中的一步反应为:

回答下列问题:
(1)Cr3+价电子核外电子排布式为______ ,分子甲中除铬外其他元素的电负性由大到小依次为______ (填元素符号)。
(2)一定条件下环戊二烯 可转化为
可转化为 ,在这个过程中C原子的杂化方式变化为由sp3变为
,在这个过程中C原子的杂化方式变化为由sp3变为_____ , 中大π键可表示为
中大π键可表示为_____ 。
(3)化合物丙中1、2、3、4处的化学键是配位键的是_______ 。
a.只有2 b.2、3、4 c.全部都是
(4)AsCl3也可以与铬离子形成配合物,当氯原子被烷基取代后,配位能力增强,其原因是__________ 。
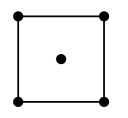
(5)水在合成铬的化合物的过程中作溶剂。研究表明水能凝结成13种类型的结晶体。重冰(密度比水大)属于立方晶系,其立方晶胞沿x、y或z轴的投影图如图所示,晶体中H2O的配位数为_________ 。
(6)一种由镍、氟、钾三种元素组成的化合物晶胞结构如图所示,原子A、B之间的距离是_________ (用字母a、b、c表示),晶胞中镍的分数坐标有____ 种。


回答下列问题:
(1)Cr3+价电子核外电子排布式为
(2)一定条件下环戊二烯
 可转化为
可转化为 ,在这个过程中C原子的杂化方式变化为由sp3变为
,在这个过程中C原子的杂化方式变化为由sp3变为 中大π键可表示为
中大π键可表示为(3)化合物丙中1、2、3、4处的化学键是配位键的是
a.只有2 b.2、3、4 c.全部都是
(4)AsCl3也可以与铬离子形成配合物,当氯原子被烷基取代后,配位能力增强,其原因是
(5)水在合成铬的化合物的过程中作溶剂。研究表明水能凝结成13种类型的结晶体。重冰(密度比水大)属于立方晶系,其立方晶胞沿x、y或z轴的投影图如图所示,晶体中H2O的配位数为

(6)一种由镍、氟、钾三种元素组成的化合物晶胞结构如图所示,原子A、B之间的距离是

您最近一年使用:0次
解题方法
4 . 我国化学家研究发现,十八胺在较高温度下具有一定的还原性,由于不同的金属盐从十八胺中获得电子的能力不同,在十八胺体系中反应可以得到不同的产物:当以两种非贵金属盐为原料时得到混合金属氧化物(如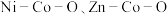 等),以
等),以 和一种非贵金属盐为原料时得到金属与金属氧化物异质结构(如
和一种非贵金属盐为原料时得到金属与金属氧化物异质结构(如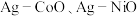 等),除
等),除 之外的其他贵金属盐和一种非贵金属盐为原料时得到合金或金属间化合物(如
之外的其他贵金属盐和一种非贵金属盐为原料时得到合金或金属间化合物(如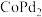 等)。
等)。
回答下列问题:
(1)十八胺中含有氮元素,含氮元素的三种离子 的键角由大到小的顺序是
的键角由大到小的顺序是___________ 。
(2) 与
与 相比,第二电离能与第一电离能差值更大的是
相比,第二电离能与第一电离能差值更大的是___________ 。
(3)以 和钴盐为原料时得到的产物
和钴盐为原料时得到的产物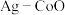 而非
而非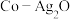 的原因是
的原因是___________ 。
(4)推测 盐和一种非贵金属盐混合后在十八胺体系中发生反应所得产物类别为
盐和一种非贵金属盐混合后在十八胺体系中发生反应所得产物类别为___________ 。
(5)一种含钴的离子结构如图所示: 的价电子轨道表示式是
的价电子轨道表示式是___________ 。已知磁矩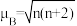 (n表示未成对电子数),则
(n表示未成对电子数),则 的磁矩
的磁矩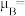
___________ 。
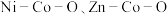 等),以
等),以 和一种非贵金属盐为原料时得到金属与金属氧化物异质结构(如
和一种非贵金属盐为原料时得到金属与金属氧化物异质结构(如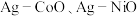 等),除
等),除 之外的其他贵金属盐和一种非贵金属盐为原料时得到合金或金属间化合物(如
之外的其他贵金属盐和一种非贵金属盐为原料时得到合金或金属间化合物(如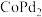 等)。
等)。
| 元素 |  |  |  |  |  |  |  |
| 电负性(鲍林标度) | 1.6 | 1.8 | 1.8 | 1.9 | 2.2 | 2.2 | 2.4 |
(1)十八胺中含有氮元素,含氮元素的三种离子
 的键角由大到小的顺序是
的键角由大到小的顺序是(2)
 与
与 相比,第二电离能与第一电离能差值更大的是
相比,第二电离能与第一电离能差值更大的是(3)以
 和钴盐为原料时得到的产物
和钴盐为原料时得到的产物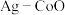 而非
而非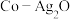 的原因是
的原因是(4)推测
 盐和一种非贵金属盐混合后在十八胺体系中发生反应所得产物类别为
盐和一种非贵金属盐混合后在十八胺体系中发生反应所得产物类别为(5)一种含钴的离子结构如图所示:
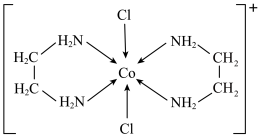
 的价电子轨道表示式是
的价电子轨道表示式是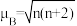 (n表示未成对电子数),则
(n表示未成对电子数),则 的磁矩
的磁矩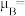
您最近一年使用:0次
解题方法
5 . Fe为重要的元素,与C、N、O等组成的化合物有广泛的用途。回答下列问题:
(1)甘氨酸亚铁络合物[ ]是一种新型的铁营养强化剂。
]是一种新型的铁营养强化剂。
① 中含有的第二周期元素的第一电离能由大到小的顺序为
中含有的第二周期元素的第一电离能由大到小的顺序为___________ 。
②甘氨酸( )的沸点比相近相对分子质量的烷烃高很多,原因是
)的沸点比相近相对分子质量的烷烃高很多,原因是___________ 。
II.砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池等,回答下列问题:
(2)基态Ga原子的核外电子排布式为[Ar]___________ 。
(3)根据元素周期律,元素的电负性Ga___________ (填“大于”或“小于”)As。
(4)杀虫剂Na3AsO4中As原子采取___________ 杂化。
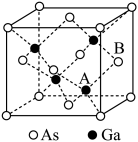
(5)共价晶体GaAs的晶胞参数a=xpm,它的晶胞结构如图所示,该晶体的密度为___________ (列出计算式,阿伏加德罗常数的值用NA表示) 。
。
(1)甘氨酸亚铁络合物[
 ]是一种新型的铁营养强化剂。
]是一种新型的铁营养强化剂。①
 中含有的第二周期元素的第一电离能由大到小的顺序为
中含有的第二周期元素的第一电离能由大到小的顺序为②甘氨酸(
 )的沸点比相近相对分子质量的烷烃高很多,原因是
)的沸点比相近相对分子质量的烷烃高很多,原因是II.砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池等,回答下列问题:
(2)基态Ga原子的核外电子排布式为[Ar]
(3)根据元素周期律,元素的电负性Ga
(4)杀虫剂Na3AsO4中As原子采取
(5)共价晶体GaAs的晶胞参数a=xpm,它的晶胞结构如图所示,该晶体的密度为
 。
。
您最近一年使用:0次
名校
解题方法
6 . X、Y、Z、Q是原子序数依次增大的前四周期元素,其中X是宇宙中含量最多的元素;Y元素基态原子的价层电子排布是 ;Z、Q元素原子的最外层均只有1个电子,Z元素原子中只有两种形状的电子云,Q元素基态原子内层轨道均排满电子。下列说法正确的是
;Z、Q元素原子的最外层均只有1个电子,Z元素原子中只有两种形状的电子云,Q元素基态原子内层轨道均排满电子。下列说法正确的是
 ;Z、Q元素原子的最外层均只有1个电子,Z元素原子中只有两种形状的电子云,Q元素基态原子内层轨道均排满电子。下列说法正确的是
;Z、Q元素原子的最外层均只有1个电子,Z元素原子中只有两种形状的电子云,Q元素基态原子内层轨道均排满电子。下列说法正确的是A.电负性: | B.ZX属于共价化合物 |
C. 的阴阳离子数之比为1:1 的阴阳离子数之比为1:1 | D.Q元素位于元素周期表的ds区 |
您最近一年使用:0次
2023-05-05更新
|
590次组卷
|
3卷引用:山东省烟台市龙口某校2023-2024学年高二上学期12月月考化学试题
山东省烟台市龙口某校2023-2024学年高二上学期12月月考化学试题(已下线)第06练 元素“位—构—性”的综合推断 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)福建省三明市2022-2023学年普通高中高三下学期5月份质量检测化学试题
名校
解题方法
7 . 在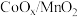 催化下醇的氧化氰化反应如图所示。下列叙述正确的是
催化下醇的氧化氰化反应如图所示。下列叙述正确的是

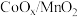 催化下醇的氧化氰化反应如图所示。下列叙述正确的是
催化下醇的氧化氰化反应如图所示。下列叙述正确的是
A.熔点: | B.键角: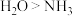 |
C.I和II分子中 键数目相同 键数目相同 | D.II含有的元素中 的电负性最大 的电负性最大 |
您最近一年使用:0次
2023-03-16更新
|
2417次组卷
|
4卷引用:山东省菏泽市曹县第一中学2022-2023学年高二下学期3月月考化学试题
名校
解题方法
8 . 硒化锌是一种重要的半导体材料;其晶胞结构如图甲所示,已知晶胞参数为pnm,乙图为晶胞的俯视图,下列说法正确的是
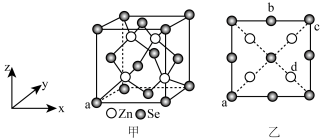
| A.晶胞中硒原子的配位数为12 |
B.晶胞中d点原子分数坐标为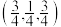 |
C.相邻两个Zn原子的最短距离为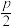 nm nm |
| D.电负性:Zn>Se |
您最近一年使用:0次
2023-03-03更新
|
1858次组卷
|
11卷引用:山东省德州市第一中学2022-2023学年高二下学期3月月考化学试题
山东省德州市第一中学2022-2023学年高二下学期3月月考化学试题山东省临沂市第二十四中学2023-2024学年高二下学期3月学科素养水平监测化学试题山东省济宁市2023届高三一模考试(3月)化学试题河南省郑州市六校联盟2022-2023学年高二下学期4月期中考试化学试题福建省龙岩市连城县第一中学2022-2023学年高二下学期5月月考化学试题河南省驻马店市环际大联考2022-2023学年高二下学期4月期中考试化学试题(已下线)热点08 金属晶体和离子晶体山东省烟台市第一中学2023-2024学年高三下学期3月月考化学试题(已下线)湖北省七市(州)2023届高三3月联合统一调研测试化学试题变式题(选择题11-15)(已下线)专题十 晶胞示意图(练)河北省张家口市宣化第一中学2023届高三模拟试题(三)化学试题
9 . 回答下列问题:
(1)化合物III也是一种汞解毒剂。化合物IV是一种强酸。下列说法正确的有_____ 。

A.在I中S原子采取sp3杂化
B.在II中S元素的电负性最大
C.在III中C-C-C键角是180°
D.在III中存在离子键与共价键
E.在IV中硫氧键的键能均相等
(2)汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。化合物I与化合物III相比,水溶性较好的是_____ 。
(3)NH3、PH3、AsH3分子的键角分别为107.3°、93.3°、91.8°,其键角逐渐减小的原因是____ 。
(4) 中含有各元素的电负性由小到大的顺序为
中含有各元素的电负性由小到大的顺序为____ ;该物质中,含有σ键和π键数目之比为____ 。
(5)在CO分子中每个原子均为8电子稳定结构,则C与O之间形成_____ 个σ键____ 个π键,在这些化学键中,O原子共提供了____ 个电子。
(6)乙腈(CH3CN)分子中碳原子的杂化类型有____ ,与N同周期的主族元素中,第一电离能大于N的有_____ 种,写出一种与N 互为等电子体的分子的化学式
互为等电子体的分子的化学式_____ ,NO 离子的立体构型是
离子的立体构型是____ 。
(7)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据列于表:
锰元素位于第四周期第VIIB族。请写出基态Mn2+的价电子排布式:_____ ,比较两元素的I2、I3可知,气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难,对此你的解释是_____ 。
(1)化合物III也是一种汞解毒剂。化合物IV是一种强酸。下列说法正确的有

A.在I中S原子采取sp3杂化
B.在II中S元素的电负性最大
C.在III中C-C-C键角是180°
D.在III中存在离子键与共价键
E.在IV中硫氧键的键能均相等
(2)汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。化合物I与化合物III相比,水溶性较好的是
(3)NH3、PH3、AsH3分子的键角分别为107.3°、93.3°、91.8°,其键角逐渐减小的原因是
(4)
 中含有各元素的电负性由小到大的顺序为
中含有各元素的电负性由小到大的顺序为(5)在CO分子中每个原子均为8电子稳定结构,则C与O之间形成
(6)乙腈(CH3CN)分子中碳原子的杂化类型有
 互为等电子体的分子的化学式
互为等电子体的分子的化学式 离子的立体构型是
离子的立体构型是(7)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据列于表:
| 元素 | Mn | Fe | |
| 电离能/kJ•mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
您最近一年使用:0次
名校
解题方法
10 . C、N、P、Si是重要的非金属元素,在生产、生活中有重要应用。回答下列问题:
(1)下列氮原子的电子排布图表示的状态中,能量最高的是_______(填序号)。
(2)原子中运动的电子有两种相反的自旋状态,一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态Si原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态Si原子,其价电子自旋磁量子数的代数和为_______ 。
(3) 中共用电子对偏向C,
中共用电子对偏向C, 中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为
中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为_______ 。
(4) 分子的中心原子的价层电子对数为
分子的中心原子的价层电子对数为_______ ,分子的立体构型为三角双锥形, 属于
属于_______ 分子(填“极性”或“非极性”),其中心原子杂化类型为_______ (填序号)。
A. B.
B. C.
C. D.
D.
(5)试用下表中的键能数据解释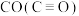 比
比 相对活泼的原因:
相对活泼的原因:_______ 。
(1)下列氮原子的电子排布图表示的状态中,能量最高的是_______(填序号)。
A.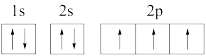 | B.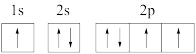 |
C.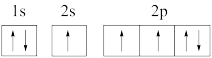 | D.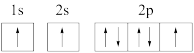 |
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态Si原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态Si原子,其价电子自旋磁量子数的代数和为(3)
 中共用电子对偏向C,
中共用电子对偏向C, 中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为
中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为(4)
 分子的中心原子的价层电子对数为
分子的中心原子的价层电子对数为 属于
属于A.
 B.
B. C.
C. D.
D.
(5)试用下表中的键能数据解释
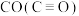 比
比 相对活泼的原因:
相对活泼的原因:| C—O | C=O |  | |
键能 | 357.7 | 798.9 | 1071.9 |
| N—N | N=N |  | |
键能 | 154.8 | 418.4 | 941.7 |
您最近一年使用:0次
2022-08-21更新
|
352次组卷
|
2卷引用:山东省潍坊市2021-2022学年高二上学期期末考试化学试题



