1 . 最近科研人员发现,用[Ni(cyclam)]2+(结构如图a)作电催化剂、二茂铁(结构如图c)作为牺牲电子供体,NH4PF6作为电解质和质子供体,CH3CN作溶剂,可实现有效催化还原CO2。
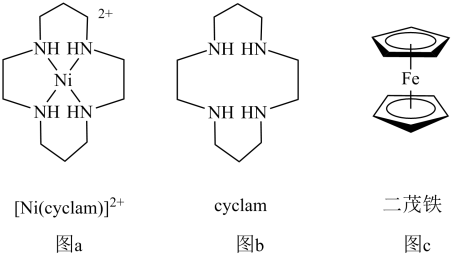
回答下列问题:
(1)基态Ni原子转化为基态Ni2+失去_______ 轨道的电子;基态Fe原子核外电子排布式为_______ 。
(2)NH4PF6中NH 空间构型为
空间构型为_______ ;N、P、F的电负性由大到小的顺序为_______ 。
(3)CH3CN分子中碳原子杂化方式为_______ 。
(4)已知3个及以上原子构成的离子团或分子中,原子有彼此平行的未参与杂化的p轨道电子,连贯重叠在一起构成π型化学键,又称为大π键,可用符号 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数,如苯中的大π键可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数,如苯中的大π键可表示为 。二茂铁[(C5H5)2Fe]中五元环的大π键可表示为
。二茂铁[(C5H5)2Fe]中五元环的大π键可表示为_______ 。
(5)[Ni (cyclam)]2+可由某些镍的化合物与cyclam 反应制得。[Ni(cyclam)]2+中,Ni2+的配位数为_______ ;cyclam可溶于水,而环十四烷不溶于水,其原因是_______ 。
(6)某镍、砷晶体结构如图所示。该晶体的密度为_______ g·cm-3(列出计算式即可)。
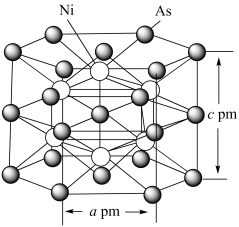

回答下列问题:
(1)基态Ni原子转化为基态Ni2+失去
(2)NH4PF6中NH
 空间构型为
空间构型为(3)CH3CN分子中碳原子杂化方式为
(4)已知3个及以上原子构成的离子团或分子中,原子有彼此平行的未参与杂化的p轨道电子,连贯重叠在一起构成π型化学键,又称为大π键,可用符号
 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数,如苯中的大π键可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数,如苯中的大π键可表示为 。二茂铁[(C5H5)2Fe]中五元环的大π键可表示为
。二茂铁[(C5H5)2Fe]中五元环的大π键可表示为(5)[Ni (cyclam)]2+可由某些镍的化合物与cyclam 反应制得。[Ni(cyclam)]2+中,Ni2+的配位数为
(6)某镍、砷晶体结构如图所示。该晶体的密度为

您最近一年使用:0次
2 . 一般认为,含氧酸酸性强弱主要与两个因素有关:一是中心原子的电负性越大,酸性越强:一是中心原子所连接的“非羟基氧”数目越多,酸性越强。据此推断下列说法正确的是
A. 是一种二元强酸 是一种二元强酸 |
B.H3PO2的分子结构是 ,它是一种三元弱酸 ,它是一种三元弱酸 |
| C.HPO3、 HClO3、HClO4的酸性依次增强 |
D.某元素X形成的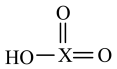 比HO-X的酸性强,氧化性也强 比HO-X的酸性强,氧化性也强 |
您最近一年使用:0次
2022-05-27更新
|
933次组卷
|
3卷引用:山东省名校联盟2022届高三下学期5月模拟考试化学试题
3 . 一种无机纳米晶体材料,仅由铯、铅、溴三种元素构成,在太阳能电池方向有巨大应用前景。回答下列问题:
(1)基态 原子核外电子占据能量最高的能级的电子云轮廓图形状为
原子核外电子占据能量最高的能级的电子云轮廓图形状为_______ 。 属于
属于_______ 区元素。
(2)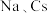 位于同主族,
位于同主族,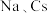 元素的第一电离能分别为
元素的第一电离能分别为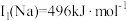 、
、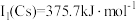 。
。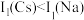 的原因是
的原因是_______ 。
(3) 三种元素的电负性如下表。
三种元素的电负性如下表。 具有较高的熔点(855℃),PbBr2具有较低的熔点(373℃),原因是
具有较高的熔点(855℃),PbBr2具有较低的熔点(373℃),原因是_______ 。
(4)该晶体材料的立方结构如图所示,其化学式为_______ 。若其晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体密度=
,则该晶体密度=_______  。
。
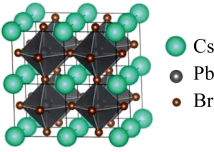
(5)该晶体材料电池并未实现商业化,原因在于自身的不稳定性。
①该晶体材料在潮湿环境中易从固体变成溶液(发生相变),导致器件效率降低,其原因是_______ 。
②某大学采用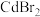 对该材料进行钝化处理可有效提高其稳定性,钝化机理如图所示。根据晶格应变驰豫,
对该材料进行钝化处理可有效提高其稳定性,钝化机理如图所示。根据晶格应变驰豫,_______ (离子)脱离晶格,用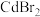 钝化后的晶体比原晶体材料更稳定,其原因是
钝化后的晶体比原晶体材料更稳定,其原因是_______ 。
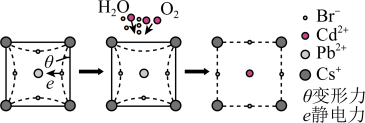
(已知:应力与应变相伴而生,从原子尺度上来理解,应力为单位晶格上的作用力,应变即为晶格的拉伸或收缩,对应于拉伸应变和压缩应变。对应出现的驰豫是指一个宏观平衡系统由于受到外界的作用变为非平衡状态,再从非平衡状态过渡到新的平衡态的过程。)
(1)基态
 原子核外电子占据能量最高的能级的电子云轮廓图形状为
原子核外电子占据能量最高的能级的电子云轮廓图形状为 属于
属于(2)
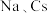 位于同主族,
位于同主族,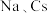 元素的第一电离能分别为
元素的第一电离能分别为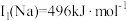 、
、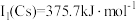 。
。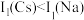 的原因是
的原因是(3)
 三种元素的电负性如下表。
三种元素的电负性如下表。 具有较高的熔点(855℃),PbBr2具有较低的熔点(373℃),原因是
具有较高的熔点(855℃),PbBr2具有较低的熔点(373℃),原因是| 电负性 | ||
| F | Br | Pb |
| 4.0 | 2.8 | 1.9 |
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体密度=
,则该晶体密度= 。
。
(5)该晶体材料电池并未实现商业化,原因在于自身的不稳定性。
①该晶体材料在潮湿环境中易从固体变成溶液(发生相变),导致器件效率降低,其原因是
②某大学采用
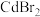 对该材料进行钝化处理可有效提高其稳定性,钝化机理如图所示。根据晶格应变驰豫,
对该材料进行钝化处理可有效提高其稳定性,钝化机理如图所示。根据晶格应变驰豫,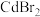 钝化后的晶体比原晶体材料更稳定,其原因是
钝化后的晶体比原晶体材料更稳定,其原因是
(已知:应力与应变相伴而生,从原子尺度上来理解,应力为单位晶格上的作用力,应变即为晶格的拉伸或收缩,对应于拉伸应变和压缩应变。对应出现的驰豫是指一个宏观平衡系统由于受到外界的作用变为非平衡状态,再从非平衡状态过渡到新的平衡态的过程。)
您最近一年使用:0次
名校
解题方法
4 . 2022年春晚节目《只此青绿》取材于宋代名画《千里江山图》,该画描绘了山清水秀的美丽景色,历经千年色彩依然,其中青色来自蓝铜矿颜料[主要成分为Cu3(CO3)2(OH)2]。请回答下列问题:
(1)基态铜原子价电子排布式为_______ 。从原子结构角度分析,第二电离能I2(Fe)与I2(Cu)的关系是I2(Fe)_______ I2(Cu) (填“>”“<”或“=”),并解释有关原因_______ 。
(2) 的空间构型为
的空间构型为_______ 。
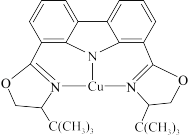
(3)我国科学家制取了一种铜的配合物如图所示,该配合物中四种非金属元素电负性由大到小的顺序是_______ (填元素符号),该配合物中采用sp2杂化的碳原子与sp3杂化的碳原子个数比为_______ 。
(4)黄铜矿是主要的炼铜原料,晶胞结构如下图1所示,晶胞中S原子的投影位置如图2所示。
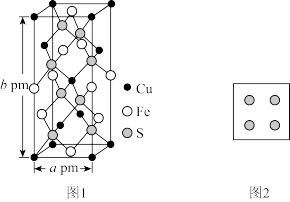
①Fe3+周围距离最近的S2-的个数为_______ 。
②该晶胞上下底面均为正方形,侧面与底面垂直,晶胞参数如图所示,晶胞的密度为ρ g/cm3,则阿伏加德罗常数(NA)为_______ mol-1(用a、b、ρ表示,并化成最简)。
(1)基态铜原子价电子排布式为
(2)
 的空间构型为
的空间构型为(3)我国科学家制取了一种铜的配合物如图所示,该配合物中四种非金属元素电负性由大到小的顺序是

(4)黄铜矿是主要的炼铜原料,晶胞结构如下图1所示,晶胞中S原子的投影位置如图2所示。

①Fe3+周围距离最近的S2-的个数为
②该晶胞上下底面均为正方形,侧面与底面垂直,晶胞参数如图所示,晶胞的密度为ρ g/cm3,则阿伏加德罗常数(NA)为
您最近一年使用:0次
2022-05-04更新
|
739次组卷
|
4卷引用:安徽省淮北市2022届高三第二次模拟考试理科综合化学试题
安徽省淮北市2022届高三第二次模拟考试理科综合化学试题(已下线)专项17 物质结构与性质综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)山东省菏泽市单县第二中学2021-2022学年高二下学期慧光班段考化学试题四川省南充高级中学2021-2022学年高二下学期期中考试化学试题
5 . 我国科学家研究发现,在KOH催化下,CO(NH2)2和LiTPSI还原形成稳定的LiF/高分子双层SEI,使LiMn2O4//Li4T15O12电池稳定工作。请回答下列问题:
(1)基态Mn2+的电子排布式为[Ar]____ 。基态K原子核外电子云轮廓图呈球形的能级上占据的电子总数为____ 。
(2)Mn的第三电离能大于Fe的第三电离能的主要原因是____ 。
(3)CO(NH2)2中元素电负性由大到小的顺序为____ (用元素符号表示)。CO(NH2)2分子中碳原子的杂化方式为____ 。
(4)几种钛的卤化物的熔点如表所示:
钛的卤化物熔点呈上述变化的主要原因是____ 。
(5)一种钛的氧化物晶胞如图1所示,其化学式为____ 。
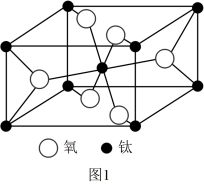
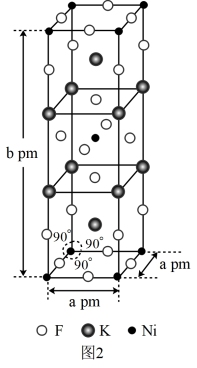
(6)由钾、镍、氟组成的一种晶体结构如图2所示,该晶体密度为____ g·cm-3(只列计算式即可)。
(1)基态Mn2+的电子排布式为[Ar]
(2)Mn的第三电离能大于Fe的第三电离能的主要原因是
(3)CO(NH2)2中元素电负性由大到小的顺序为
(4)几种钛的卤化物的熔点如表所示:
| 卤化物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -25 | 39 | 150 |
(5)一种钛的氧化物晶胞如图1所示,其化学式为

(6)由钾、镍、氟组成的一种晶体结构如图2所示,该晶体密度为

您最近一年使用:0次
6 . 我国科学家预测全固态氟离子电池(CsPb1-xKxF3-x)可能替代锂离子电池。回答下列问题:
(1)基态K原子核外电子云轮廓图呈球形的能级上占据电子总数为_______ 。基态氟离子的电子排布式为_______ 。
(2)常见的含氟分子有HF、SiF4、OF2.其中,属于非极性分子的有_______ (填化学式),氟的电负性大于氯,但是HF的酸性比HCl的弱,其主要原因是_______ (提示:从分子间作用力角度分析)。
(3)我国科学家研究发现,在锂/氟化石墨电池中添加BF3,会提高能量转化效率。放电时,发生反应为LiF(s)+BF3(g)=LiBF4(aq),BF 的空间结构为
的空间结构为_______ ,上述反应中B原子的杂化类型变化为_______ 。
(4)CsF、KF的熔点分别为682℃、858℃,其熔点差异的主要原因是_______ 。
(5)铯、金、氯组成一种晶体,已知金元素有+1、+3价,它的晶胞如图1所示。大灰球为Cs,小黑球为Cl,其余球为Au。该晶体的化学式为_______ ,其中金原子有2种不同的化学环境,形成2种不同的离子,它们是_______ 和_______ 。
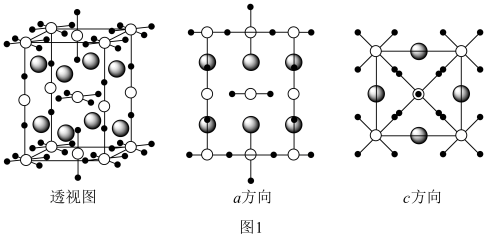
(6)铅单质的面心立方最密晶胞如图2所示。它的晶胞空隙率为_______ (用含π的式子表示;提示:晶胞空隙率=1-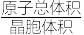 )。
)。
(1)基态K原子核外电子云轮廓图呈球形的能级上占据电子总数为
(2)常见的含氟分子有HF、SiF4、OF2.其中,属于非极性分子的有
(3)我国科学家研究发现,在锂/氟化石墨电池中添加BF3,会提高能量转化效率。放电时,发生反应为LiF(s)+BF3(g)=LiBF4(aq),BF
 的空间结构为
的空间结构为(4)CsF、KF的熔点分别为682℃、858℃,其熔点差异的主要原因是
(5)铯、金、氯组成一种晶体,已知金元素有+1、+3价,它的晶胞如图1所示。大灰球为Cs,小黑球为Cl,其余球为Au。该晶体的化学式为

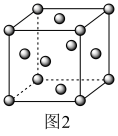
(6)铅单质的面心立方最密晶胞如图2所示。它的晶胞空隙率为
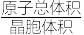 )。
)。
您最近一年使用:0次
解题方法
7 . 物质的结构决定物质的性质。请回答下列问题:
(1)下列有关物质结构与性质的说法中错误的有_______ (填标号)。
A.酸性强弱:三氟乙酸>三氯乙酸>乙酸
B.C2H4分子中的H原子与C原子之间形成s-sp2σ键
C.价层电子对互斥模型中,π键电子对数不计入中心原子的价层电子对数
D.H2S和NH3均是价层电子对数为4的极性分子,且H2S分子的键角较小
E.冰属于分子晶体,其中的氢键可以表示为O- H …O,具有“分子密堆积”特征
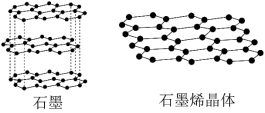
(2)石墨烯是从石墨材料中剥离出来,由碳原子组成的只有一层原子厚度的二维晶体(见下图)。从石墨中剥离出石墨烯需要破坏的作用力是_______ ,12g石墨烯中由碳原子连接成的六元环的物质的量约为_______ mol。
(3)冠醚是由多个二元醇分子之间失水形成的环状化合物,它们能与碱金属离子作用并随着环的大小不同而与不同金属离子作用。由于烯烃难溶于水,故被KMnO4水溶液氧化的效果较差。
①烯烃难溶于水的原因是_______ 。
②若在烯烃中溶人某冠醚,与KMnO4发生如下所示的变化后,氧化效果明显提升。加入该冠醚后,烯烃的氧化效果明显提升的原因是_______ 。
KMnO4+

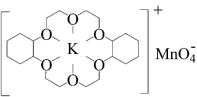
(4)多原子分子中各原子若在同一平面内,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”。下列物质中存在“离域π键”的是_______(填标号)。
(5)硅的含氧化合物都以硅氧四面体(SiO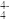 )作为基本结构单元,如图甲所示,可简化为图乙。硅氧四面体通过共用氧原子可形成各种不同的硅酸根离子,如图丙和图丁,则丙的化学式为
)作为基本结构单元,如图甲所示,可简化为图乙。硅氧四面体通过共用氧原子可形成各种不同的硅酸根离子,如图丙和图丁,则丙的化学式为_______ 。在无限长链的硅酸根离子中硅原子与氧原子个数比为_______ 。
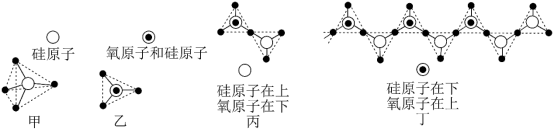
(1)下列有关物质结构与性质的说法中错误的有
A.酸性强弱:三氟乙酸>三氯乙酸>乙酸
B.C2H4分子中的H原子与C原子之间形成s-sp2σ键
C.价层电子对互斥模型中,π键电子对数不计入中心原子的价层电子对数
D.H2S和NH3均是价层电子对数为4的极性分子,且H2S分子的键角较小
E.冰属于分子晶体,其中的氢键可以表示为O- H …O,具有“分子密堆积”特征
(2)石墨烯是从石墨材料中剥离出来,由碳原子组成的只有一层原子厚度的二维晶体(见下图)。从石墨中剥离出石墨烯需要破坏的作用力是

(3)冠醚是由多个二元醇分子之间失水形成的环状化合物,它们能与碱金属离子作用并随着环的大小不同而与不同金属离子作用。由于烯烃难溶于水,故被KMnO4水溶液氧化的效果较差。
①烯烃难溶于水的原因是
②若在烯烃中溶人某冠醚,与KMnO4发生如下所示的变化后,氧化效果明显提升。加入该冠醚后,烯烃的氧化效果明显提升的原因是
KMnO4+



(4)多原子分子中各原子若在同一平面内,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”。下列物质中存在“离域π键”的是_______(填标号)。
| A.苯 | B.三氧化硫 | C.四氯化碳 | D.环己烷 |
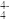 )作为基本结构单元,如图甲所示,可简化为图乙。硅氧四面体通过共用氧原子可形成各种不同的硅酸根离子,如图丙和图丁,则丙的化学式为
)作为基本结构单元,如图甲所示,可简化为图乙。硅氧四面体通过共用氧原子可形成各种不同的硅酸根离子,如图丙和图丁,则丙的化学式为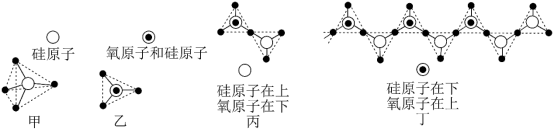
您最近一年使用:0次
名校
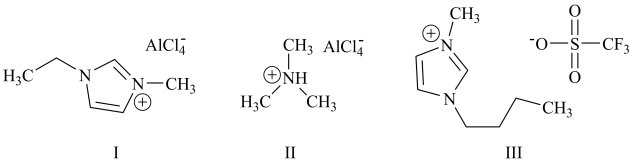
8 . 铝离子电池能量密度高、成本低且安全性高,是有前景的下一代储能电池。铝离子电池一般采用离子液体作为电解质,几种离子液体的结构如下。
(1)基态铝原子的核外电子排布式为___________ 。
(2)基态氮原子的价层电子排布图为___________(填编号)。
(3)化合物I中碳原子的杂化轨道类型为___________ ,化合物II中阳离子的空间构型为___________ 。
(4)化合物III中O、F、S电负性由大到小的顺序为___________ 。
(5)传统的有机溶剂大多易挥发,而离子液体有相对难挥发的优点,原因是___________ 。
(6)铝离子电池的其中一种正极材料为AlMn2O4,其晶胞中铝原子的骨架如图所示。___________ 。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,如图中原子1的坐标为( ,
, ,
, ),原子2的坐标为(
),原子2的坐标为( ,
, ,
, ),则原子3的坐标为
),则原子3的坐标为_____ 。
③已知该晶体属于立方晶系,晶胞参数为apm,阿伏加德罗常数的值为NA,则晶体的密度为______ g·cm-3(列出计算式)。
(1)基态铝原子的核外电子排布式为
(2)基态氮原子的价层电子排布图为___________(填编号)。
A.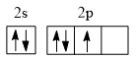 | B.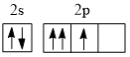 | C.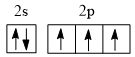 | D.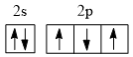 |
(4)化合物III中O、F、S电负性由大到小的顺序为
(5)传统的有机溶剂大多易挥发,而离子液体有相对难挥发的优点,原因是
(6)铝离子电池的其中一种正极材料为AlMn2O4,其晶胞中铝原子的骨架如图所示。
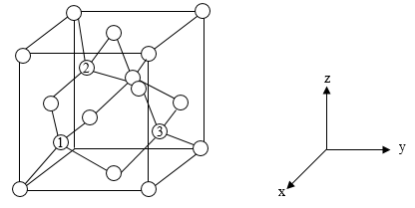
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,如图中原子1的坐标为(
 ,
, ,
, ),原子2的坐标为(
),原子2的坐标为( ,
, ,
, ),则原子3的坐标为
),则原子3的坐标为③已知该晶体属于立方晶系,晶胞参数为apm,阿伏加德罗常数的值为NA,则晶体的密度为
您最近一年使用:0次
2022-03-17更新
|
2774次组卷
|
10卷引用:广东省广州市2022届高三一模考试化学试题
广东省广州市2022届高三一模考试化学试题(已下线)必刷卷01-2022年高考化学考前信息必刷卷(全国乙卷)(已下线)回归教材重难点11 物质结构与性质(选考)-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)江西省新余市2022届高三第二次模拟考试理综化学试题吉林省长春市吉林省实验中学2022届高三最后一次模拟考试理综化学试题(已下线)广东省广州市2022届高三一模考试(结构与性质)广东省广州市2021-2022学年高三下学期一模考试化学试题2024届四川省兴文第二中学校高三上学期一诊模拟考试理综试题(已下线)热点25 物质结构与性质综合题广东省广州市第六中学2023-2024学年高二下学期期中考试化学试题
解题方法
9 . 磷及其化合物在工农业生产中都有重要作用。
(1)磷原子核外电子排布式为_______ 。
(2)羟基磷灰石[Ca5(PO4)3OH]是牙齿中的重要矿物质,其中羟基(-OH)中氧原子的杂化方式为_______ , 的空间构型为
的空间构型为_______ ,该化合物中所含元素电负性最大的是_______ 。
(3)磷化硼为立方晶系晶体,该晶胞中原子的分数坐标为:
B:(0,0,0);( ,
, ,0);(
,0);( ,0,
,0, );(0,
);(0, ,
, )……
)……
P:( ,
, ,
, );(
);( ,
, ,
, );(
);( ,
, ,
, );(
);( ,
, ,
, )……
)……
①请在图中画出磷化硼晶胞的俯视图_______ 。
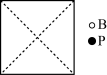
②与每个磷原子紧邻的硼原子有_______ 个,与每个硼原子紧邻的硼原子有_______ 个。
(4)磷钇矿可提取稀土元素钇(Y),某磷钇矿的结构如图所示。该磷钇矿的化学式为_______ ,与 互为等电子体的阴离子有
互为等电子体的阴离子有_______ (写出一种离子符号)。已知晶胞参数a=0.69nm,c=0.60nm,阿伏加德罗常数的值为NA,则该磷钇矿的密度为_______ g·cm-3(列出计算式)。

(1)磷原子核外电子排布式为
(2)羟基磷灰石[Ca5(PO4)3OH]是牙齿中的重要矿物质,其中羟基(-OH)中氧原子的杂化方式为
 的空间构型为
的空间构型为(3)磷化硼为立方晶系晶体,该晶胞中原子的分数坐标为:
B:(0,0,0);(
 ,
, ,0);(
,0);( ,0,
,0, );(0,
);(0, ,
, )……
)……P:(
 ,
, ,
, );(
);( ,
, ,
, );(
);( ,
, ,
, );(
);( ,
, ,
, )……
)……①请在图中画出磷化硼晶胞的俯视图

②与每个磷原子紧邻的硼原子有
(4)磷钇矿可提取稀土元素钇(Y),某磷钇矿的结构如图所示。该磷钇矿的化学式为
 互为等电子体的阴离子有
互为等电子体的阴离子有
您最近一年使用:0次
2021-07-13更新
|
404次组卷
|
3卷引用:青海省西宁市大通回族土族自治县2021届高三下学期高考二模化学试题
青海省西宁市大通回族土族自治县2021届高三下学期高考二模化学试题(已下线)专题35 磷、砷及其化合物-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)湖南省长沙市宁乡市2022届高三下学期5月模拟考试化学试题
解题方法
10 . 环己酮是重要的化工原料和化工溶剂,某研究小组对其进行了一些探究。
Ⅰ.环己酮的制备。反应原理为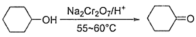 ,还原产物为
,还原产物为 ,反应过程放热,温度过高时环己酮易进一步被氧化,实验装置如图所示。
,反应过程放热,温度过高时环己酮易进一步被氧化,实验装置如图所示。
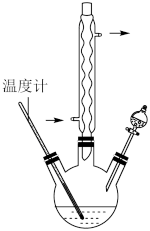
已知: 溶液呈橙红色,
溶液呈橙红色, 溶液呈墨绿色。
溶液呈墨绿色。
(1)分液漏斗中盛放的试剂为_______ 。(填字母)
a. 溶液 b.环己醇的硫酸溶液
溶液 b.环己醇的硫酸溶液
(2)三颈烧瓶中反应体系的温度需控制在55~60℃,其加热方式为_______ 。
(3)反应结束后,还需滴加甲醇,直到_______ (填实验现象)为止,随后分离提纯得到环己酮。
(4)若20.0 mL环己醇(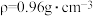 )完全反应并提纯后,得到纯环己酮(
)完全反应并提纯后,得到纯环己酮(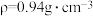 )9.6 mL,则环己酮的产率为
)9.6 mL,则环己酮的产率为_______ 。(计算结果保留2位有效数字)
Ⅱ.环己酮的结构与性质
(5)环己酮中三种元素的电负性由小到大的顺序为_______ 。(用元素符号表示)
(6)若要测定环己酮的相对分子质量,可以采用的波谱分析手段为_______ 。
(7)已知: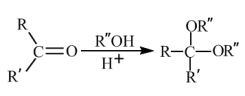 。环己酮和乙二醇在酸性条件下反应生成分子式为
。环己酮和乙二醇在酸性条件下反应生成分子式为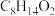 的产物,其结构简式为
的产物,其结构简式为_______ 。
Ⅰ.环己酮的制备。反应原理为
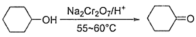 ,还原产物为
,还原产物为 ,反应过程放热,温度过高时环己酮易进一步被氧化,实验装置如图所示。
,反应过程放热,温度过高时环己酮易进一步被氧化,实验装置如图所示。
已知:
 溶液呈橙红色,
溶液呈橙红色, 溶液呈墨绿色。
溶液呈墨绿色。(1)分液漏斗中盛放的试剂为
a.
 溶液 b.环己醇的硫酸溶液
溶液 b.环己醇的硫酸溶液(2)三颈烧瓶中反应体系的温度需控制在55~60℃,其加热方式为
(3)反应结束后,还需滴加甲醇,直到
(4)若20.0 mL环己醇(
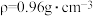 )完全反应并提纯后,得到纯环己酮(
)完全反应并提纯后,得到纯环己酮(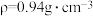 )9.6 mL,则环己酮的产率为
)9.6 mL,则环己酮的产率为Ⅱ.环己酮的结构与性质
(5)环己酮中三种元素的电负性由小到大的顺序为
(6)若要测定环己酮的相对分子质量,可以采用的波谱分析手段为
(7)已知:
 。环己酮和乙二醇在酸性条件下反应生成分子式为
。环己酮和乙二醇在酸性条件下反应生成分子式为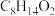 的产物,其结构简式为
的产物,其结构简式为
您最近一年使用:0次
2021-07-02更新
|
435次组卷
|
2卷引用:江苏省泰州市2020-2021学年高二下学期期末考试化学试题



