1 . X、Y、Z、W、Q五种元素的原子序数依次增大。甲、乙、丙、丁、戊为这些元素形成的化合物,R、T为其中两种元素对应的单质,T为紫红色金属,甲的水溶液显弱碱性,丁为常见无色透明且有特殊香味的液体。它们之间的转化关系如图。下列说法错误的是
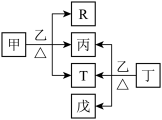
| A.第一电离能:Z>W>Y |
| B.电负性:W>Z>Y>X |
| C.X、Y、Z、W四种元素不能组成两性化合物 |
| D.X、Y、Z、Q分属于元素周期表3个不同的分区 |
您最近一年使用:0次
名校
2 . 氮、磷化合物在科研和生产中有许多重要用途。回答下列问题:
(1)氨硼烷(NH3BH3)是极具潜力的固体储氢材料,分子中与N原子相连的H呈正电性(H +),与B原子相连的H呈负电性(H
+),与B原子相连的H呈负电性(H -)。B原子的杂化方式为
-)。B原子的杂化方式为_________ ,H、B、N的电负性由大到小的顺序为____ 。与氨硼烷互为等电子体的分子是_______ (写名称),其熔点比NH3BH3低,原因是__________ 。
(2)南开大学某课题组成功合成[FeP6]2-。结构如图,环状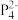 结构与苯相似,
结构与苯相似,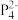 中的大π键可表示为
中的大π键可表示为___________ 。
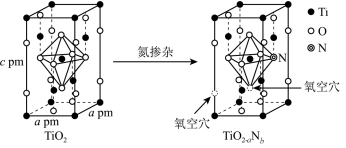
___ 种,TiO2晶胞的密度为_________ g/cm3,TiO2-aNb 晶体中a:b=_________ 。
(1)氨硼烷(NH3BH3)是极具潜力的固体储氢材料,分子中与N原子相连的H呈正电性(H
 +),与B原子相连的H呈负电性(H
+),与B原子相连的H呈负电性(H -)。B原子的杂化方式为
-)。B原子的杂化方式为(2)南开大学某课题组成功合成[FeP6]2-。结构如图,环状
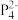 结构与苯相似,
结构与苯相似,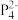 中的大π键可表示为
中的大π键可表示为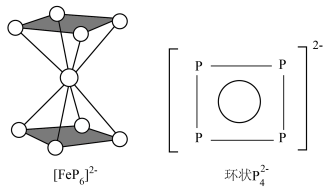
您最近一年使用:0次
名校
解题方法
3 . 氮族元素可以形成多种多样的化合物,回答下列问题:
(1)基态As原子的价电子的轨道表示式是______ 。
(2)叠氮酸(HN3)常用于引爆剂,可用联氨( )制取。比较联氨与双氧水分子中键角大小:
)制取。比较联氨与双氧水分子中键角大小:
______ 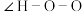 (填“>”、“=”或“<”,下同)。叠氮酸结构如图所示:
(填“>”、“=”或“<”,下同)。叠氮酸结构如图所示: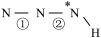 ,
, 为
为 杂化,已知参与形成π键的电子越多,键长越短,则键长;①
杂化,已知参与形成π键的电子越多,键长越短,则键长;①______ ②。
(3)乙胺( )和2-羟基乙胺(
)和2-羟基乙胺( )都可用于染料的合成,乙胺碱性更强,原因是
)都可用于染料的合成,乙胺碱性更强,原因是______ 。
(4)磷酸一氢盐受热易脱水聚合,生成环状的偏磷酸根。环状三偏磷酸根的结构如图所示,则由n个磷氧四面体连接形成的环状偏磷酸根的通式是______ 。

(5)砷与金属钠、铁、铜可形成一种绝缘体材料,其晶胞结构图钠原子沿z轴投影如图所示,已知m原子的分数坐标为 ,晶胞参数为
,晶胞参数为 ,
, 。铜周围距离最近的砷原子的个数是
。铜周围距离最近的砷原子的个数是______ ,n原子的分数坐标是______ ,若阿伏加德罗常数值为 ,该晶体密度是
,该晶体密度是______  (用含
(用含 的代数式表示)。
的代数式表示)。
(1)基态As原子的价电子的轨道表示式是
(2)叠氮酸(HN3)常用于引爆剂,可用联氨(
 )制取。比较联氨与双氧水分子中键角大小:
)制取。比较联氨与双氧水分子中键角大小:
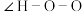 (填“>”、“=”或“<”,下同)。叠氮酸结构如图所示:
(填“>”、“=”或“<”,下同)。叠氮酸结构如图所示: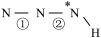 ,
, 为
为 杂化,已知参与形成π键的电子越多,键长越短,则键长;①
杂化,已知参与形成π键的电子越多,键长越短,则键长;①(3)乙胺(
 )和2-羟基乙胺(
)和2-羟基乙胺( )都可用于染料的合成,乙胺碱性更强,原因是
)都可用于染料的合成,乙胺碱性更强,原因是(4)磷酸一氢盐受热易脱水聚合,生成环状的偏磷酸根。环状三偏磷酸根的结构如图所示,则由n个磷氧四面体连接形成的环状偏磷酸根的通式是

(5)砷与金属钠、铁、铜可形成一种绝缘体材料,其晶胞结构图钠原子沿z轴投影如图所示,已知m原子的分数坐标为
 ,晶胞参数为
,晶胞参数为 ,
, 。铜周围距离最近的砷原子的个数是
。铜周围距离最近的砷原子的个数是 ,该晶体密度是
,该晶体密度是 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2024-05-21更新
|
475次组卷
|
2卷引用:山东省潍坊市2024届高三下学期二模化学试题
解题方法
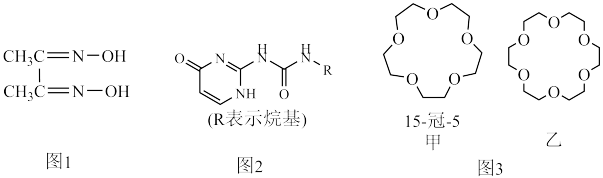
4 . 配合物和超分子广泛应用于新材料合成、物质的鉴别和分离。如丁二酮肟(如图1)可用于鉴别 Ni2+,嘧啶衍生物(如图2)是形成高韧性超分子的单体,冠醚(如图3)是皇冠状分子,可有大小不同的空穴适配不同大小的碱金属离子。
(1)基态 Ni2+核外未成对电子的数目为______ 。
(2)丁二酮肟与 Ni²⁺生成血红色配合物的结构为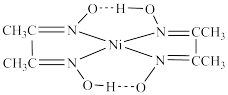 ,相同压强下,该配合物的沸点低于干二酮肟的原因为
,相同压强下,该配合物的沸点低于干二酮肟的原因为_______ 。
(3)Ni在一定条件下可与CO形成 Ni(CO)x,分子中每个Ni原子的价电子数及其周围CO提供的成键电子数之和为18,则x=_______ 。
(4)图2所示分子所含元素电负性由小到大的顺序为______ 。
(5)冠醚是状如皇冠的一类醚,分子中存在空穴,图3中甲、乙两种冠醚可分别识别 Na+、K+,其主要原因为________ ;乙的名称为______ 。
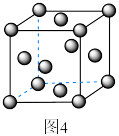
(6)金属Ni的立方晶胞结构如图4所示,则Ni的空间利用率为________ (用含π的代式表示)。
(1)基态 Ni2+核外未成对电子的数目为
(2)丁二酮肟与 Ni²⁺生成血红色配合物的结构为
 ,相同压强下,该配合物的沸点低于干二酮肟的原因为
,相同压强下,该配合物的沸点低于干二酮肟的原因为(3)Ni在一定条件下可与CO形成 Ni(CO)x,分子中每个Ni原子的价电子数及其周围CO提供的成键电子数之和为18,则x=
(4)图2所示分子所含元素电负性由小到大的顺序为
(5)冠醚是状如皇冠的一类醚,分子中存在空穴,图3中甲、乙两种冠醚可分别识别 Na+、K+,其主要原因为
(6)金属Ni的立方晶胞结构如图4所示,则Ni的空间利用率为
您最近一年使用:0次
解题方法
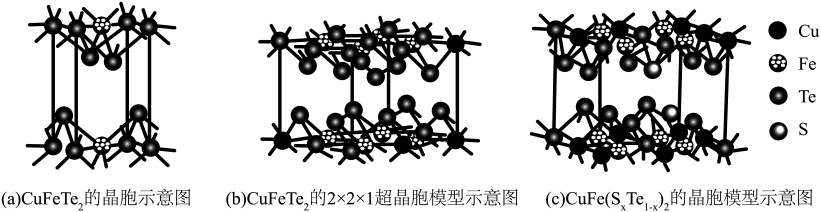
5 . 四方晶系CuFeTe2晶体是一种p型半导体,在太阳能半导体薄膜中具有巨大的潜在应用价值,其晶胞示意图如图a、图b所示。
(1)基态Cu原子的价电子排布式为___________ ;
(2)H2S中S的杂化方式为___________ ;H2O、H2Te、H2S沸点依次降低的原因是___________ 。
(3)CuFeTe2中元素的电负性由大到小的顺序为___________ ;Te的配位数为___________ 。
(4)向CuFeTe2中掺杂S原子会改善半导体性能。由图(c)可知x=___________ ;掺杂后晶胞参数分别为apm,apm,cpm,设NA为阿伏加德罗常数的值。晶体CuFe(SxTe1-x)的密度为___________ g/cm3(用含a、c和NA的代数式表示)。
(1)基态Cu原子的价电子排布式为
(2)H2S中S的杂化方式为
(3)CuFeTe2中元素的电负性由大到小的顺序为
(4)向CuFeTe2中掺杂S原子会改善半导体性能。由图(c)可知x=
您最近一年使用:0次
解题方法
6 . 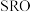 是高温超导或非常规超导物理中的重要角色,同时还是很好的催化材料。回答下列问题:
是高温超导或非常规超导物理中的重要角色,同时还是很好的催化材料。回答下列问题:
(1) 与铁在元素周期表中是同列相邻元素且最外层有一个未成对电子,其价电子排布式为
与铁在元素周期表中是同列相邻元素且最外层有一个未成对电子,其价电子排布式为___________ 。
(2) 可形成
可形成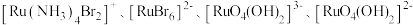 四种配离子且配离子中不存在非极性键,其中
四种配离子且配离子中不存在非极性键,其中 离子半径最小的配离子是
离子半径最小的配离子是___________ ,具有对称结构的 中
中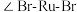 为
为___________ 。图1中通过螯合作用形成配位键的N原子的杂化方式为___________ , 离子配体中N原子与中心
离子配体中N原子与中心 离子配位的原因是
离子配位的原因是___________ 。

(3)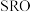 的晶体结构如图2所示。
的晶体结构如图2所示。
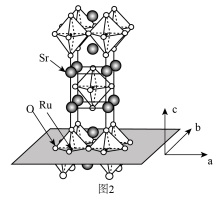
① 和
和 的电负性:
的电负性:
___________  (填“大于”“小于”或“等于”),基态O原子电子占据最高能级的电子云轮廓图为
(填“大于”“小于”或“等于”),基态O原子电子占据最高能级的电子云轮廓图为___________ 形。
②用 表示阿伏伽德罗常数的值,晶胞参数为
表示阿伏伽德罗常数的值,晶胞参数为 ,
, ,则其密度为
,则其密度为___________  (列出计算式即可)。
(列出计算式即可)。
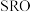 是高温超导或非常规超导物理中的重要角色,同时还是很好的催化材料。回答下列问题:
是高温超导或非常规超导物理中的重要角色,同时还是很好的催化材料。回答下列问题:(1)
 与铁在元素周期表中是同列相邻元素且最外层有一个未成对电子,其价电子排布式为
与铁在元素周期表中是同列相邻元素且最外层有一个未成对电子,其价电子排布式为(2)
 可形成
可形成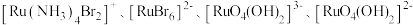 四种配离子且配离子中不存在非极性键,其中
四种配离子且配离子中不存在非极性键,其中 离子半径最小的配离子是
离子半径最小的配离子是 中
中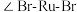 为
为 离子配体中N原子与中心
离子配体中N原子与中心 离子配位的原因是
离子配位的原因是
(3)
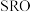 的晶体结构如图2所示。
的晶体结构如图2所示。
①
 和
和 的电负性:
的电负性:
 (填“大于”“小于”或“等于”),基态O原子电子占据最高能级的电子云轮廓图为
(填“大于”“小于”或“等于”),基态O原子电子占据最高能级的电子云轮廓图为②用
 表示阿伏伽德罗常数的值,晶胞参数为
表示阿伏伽德罗常数的值,晶胞参数为 ,
, ,则其密度为
,则其密度为 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
解题方法
7 . 金属锂溶于液氨可得到具有高反应活性的金属电子溶液,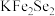 与其作用可制得超导体
与其作用可制得超导体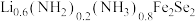 ,进一步可制得超导材料
,进一步可制得超导材料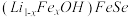 。
。
回答下列问题:
(1)与Fe元素同周期,基态原子有2个未成对电子的金属元素有______ 种,下列状态的铁中,电离最外层一个电子所需能量最大的是______ (填标号)
A. B.
B. C.
C.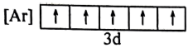 D.
D.
(2)液氨可以发生微弱的电离生成 和
和 ,下列说法错误的是
,下列说法错误的是________
(3)Fe2+可与邻二氮菲形成红色配合物,结构如图所示。元素的电负性从大到小的顺序为______ (填元素符号)。配合物中N原子的VSEPR模型为____________ ;下列对Fe杂化方式推断合理的是______ (填标号)。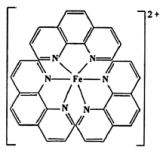
A. B.
B. C.
C. D.
D.
(4)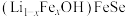 晶体属四方晶系,其结构由铁硒层和锂铁氢氧层交替堆垛而成,晶胞中铁硒层在bc、ac和ab平面投影如图所示。铁硒层中Fe原子的配位数是
晶体属四方晶系,其结构由铁硒层和锂铁氢氧层交替堆垛而成,晶胞中铁硒层在bc、ac和ab平面投影如图所示。铁硒层中Fe原子的配位数是______ ,铁硒层和锂铁氢氧层之间由极其微弱的氢键相连,该氢键可表示为______ 。已知锂铁氢氧层中锂铁个数之比为4∶1,阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为______ g·cm 。
。

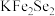 与其作用可制得超导体
与其作用可制得超导体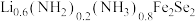 ,进一步可制得超导材料
,进一步可制得超导材料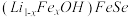 。
。回答下列问题:
(1)与Fe元素同周期,基态原子有2个未成对电子的金属元素有
A.
 B.
B. C.
C. D.
D.
(2)液氨可以发生微弱的电离生成
 和
和 ,下列说法错误的是
,下列说法错误的是A.键角: | B.结合质子能力: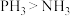 |
C.热稳定性: | D. 与 与 的分子构型及N的化合价均相同 的分子构型及N的化合价均相同 |

A.
 B.
B. C.
C. D.
D.
(4)
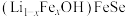 晶体属四方晶系,其结构由铁硒层和锂铁氢氧层交替堆垛而成,晶胞中铁硒层在bc、ac和ab平面投影如图所示。铁硒层中Fe原子的配位数是
晶体属四方晶系,其结构由铁硒层和锂铁氢氧层交替堆垛而成,晶胞中铁硒层在bc、ac和ab平面投影如图所示。铁硒层中Fe原子的配位数是 ,则该晶体的密度为
,则该晶体的密度为 。
。
您最近一年使用:0次
8 . 前四周期元素W、X、Y、Z的原子序数依次增大。基态W原子中有7个运动状态不同的电子,基态X原子最高能级中自旋状态不同的电子数之比为 ,基态Y原子的价层电子排布式为
,基态Y原子的价层电子排布式为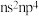 ,基态Z原子次外层全充满,最外层电子数为1,下列说法错误的是
,基态Z原子次外层全充满,最外层电子数为1,下列说法错误的是
 ,基态Y原子的价层电子排布式为
,基态Y原子的价层电子排布式为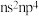 ,基态Z原子次外层全充满,最外层电子数为1,下列说法错误的是
,基态Z原子次外层全充满,最外层电子数为1,下列说法错误的是| A.电负性:X>W>Y | B.熔点:化合物ZX>化合物ZY |
| C.简单氢化物的稳定性:W<X | D.X、Y形成的化合物一定为极性分子 |
您最近一年使用:0次
2023-04-28更新
|
545次组卷
|
3卷引用:山东省东营市第一中学2023届高三下学期二模化学试题
2023·河南郑州·二模
名校
解题方法
9 . 2023年1月30日,中国科学院朱庆山团队研究六方相砷化镍(NiAs)型到正交相磷化锰(MnP)型结构转变,实现了对锂硫催化剂的精确设计。回答下列问题:
(1)Li、P、S三种元素中,电负性最小的是___________ 。第三周期元素中第一电离能比P大的元素有___________ 种。
(2)基态S原子核外有___________ 个电子自旋状态相同。基态As原子的电子排布式为___________ 。
(3)PH3、AsH3中沸点较高的是___________ ,其主要原因是___________ 。
(4)Mn的一种配合物化学式为[Mn(CO)5(CH3CN)],该配合物中锰原子的配位数为___________ 。
(5)CH3CN中C原子的杂化类型为___________ 。
(6)等物质的量的CH3CN和CO中,π键数目之比___________ 。
(7)NiAs的一种晶胞结构如图所示。若阿伏加德罗常数的值为NA,晶体的密度为ρ g/cm3,则该晶胞中最近的砷原子之间的距离为___________ pm。

(1)Li、P、S三种元素中,电负性最小的是
(2)基态S原子核外有
(3)PH3、AsH3中沸点较高的是
(4)Mn的一种配合物化学式为[Mn(CO)5(CH3CN)],该配合物中锰原子的配位数为
(5)CH3CN中C原子的杂化类型为
(6)等物质的量的CH3CN和CO中,π键数目之比
(7)NiAs的一种晶胞结构如图所示。若阿伏加德罗常数的值为NA,晶体的密度为ρ g/cm3,则该晶胞中最近的砷原子之间的距离为

您最近一年使用:0次
2023-04-06更新
|
736次组卷
|
4卷引用:化学-2023年高考押题预测卷03(山东卷)(含考试版、全解全析、参考答案、答题卡)
(已下线)化学-2023年高考押题预测卷03(山东卷)(含考试版、全解全析、参考答案、答题卡)河南省郑州市2023届高三下学期第二次质量预测理科综合化学试题(已下线)考点43 晶体结构与性质(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)甘肃省武威第一中学2023-2024学年高三上学期第三次月考化学试题
名校
解题方法
10 . 硒化锌是一种重要的半导体材料;其晶胞结构如图甲所示,已知晶胞参数为pnm,乙图为晶胞的俯视图,下列说法正确的是
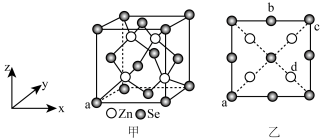
| A.晶胞中硒原子的配位数为12 |
B.晶胞中d点原子分数坐标为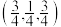 |
C.相邻两个Zn原子的最短距离为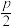 nm nm |
| D.电负性:Zn>Se |
您最近一年使用:0次
2023-03-03更新
|
1858次组卷
|
11卷引用:山东省济宁市2023届高三一模考试(3月)化学试题
山东省济宁市2023届高三一模考试(3月)化学试题山东省德州市第一中学2022-2023学年高二下学期3月月考化学试题河北省张家口市宣化第一中学2023届高三模拟试题(三)化学试题山东省烟台市第一中学2023-2024学年高三下学期3月月考化学试题山东省临沂市第二十四中学2023-2024学年高二下学期3月学科素养水平监测化学试题(已下线)湖北省七市(州)2023届高三3月联合统一调研测试化学试题变式题(选择题11-15)河南省郑州市六校联盟2022-2023学年高二下学期4月期中考试化学试题(已下线)专题十 晶胞示意图(练)福建省龙岩市连城县第一中学2022-2023学年高二下学期5月月考化学试题河南省驻马店市环际大联考2022-2023学年高二下学期4月期中考试化学试题(已下线)热点08 金属晶体和离子晶体



