解题方法
1 . Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1) 的价电子排布图为:
的价电子排布图为:__ ;基态磷原子有___ 种空间运动状态不同的电子。
(2)Li、O、P三种元素的电负性由大到小的顺序是:__ 。
(3)写出一种与 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:__ ,该分子的中心原子的价层电子对数等于__ 。
(4)已知无水硫酸铜为白色粉末,溶于水形成蓝色溶液,则硫酸铜稀溶液中不存在的微粒间作用力有:__ 。
A.配位键 B.金属键 C.离子键 D.共价键 E.氢键 F.范德华力
(5)N和P是同主族元素,但是 分子中的键角大于
分子中的键角大于 分子中的键角,原因是:
分子中的键角,原因是:___ 。
(6) 为离子晶体,具有反萤石结构,晶胞如下图所示。则
为离子晶体,具有反萤石结构,晶胞如下图所示。则 配位数为:
配位数为:__ ,若晶胞参数为bnm,阿伏加德罗常数的值为 ,则
,则 的密度为
的密度为__  (列出计算式即可)。
(列出计算式即可)。

(1)
 的价电子排布图为:
的价电子排布图为:(2)Li、O、P三种元素的电负性由大到小的顺序是:
(3)写出一种与
 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:(4)已知无水硫酸铜为白色粉末,溶于水形成蓝色溶液,则硫酸铜稀溶液中不存在的微粒间作用力有:
A.配位键 B.金属键 C.离子键 D.共价键 E.氢键 F.范德华力
(5)N和P是同主族元素,但是
 分子中的键角大于
分子中的键角大于 分子中的键角,原因是:
分子中的键角,原因是:(6)
 为离子晶体,具有反萤石结构,晶胞如下图所示。则
为离子晶体,具有反萤石结构,晶胞如下图所示。则 配位数为:
配位数为: ,则
,则 的密度为
的密度为 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
2021-04-06更新
|
486次组卷
|
2卷引用:江西省鹰潭市2021届高三一模理综化学试题
名校
解题方法
2 . N、P、As都是VA族元素,且原子序数依次增大,它们的单质和化合物在生产、生活中有广泛应用。请回答下列相关问题。
(1)基态砷原子的价电子排布式为____ 。
(2)从结构分析硝酸符合形成氢键的条件但硝酸的沸点较低,其可能的原因是____ 。
(3) 与钴盐形成的配离子[Co(NO2)6]3-可用于检验K+的存在。
与钴盐形成的配离子[Co(NO2)6]3-可用于检验K+的存在。 离子的VSEPR模型名称为
离子的VSEPR模型名称为___ ,K3[Co(NO2)6]是黄色沉淀,该物质中四种元素的电负性由大到小的顺序是___ 。(用元素符号表示)
(4)磷化硼(BP)可作为金属表面的保护薄膜,其晶胞如图1所示,在BP晶胞中B原子配位数是___ ,P原子占据的是B原子堆积的____ (选填“立方体”“正四面体”或“正八面体”)空隙。建立如图2所示坐标系,可得晶胞中A、C处原子的分数坐标,则M处的P原子分数坐标为____ ,若晶胞中B原子和P原子之间的最近核间距为a pm,则晶胞边长为____ cm。
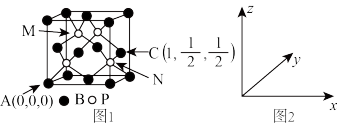
(1)基态砷原子的价电子排布式为
(2)从结构分析硝酸符合形成氢键的条件但硝酸的沸点较低,其可能的原因是
(3)
 与钴盐形成的配离子[Co(NO2)6]3-可用于检验K+的存在。
与钴盐形成的配离子[Co(NO2)6]3-可用于检验K+的存在。 离子的VSEPR模型名称为
离子的VSEPR模型名称为(4)磷化硼(BP)可作为金属表面的保护薄膜,其晶胞如图1所示,在BP晶胞中B原子配位数是

您最近一年使用:0次
2021-03-26更新
|
385次组卷
|
2卷引用:江西省抚州市临川第一中学2022届高三下学期4月模拟考试理科综合化学试题
3 . 利用铟(In)与锡(Sn)形成的金属间化合物InSn为基体,N(C2H5)3为催化剂,可将CO2与H2转化为HCOOH,反应的化学方程式为:CO2+H2 HCOOH。回答下列问题:
HCOOH。回答下列问题:
(1)In与Al为同族元素,其核外电子占据最高能层的符号为O,则In在元素周期表中的位置为___ 。基态In原子最高能级电子云轮廓图为____ 形。
(2)Sb为第ⅤA族从上到下的第四种元素,其价电子的轨道表示式为______ 。
(3)化学方程式中涉及的四种非金属元素电负性由小到大的顺序为_____ (用元素符号表示)。写出与CO2互为等电子体的一种阴离子____ (填离子符号)。
(4)催化剂N(C2H5)3分子中N原子的杂化方式为_____ ,其中碳原子成键电子对的空间构型为_____ 。
(5)HCOOH在水中溶解度远大于CO2的原因为____________ 。
(6)InSb晶体晶胞为立方晶胞(如图1),晶胞参数为631 pm,Sb位于顶点和面心,In位于Sb原子构成的四面体的体心。InSb晶体常用作金属锂的镶嵌材料,某种镶嵌锂之后的晶胞如图2,晶胞参数为664 pm(“ ”代表锂原子)。
”代表锂原子)。
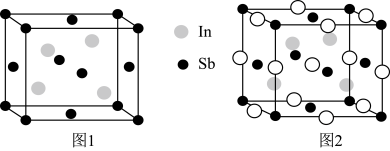
①图1所示晶胞中,距离最近的两个In原子间的距离为______ pm。(已知 ≈1.4)
≈1.4)
②图2所示晶胞的密度为______ g·cm−3。(列出计算式即可)
 HCOOH。回答下列问题:
HCOOH。回答下列问题: (1)In与Al为同族元素,其核外电子占据最高能层的符号为O,则In在元素周期表中的位置为
(2)Sb为第ⅤA族从上到下的第四种元素,其价电子的轨道表示式为
(3)化学方程式中涉及的四种非金属元素电负性由小到大的顺序为
(4)催化剂N(C2H5)3分子中N原子的杂化方式为
(5)HCOOH在水中溶解度远大于CO2的原因为
(6)InSb晶体晶胞为立方晶胞(如图1),晶胞参数为631 pm,Sb位于顶点和面心,In位于Sb原子构成的四面体的体心。InSb晶体常用作金属锂的镶嵌材料,某种镶嵌锂之后的晶胞如图2,晶胞参数为664 pm(“
 ”代表锂原子)。
”代表锂原子)。
①图1所示晶胞中,距离最近的两个In原子间的距离为
 ≈1.4)
≈1.4)②图2所示晶胞的密度为
您最近一年使用:0次
名校
解题方法
4 . 黑磷是磷的一种稳定的同素异形体,黑磷具有正交晶系的晶体结构(图A),晶胞参数a=3.310A,b=4.380A,c=10.500A。黑磷烯是二维的单层黑磷(图B),黑磷烯与石墨烯结构相似,P的配位数为3。与石墨烯相比,黑磷烯具有半导体性质,更适合于制作电子器件。已知黑磷结构中只有一种等效的三配位P,所有P原子的成键环境一样,图A中编号为①的P原子的晶胞内坐标为(0.50,0.090,0.598)。请回答下列问题:
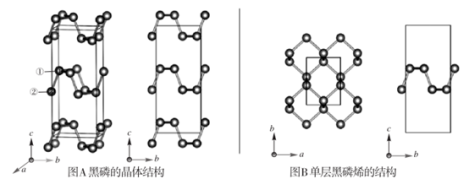
(1)写出P原子的价电子排布:___ 。
(2)P和F的电负性大小顺序是X(P)___ X(F)。(填“<”“=”或“>”)P和F形成的分子PF3和PF5,它们的几何构型分别为__ 、__ 。
(3)①黑磷中P原子杂化类型是__ 。黑磷中不存在__ (选填字母序号)。
A.共价键 B.σ键 C.π键 D.范德华力
②红磷、白磷与黑磷熔点从高到低的顺序为__ ,原因是__ 。
(4)图A中编号为②的P原子的晶胞内坐标为__ ,黑磷的晶胞中含有__ 个P原子。

(1)写出P原子的价电子排布:
(2)P和F的电负性大小顺序是X(P)
(3)①黑磷中P原子杂化类型是
A.共价键 B.σ键 C.π键 D.范德华力
②红磷、白磷与黑磷熔点从高到低的顺序为
(4)图A中编号为②的P原子的晶胞内坐标为
您最近一年使用:0次
2020-07-13更新
|
233次组卷
|
2卷引用:江西省吉安、抚州、赣州市2020届高三一模理科综合化学试题
5 . 钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,回答下列问题:
(1)基态Ti原子的核外电子排布式为____________ 。
(2)Ti的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是____________ 。
(3)CaTiO3的晶胞如图(a)所示,其组成元素的电负性大小顺序是__________ ;金属离子与氧离子间的作用力为__________ ,Ca2+的配位数是__________ 。
(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I﹣和有机碱离子 ,其晶胞如图(b)所示。其中Pb2+与图(a)中
,其晶胞如图(b)所示。其中Pb2+与图(a)中__________ 的空间位置相同,有机碱 中,N原子的杂化轨道类型是
中,N原子的杂化轨道类型是__________ ;若晶胞参数为a nm,则晶体密度为_________ g·cm-3(列出计算式)。_______ 、_______ 。
(1)基态Ti原子的核外电子排布式为
(2)Ti的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | ﹣24.12 | 38.3 | 155 |
(3)CaTiO3的晶胞如图(a)所示,其组成元素的电负性大小顺序是
(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I﹣和有机碱离子
 ,其晶胞如图(b)所示。其中Pb2+与图(a)中
,其晶胞如图(b)所示。其中Pb2+与图(a)中 中,N原子的杂化轨道类型是
中,N原子的杂化轨道类型是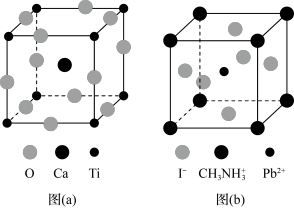
您最近一年使用:0次
2020-07-08更新
|
15508次组卷
|
21卷引用:江西省九江市2022届第二次高考模拟统一考试理综化学试题
江西省九江市2022届第二次高考模拟统一考试理综化学试题2020年全国卷Ⅱ化学真题变式题贵州省罗甸县边阳中学2022届高三模拟测试化学试题2020年全国统一考试化学试题(新课标Ⅱ)(已下线)专题17 物质结构与性质(选修)-2020年高考真题和模拟题化学分项汇编(已下线)专题11 物质结构与性质——备战2021年高考化学纠错笔记(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)押全国卷理综第35题 物质结构与性质-备战2021年高考化学临考题号押题北京一零一中学2021-2022学年高三上学期10月月考化学试题(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题13 物质结构与性质—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)回归教材重难点11 物质结构与性质(选考)-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)押全国卷理综第35题 物质结构与性质-备战2022年高考化学临考题号押题(课标全国卷)(已下线)专题18物质结构与性质(选修)-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题18物质结构与性质(选修)-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题九 物质结构与性质-实战高考·二轮复习核心突破(已下线)专题02 物质结构专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)(已下线)专题20 结构与性质四川省成都锦江区嘉祥外国语高级中学2023-2024学年高三下学期第一次诊断性考试理科综合试题-高中化学河南省开封市铁路中学2020-2021学年高二下学期期中考试化学试题重庆市万州第二高级中学2021-2022学年高二下学期6月第三次质量检测化学试题
解题方法
6 . 黑磷是磷的一种稳定的同素异形体,黑磷具有正交晶系的晶体结构(图A),晶胞参数a=3.310A,b=4.380A。,c=10.500A。。黑磷烯是二维的单层黑磷(图B),黑磷烯与石墨烯结构相似,P的配位数为3。与石墨烯相比,黑磷烯具有半导体性质,更适合于制作电子器件。已知黑磷结构中只有一种等效的三配位 P,所有P原子的成键环境一样,图 A中编 号为①的 P原子的晶胞内坐标为(0.500,0.090,0.598)。请回答下列问题:
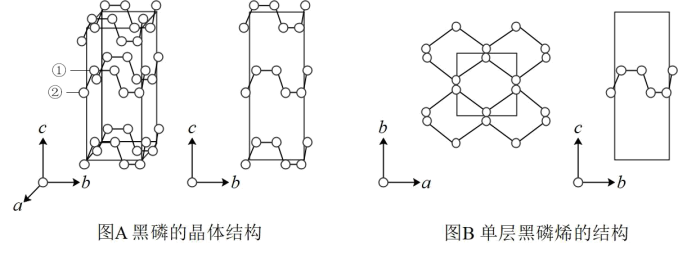
(1)写出基态P原子的价电子排布图: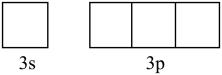
__________ 。
(2)P和 F的电负性大小顺序是 x(P)______ x(F)。(填 “<” “ =” 或 “ >” )P和 F形成的分子 PF3和PF5,它们的几何构型分别为__________ 、__________ 。
(3)①黑磷中 P原子杂化类型是__________ 。黑磷中不存在__________ (选填字母序号)。
A 共价键 B σ键 C π键 D 范德华力
②红磷、白磷与黑磷熔点从高到低的顺序为__________ ,原因是___________ 。
(4)图 A中编号为②的 P原子的晶胞内坐标为_______ ,黑磷的晶胞中含有________ 个 P原子。

(1)写出基态P原子的价电子排布图:

(2)P和 F的电负性大小顺序是 x(P)
(3)①黑磷中 P原子杂化类型是
A 共价键 B σ键 C π键 D 范德华力
②红磷、白磷与黑磷熔点从高到低的顺序为
(4)图 A中编号为②的 P原子的晶胞内坐标为
您最近一年使用:0次
名校
解题方法
7 . 钯(Pd)、锌及其化合物在合成酮类物质中有极其重要的作用,如图为合成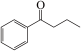 的反应过程:
的反应过程:
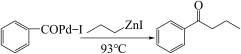
回答下列问题:
(1)I原子价电子排布式为___________ ,其能量最高的能层是___________ (填能层符号)。
(2)H、C、O三种元素的电负性由大到小的顺序为___________ 。
(3)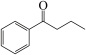 中碳原子的杂化方式为
中碳原子的杂化方式为___________ 。
(4)ZnCl2溶液中加入足量氨水,发生的反应为ZnCl2+4NH3·H2O=[Zn(NH3)4]Cl2+4H2O。
①上述反应涉及的物质中,固态时属于分子晶体的是___________ 。
②NH3的空间构型为___________ 。
③1 mol [Zn(NH3)4]Cl2中含有___________ mol σ键。
(5)Zn和Cu可形成金属互化物(ZnCu),该金属互化物中所有金属原子均按面心立方最密堆积,若所有Cu均位于晶胞的面心,则Zn位于晶胞的___________ 。
(6)金属钯的堆积方式如图所示:
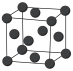
①该晶胞中原子的空间利用率为___________ (用含π的式子表示)。
②若该晶胞参数a=658 pm,则该晶胞密度为___________ (列出计算表达式)g·cm-3。
 的反应过程:
的反应过程:
回答下列问题:
(1)I原子价电子排布式为
(2)H、C、O三种元素的电负性由大到小的顺序为
(3)
 中碳原子的杂化方式为
中碳原子的杂化方式为(4)ZnCl2溶液中加入足量氨水,发生的反应为ZnCl2+4NH3·H2O=[Zn(NH3)4]Cl2+4H2O。
①上述反应涉及的物质中,固态时属于分子晶体的是
②NH3的空间构型为
③1 mol [Zn(NH3)4]Cl2中含有
(5)Zn和Cu可形成金属互化物(ZnCu),该金属互化物中所有金属原子均按面心立方最密堆积,若所有Cu均位于晶胞的面心,则Zn位于晶胞的
(6)金属钯的堆积方式如图所示:

①该晶胞中原子的空间利用率为
②若该晶胞参数a=658 pm,则该晶胞密度为
您最近一年使用:0次
2020-04-29更新
|
313次组卷
|
4卷引用:江西省南昌市八一中学2020届高三第三次模拟理科综合化学试题
江西省南昌市八一中学2020届高三第三次模拟理科综合化学试题2020年全国高考冲刺压轴卷(样卷) 理综(全国1卷)化学试题(已下线)第十一单元 物质的结构与性质测试题-2021年高考化学一轮复习名师精讲练安徽省六安市舒城中学2019-2020学年高二下学期期末考试化学试题
解题方法
8 . GaN是制造5G芯片的材料,氮化镓和氮化铝LED可发出紫外光。回答下列问题:
(1)基态Ga原子的核外电子排布式为[Ar]____ 。
(2)根据元素周期律,元素的电负性Ga____ (填“大于”或“小于”,下同)As。
(3)科学家合成了一种阳离子为“N5n+”,其结构是对称的,5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N5n+”化学式为“N8”的离子晶体,其电子式为____ ,其中的阴离子的空间构型为____ 。
(4)组成相似的CaF3和GaCl3晶体,前者属于离子晶体,后者属于分子晶体。从F-和Cl-结构的不同分析其原因是________ 。
(5)原子晶体GaAs的晶胞参数a=xpm,它的晶胞结构如下图所示。该晶胞内部存在的共价键数为___ ;紧邻的As原子之间的距离为b,紧邻的As、Ca原子之间的距离为d,则b:d=____ ,该晶胞的密度为__ g ▪cm-3。(阿伏加 德罗常数用NA表示)

(1)基态Ga原子的核外电子排布式为[Ar]
(2)根据元素周期律,元素的电负性Ga
(3)科学家合成了一种阳离子为“N5n+”,其结构是对称的,5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N5n+”化学式为“N8”的离子晶体,其电子式为
(4)组成相似的CaF3和GaCl3晶体,前者属于离子晶体,后者属于分子晶体。从F-和Cl-结构的不同分析其原因是
(5)原子晶体GaAs的晶胞参数a=xpm,它的晶胞结构如下图所示。该晶胞内部存在的共价键数为

您最近一年使用:0次
名校
解题方法
9 . (NH4)3[Fe(SCN)6]、[Fe(TCNE)(NCCH3)2][FeCl4] 、K4[Fe(CN)6]·3H2O等铁的配合物用途非常广泛。回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为______ 。
(2)Fe与Ca位于同一周期且最外层电子构型相同,铁的熔点和沸点均比钙的高,其原因是____ 。
(3)配合物(NH4)3[Fe(SCN)6]中的H、S、N的电负性从大到小的顺序是_____ 。
(4)[Fe(TCNE)(NCCH3)2][FeCl4]中,配体为CH3CN和TCNE(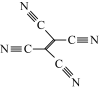 )。
)。
①CH3CN中碳原子的杂化方式是____ 和_____ 。
②TCNE中第一电离能较大的是___ (填元素符号),分子中所有原子____ (填“在”或“不在”)同一平面,分子中σ 键与π键的数目之比是 ___ 。
(5)K4[Fe(CN)6]·3H2O是食盐的抗结剂,强热分解有Fe3C生成, Fe3C 的晶胞结构如图所示:

Fe3C的密度为___ (列出计算式)g·cm-3。
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为
(2)Fe与Ca位于同一周期且最外层电子构型相同,铁的熔点和沸点均比钙的高,其原因是
(3)配合物(NH4)3[Fe(SCN)6]中的H、S、N的电负性从大到小的顺序是
(4)[Fe(TCNE)(NCCH3)2][FeCl4]中,配体为CH3CN和TCNE(
 )。
)。①CH3CN中碳原子的杂化方式是
②TCNE中第一电离能较大的是
(5)K4[Fe(CN)6]·3H2O是食盐的抗结剂,强热分解有Fe3C生成, Fe3C 的晶胞结构如图所示:

Fe3C的密度为
您最近一年使用:0次
2020-04-06更新
|
624次组卷
|
4卷引用:江西省九江市十校2020届高三下学期模拟考试理综化学试题
江西省九江市十校2020届高三下学期模拟考试理综化学试题河南等省五岳2020届高三4月联考(全国I卷)理综化学试题河南省临颍县南街高级中学2020届高三下学期第一次月考理综化学试题(已下线)01 物质结构与性质综合题型集训(1) (解析)-备战2023年高考化学大题逐空突破系列(全国通用)
解题方法
10 . 2019年诺贝尔化学奖授予三位化学家,以表彰其对研究开发锂离子电池作出的卓越贡献。LiFePO4、聚乙二醇、LiPF6、LiAsF6和LiCl等可作锂离子聚合物电池的材料。回答下列问题:
(1)Fe的价层电子排布式为___ 。
(2)Li、F、P、As四种元素的电负性由大到小的顺序为___ 。
(3)乙二醇(HOCH2CH2OH)的相对分子质量与丙醇(CH3CH2CH2OH)相近,但沸点高出100℃,原因是___ 。
(4)电池工作时,Li+沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出)。电解质LiPF6或LiAsF6的阴离子结构如图乙所示(X=P、As)。
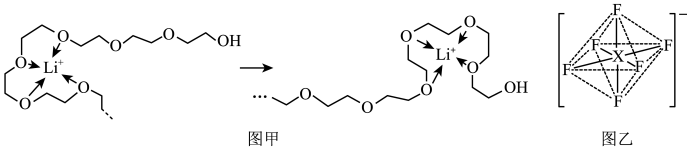
①聚乙二醇分子中,碳、氧的杂化类型分别是___ 、___ 。
②从化学键角度看,Li+迁移过程发生___ (填“物理变化”或“化学变化”)。
③PF6中P的配位数为___ 。
④相同条件,Li+在___ (填“LiPF6”或“LiAsF6”)中迁移较快,原因是___ 。
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。LiCl·3H2O属正交晶系(长方体形)。晶胞参数为0.72nm、1.0nm、0.56nm。如图为沿x轴投影的晶胞中所有Cl原子的分布图和原子分数坐标。据此推断该晶胞中Cl原子的数目为___ 。LiCl·3H2O的摩尔质量为Mg·mol-1,设NA为阿伏加 德罗常数的值,则LiCl·3H2O晶体的密度为___ g·cm-3(列出计算表达式)。
(1)Fe的价层电子排布式为
(2)Li、F、P、As四种元素的电负性由大到小的顺序为
(3)乙二醇(HOCH2CH2OH)的相对分子质量与丙醇(CH3CH2CH2OH)相近,但沸点高出100℃,原因是
(4)电池工作时,Li+沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出)。电解质LiPF6或LiAsF6的阴离子结构如图乙所示(X=P、As)。

①聚乙二醇分子中,碳、氧的杂化类型分别是
②从化学键角度看,Li+迁移过程发生
③PF6中P的配位数为
④相同条件,Li+在
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。LiCl·3H2O属正交晶系(长方体形)。晶胞参数为0.72nm、1.0nm、0.56nm。如图为沿x轴投影的晶胞中所有Cl原子的分布图和原子分数坐标。据此推断该晶胞中Cl原子的数目为

您最近一年使用:0次
2020-03-13更新
|
293次组卷
|
2卷引用:江西省上饶市2020届高三5月第三次模拟考试理综化学试题



