22-23高三上·江苏连云港·期中
1 . 转化 的方法主要有电催化、热还原等。
的方法主要有电催化、热还原等。
(1) 电催化制CO。在电解过程中向电解质中加入离子导体(
电催化制CO。在电解过程中向电解质中加入离子导体( )可以提高CO的选择性(CO是指
)可以提高CO的选择性(CO是指 转化生成CO的百分比,下同)。
转化生成CO的百分比,下同)。
①离子导体M中含有H、B、C、N、F等元素,其中B、C、N、F四种元素的第一电离能由小到大的顺序为_______ 。 的空间构型是
的空间构型是_______ 。
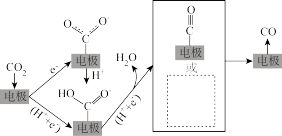
②电催化还原 制CO的示意图如下图所示。请在虚线框中画出还有可能得到的中间体的结构示意图
制CO的示意图如下图所示。请在虚线框中画出还有可能得到的中间体的结构示意图_______ 。
(2) 热还原制
热还原制 和CO。在常压、
和CO。在常压、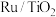 催化下,
催化下, 和
和 混和气体(体积比1:4)进行反应,测得
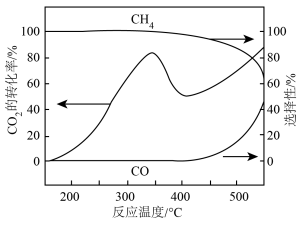
混和气体(体积比1:4)进行反应,测得 转化率、
转化率、 和CO的选择性随温度变化如图所示。
和CO的选择性随温度变化如图所示。
反应I:

反应II:

①400℃后,随温度升高 转化率不断上升的原因是
转化率不断上升的原因是_______ 。
②反应II中 和
和 在
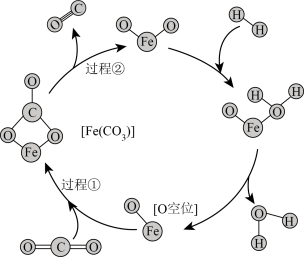
在 (存在O空位)催化剂的作用下,可以提高CO的选择性,反应机理如图所示。从电负性的角度,过程①和②能发生的原因是
(存在O空位)催化剂的作用下,可以提高CO的选择性,反应机理如图所示。从电负性的角度,过程①和②能发生的原因是_______ 。
 的方法主要有电催化、热还原等。
的方法主要有电催化、热还原等。(1)
 电催化制CO。在电解过程中向电解质中加入离子导体(
电催化制CO。在电解过程中向电解质中加入离子导体( )可以提高CO的选择性(CO是指
)可以提高CO的选择性(CO是指 转化生成CO的百分比,下同)。
转化生成CO的百分比,下同)。①离子导体M中含有H、B、C、N、F等元素,其中B、C、N、F四种元素的第一电离能由小到大的顺序为
 的空间构型是
的空间构型是②电催化还原
 制CO的示意图如下图所示。请在虚线框中画出还有可能得到的中间体的结构示意图
制CO的示意图如下图所示。请在虚线框中画出还有可能得到的中间体的结构示意图
(2)
 热还原制
热还原制 和CO。在常压、
和CO。在常压、 催化下,
催化下, 和
和 混和气体(体积比1:4)进行反应,测得
混和气体(体积比1:4)进行反应,测得 转化率、
转化率、 和CO的选择性随温度变化如图所示。
和CO的选择性随温度变化如图所示。
反应I:


反应II:


①400℃后,随温度升高
 转化率不断上升的原因是
转化率不断上升的原因是②反应II中
 和
和 在
在 (存在O空位)催化剂的作用下,可以提高CO的选择性,反应机理如图所示。从电负性的角度,过程①和②能发生的原因是
(存在O空位)催化剂的作用下,可以提高CO的选择性,反应机理如图所示。从电负性的角度,过程①和②能发生的原因是
您最近一年使用:0次
解题方法
2 . (1)Fe基态原子核外电子排布式为_____________________ 。
(2)H、N、O的电负性从小到大的顺序是___________________ 。
(3)与 互为等电子体的一种分子为
互为等电子体的一种分子为______________ (填化学式)。
氨基(-NH2)中氮原子的杂化类型为_________________ 。
(4)1mol乙酸分子中含有σ键的数目为____________________ 。
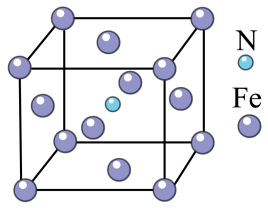
(5)Fe与N形成的某化合物晶胞如图所示,则该晶体的化学式为_______________ 。
(2)H、N、O的电负性从小到大的顺序是
(3)与
 互为等电子体的一种分子为
互为等电子体的一种分子为氨基(-NH2)中氮原子的杂化类型为
(4)1mol乙酸分子中含有σ键的数目为
(5)Fe与N形成的某化合物晶胞如图所示,则该晶体的化学式为

您最近一年使用:0次
3 . 物质结构与性质》从原子、分子水平上帮助我们认识物质构成的规律:以微粒之间不同的作用力为线索,研究不同类型物质的有关性质:从物质结构决定性质的视角预测物质的有关性质。
(1)下列说法正确的是_______ (填序号)。
A.元素电负性由大到小的顺序为O>N>C
B.一个乙烯分子含2个π键和4个σ键
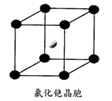
C.氯化钠和氯化铯晶体中氯离子的配位数相同
D.第一电离能的大小为Al>Mg>Na
(2)根据等电子体原理,羰基硫(OCS)分子的结构式为_______ ;光气(COCl2)各原子最外层都满 足8电子稳定结构,则光气分子的空间构型为_______ (用文字描述);
(3)Cu 2+基态的电子排布式为_______ ;向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中会析出深蓝色的[Cu(NH3)4]SO4晶体,硫酸根离子中硫原子的杂化方式为_______ ;不考虑空间构型,其内界结构可用示意图表示为_______ 。
(1)下列说法正确的是

A.元素电负性由大到小的顺序为O>N>C
B.一个乙烯分子含2个π键和4个σ键
C.氯化钠和氯化铯晶体中氯离子的配位数相同
D.第一电离能的大小为Al>Mg>Na
(2)根据等电子体原理,羰基硫(OCS)分子的结构式为
(3)Cu 2+基态的电子排布式为
您最近一年使用:0次



