名校
解题方法
1 . 据媒体报道,法国一家公司Tiamat日前研发出比当前广泛使用的锂电池成本更低、寿命更长、充电速度更快的钠离子电池,预计从2020年开始实现工业生产。该电池的负极材料为Na2Co2TeO6(制备原料为Na2CO3、Co3O4和TeO2),电解液为NaClO4的碳酸丙烯酯溶液。回答下列问题:
(1)Co 属于元素周期表中___________ 区元素,其基态原子的价电子排布式为___________ 。
(2)基态Na原子中,核外电子占据的原子轨道总数为___________ ,最高能层电子云轮廓图形状为___________
(3)结合题中信息判断:C、O、Cl的电负性由小到大的顺序为___________ (用元素符号表示)。
(4) 的几何构型为
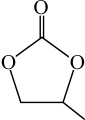
的几何构型为___________ ;碳酸丙烯酯的结构简式如图所示,则其中碳原子的杂化轨道类型为___________ ,1mol碳酸丙烯酯中 键的数目为
键的数目为___________ 。
(5)[Co(H2O)6]3+的几何构型为正八面体形,配体是___________ ,该配离子包含的作用力为___________ (填选项字母)。
A.离子键 B.金属键 C.配位键 D.氢键 E.极性键
(1)Co 属于元素周期表中
(2)基态Na原子中,核外电子占据的原子轨道总数为
(3)结合题中信息判断:C、O、Cl的电负性由小到大的顺序为
(4)
 的几何构型为
的几何构型为 键的数目为
键的数目为
(5)[Co(H2O)6]3+的几何构型为正八面体形,配体是
A.离子键 B.金属键 C.配位键 D.氢键 E.极性键
您最近一年使用:0次
2 . 下表是元素周期表的一部分,其中的字母编号代表对应的元素。试回答问题:
(1)元素⑦的原子结构示意图为_______ ,元素⑨价电子的轨道表示式为 _______ 。
(2)元素④基态原子核外共有_______ 种不同运动状态的电子,未成对电子数共有_______ 个。
(3)元素③的最简单氢化物分子的空间构型为_______ ,该氢化物含有_______ (填“极性”或“非极性”)键。
(4)③④⑤三种元素的原子电负性由小到大的顺序是_______ (用元素符号表示)。
(5)⑤⑥⑧三种元素的原子半径由大到小的顺序是_______ (用元素符号表示)。
(6)由元素⑩形成的1mol晶体中,含有的共价键为_______ mol。
| ① | ② | ③ | ④ | ⑤ | |||||||||||||
| ⑥ | ⑦ | ⑩ | ⑧ | ||||||||||||||
| ⑨ | |||||||||||||||||
(2)元素④基态原子核外共有
(3)元素③的最简单氢化物分子的空间构型为
(4)③④⑤三种元素的原子电负性由小到大的顺序是
(5)⑤⑥⑧三种元素的原子半径由大到小的顺序是
(6)由元素⑩形成的1mol晶体中,含有的共价键为
您最近一年使用:0次
3 . 下列曲线表示卤族元素某种性质随核电荷数递增的变化趋势,其中正确的是
A.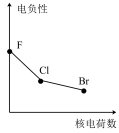 | B.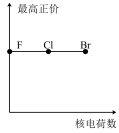 | C.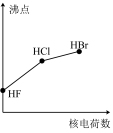 | D.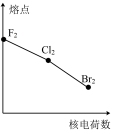 |
您最近一年使用:0次
2022-08-25更新
|
538次组卷
|
39卷引用:福建省莆田第一中学2020-2021学年高二下学期期中考试化学试题
福建省莆田第一中学2020-2021学年高二下学期期中考试化学试题【全国百强校】福建省莆田第一中学2018-2019学年高二下学期期中考试化学试题(已下线)专题4.1.4 卤族元素(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)2014-2015学年浙江省台州中学高二下第一次统练化学试卷2015-2016学年山西省大同一中高二下3月月考化学试卷2015-2016学年山西大学附中高二5月模块诊断化学试卷2016-2017学年山东省滨州市高二下学期第一次阶段性测试化学试卷安徽省淮北市第一中学2016-2017学年高二下学期期中考试化学试题山西省临汾第一中学等五校2017-2018学年高二上学期期末联考化学试题山西省大同市第三中学2017-2018学年高二下学期4月月考化学试题吉林省延边市第二中学2017-2018学年高二下学期第一次月考化学试题山东师范大学附属中学2017-2018学年高二下学期期中考试(理)化学试题山东省师范大学附属中学2017-2018学年高二下学期第七次学分认定考试(期中)(理)化学试题【全国百强校】山西省大同市第一中学2017-2018学年高二5月月考化学试题【全国百强校】天津市第一中学2017-2018学年高一下学期期中考试化学试题【全国校级联考】新疆昌吉市教育共同体四校2017-2018学年高二下学期期末联考化学试题宁夏回族自治区银川市长庆高级中学2018-2019学年高二下学期第二次月考化学试题新疆石河子第二中学2018-2019学年高二下学期期末考试化学试题宁夏银川一中2018-2019学年高二下学期期末考试化学试题河南省洛阳市2019-2020学年高二上学期期末考试化学试题四川省眉山市2018-2019学年高一下学期期末教学质量检测化学试题江苏省如东高级中学2019-2020学年高一下学期第二次阶段测试化学试题北京市朝阳区2020届高三5月适应性模拟化学试卷陕西省西安市西安高新第一中学2018-2019学年高二下学期期末考试化学试题人教版(2019)高一必修第一册 第四章 物质结构 元素周期律 章末综合检测卷江苏省东台创新高级中学2019-2020学年高二下学期4月份月检测化学试题山东潍坊高密一中2020-2021学年高二上学期12月化学月考试题甘肃省张掖市第二中学 2021-2022学年高一下学期3月月考化学试题陕西省宝鸡市长岭中学2021-2022学年高二下学期期中考试化学试题专题2 原子结构与元素性质 第二单元 元素性质的递变规律 第2课时 元素第一电离能和电负性的周期性变化山东师范大学附属中学2021-2022学年高一下学期第一次月考化学试题江苏省盐城市田家炳中学2021-2022学年高二下学期期中考试化学试题浙江省浦江中学、长兴中学、余杭高中2021-2022学年高二下学期三校联考(3月)化学试题新疆伊犁州新源县2021-2022学年高二下学期期末考试化学试题安徽省 淮北师范大学附属实验中学2022-2023学年高二下学期第一次月考化学试题湖北省武汉重点中学5G联合体2022-2023学年高二下学期期中考试化学试题2.2.2元素第一电离能和电负性的周期性变化 课后北京市中关村中学2023-2024学年高三上学期开学考试化学试卷 江苏省无锡市匡园双语学校2022-2023学年高二下学期第一次月考化学试卷
4 . 叶绿素是绿色植物进行光合作用所必需的催化剂,其结构如图所示。

(1)C、N、O三种元素电负性由大到小顺序是_______ 。
(2)MgCO3的热分解温度_______ (填“高于”或“低于”)CaCO3。
(3)叶绿素中,C原子杂化类型是_______ ,1mol该分子所含配位键的数目为_______ 个。
(4)叶绿素中存在的化学键有_______ (填字母)。
A.离子键B.极性键C.非极性键D.配位键E.氢键F.金属键
(5)多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成 键可用
键可用 符号表示,其中
符号表示,其中 代表参与形成的大
代表参与形成的大 键原子数,
键原子数, 代表参与形成的大
代表参与形成的大 键电子数(如苯分子中的大
键电子数(如苯分子中的大 键可表示为
键可表示为 )。吡咯(
)。吡咯( )中大
)中大 键可表示为
键可表示为_______ 。3-二氢吡咯( )中σ键π键的数目之比
)中σ键π键的数目之比_______ 。

(1)C、N、O三种元素电负性由大到小顺序是
(2)MgCO3的热分解温度
(3)叶绿素中,C原子杂化类型是
(4)叶绿素中存在的化学键有
A.离子键B.极性键C.非极性键D.配位键E.氢键F.金属键
(5)多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成
 键可用
键可用 符号表示,其中
符号表示,其中 代表参与形成的大
代表参与形成的大 键原子数,
键原子数, 代表参与形成的大
代表参与形成的大 键电子数(如苯分子中的大
键电子数(如苯分子中的大 键可表示为
键可表示为 )。吡咯(
)。吡咯( )中大
)中大 键可表示为
键可表示为 )中σ键π键的数目之比
)中σ键π键的数目之比
您最近一年使用:0次
名校
5 . 短周期元素W、X、Y、Z的原子序数依次增大,其中基态W原子的s能级电子总数是p能级电子总数的2倍,Y与W同主族,X的最简单氢化物的水溶液呈碱性,基态Z原子的核外电子中只有一个未成对电子。下列说法错误的是
| A.电负性:Z>W>Y | B.最简单氢化物的沸点:X>W>Y |
| C.原子半径:Y>W>X | D.Z的单质具有强氧化性 |
您最近一年使用:0次
名校
6 . 近日,我国研究人员利用硫氰酸甲基铵{[CH3NH3]+[SCN]-}气相辅助生长技术,成功制得稳定的钙钛矿型甲脒铅碘(FAPbI3)。请回答下列问题:
(1)基态S原子的价电子排布图为___________ 。
(2)甲脒(FA)的结构简式为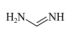
①其组成元素的电负性由小到大的排序为___________ ,其中碳原子的杂化方式为___________ 。
②甲脒比丙烷的熔点更高的原因是___________ 。
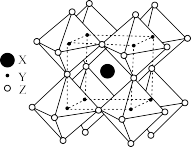
(3)FAPbI3的晶体结构单元如图所示,图中Y表示Pb,位于八面体中心,则甲脒的碘配位数为___________ 。
(1)基态S原子的价电子排布图为
(2)甲脒(FA)的结构简式为

①其组成元素的电负性由小到大的排序为
②甲脒比丙烷的熔点更高的原因是
(3)FAPbI3的晶体结构单元如图所示,图中Y表示Pb,位于八面体中心,则甲脒的碘配位数为

您最近一年使用:0次
2021-10-13更新
|
599次组卷
|
5卷引用:福建省宁化第一中学2021-2022学年高三上学期第二次阶段考试化学试题
福建省宁化第一中学2021-2022学年高三上学期第二次阶段考试化学试题天津市西青区杨柳青第一中学2021--2022 学年高三上学期第一次阶段检测化学试题天津市五校2023届高三一模联考化学试题(已下线)第19讲元素周期律与元素周期表(已下线)考点18 元素周期律与元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
解题方法
7 . 我国科研工作者最近发现并制备了一系列主要由C、P、I、Se等元素组成的导电材料。回答下列问题:
(1)基态硒原子的价电子排布图(轨道表示式)为___ ;基态P原子占据最高能级的电子云轮廓图为___ 。
(2)PF3中F—P—F键角___ PH3中H—P—H键角。(填大于、小于或等于)
(3)纯净的磷酸粘度极大,随温度升高粘度迅速下降,原因是___ ;熔融状态的磷酸导电性很好,这是由于在纯磷酸中存在如图质子交换导电机理:

由此可以推知纯磷酸液体中存在的导电微粒是H2PO 和
和___ 。
(4)黑磷是磷的一种稳定的同素异形体,黑磷具有正交晶系的晶体结构(图A)。黑磷烯是二维的单层黑磷(图B),黑磷烯与石墨烯结构相似,P的配位数为3。与石墨烯相比,黑磷烯具有半导体性质,更适合于制作电子器件。已知黑磷结构中只有一种等效的三配位P,所有P原子的成键环境一样。
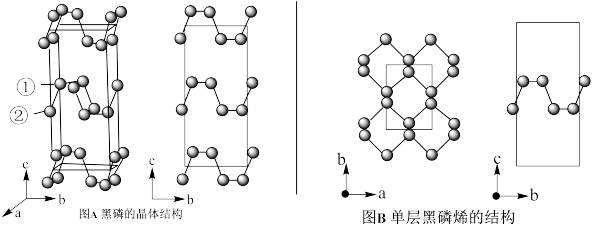
①黑磷中P原子杂化类型是___ 。
②黑磷的晶胞中含有__ 个P原子。
(1)基态硒原子的价电子排布图(轨道表示式)为
(2)PF3中F—P—F键角
(3)纯净的磷酸粘度极大,随温度升高粘度迅速下降,原因是

由此可以推知纯磷酸液体中存在的导电微粒是H2PO
 和
和(4)黑磷是磷的一种稳定的同素异形体,黑磷具有正交晶系的晶体结构(图A)。黑磷烯是二维的单层黑磷(图B),黑磷烯与石墨烯结构相似,P的配位数为3。与石墨烯相比,黑磷烯具有半导体性质,更适合于制作电子器件。已知黑磷结构中只有一种等效的三配位P,所有P原子的成键环境一样。

①黑磷中P原子杂化类型是
②黑磷的晶胞中含有
您最近一年使用:0次
解题方法
8 . 与石墨结构相似的六方氮化硼(BN)晶体在高温高压下可以转化为立方氮化硼(BN),立方氮化硼的结构与金刚石相似,硬度与金刚石相当。下列关于该物质的分析中正确的是
| A.六方氮化硼转化为立方氮化硼是物理变化 |
B.立方氮化硼(BN)中氮元素的化合价为 |
C.和 键相比, 键相比, 键的键长更长 键的键长更长 |
| D.立方氮化硼比晶体硅的熔点更高,硬度更大 |
您最近一年使用:0次
2021-09-22更新
|
538次组卷
|
4卷引用:福建泉州市第六中学2020-2021学年高二下学期期中考试化学试题
福建泉州市第六中学2020-2021学年高二下学期期中考试化学试题2021年湖北高考化学试题变式题1-103.2.2 共价晶体-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)(已下线)第3.2.2讲 共价晶体-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)
名校
解题方法
9 . 下列有关微拉性质的比较中,正确的是
A.原子半径: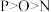 | B.最高正价: |
C.第一电离能: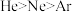 | D.电负性: |
您最近一年使用:0次
2021-09-22更新
|
465次组卷
|
5卷引用:福建泉州市第六中学2020-2021学年高二下学期期中考试化学试题
福建泉州市第六中学2020-2021学年高二下学期期中考试化学试题(已下线)第1章 原子结构与性质(章末检测)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)陕西省宝鸡市金台区2021-2022学年高二下学期期中考试化学试题吉林省吉林市田家炳高级中学2022-2023学年高二上学期期末线上考试化学试题四川省南充市阆中中学校2023-2024学年高二下学期3月月考化学试卷
名校
10 . 在以离子键为主的离子化合物中,形成离子键的两种元素电负性差距越小,则含有共价键的成分越高;下列各对原子形成的化学键中含有共价键成分最少的是
| A.Li F | B.Na F | C.Na Cl | D.Mg O |
您最近一年使用:0次
2021-09-22更新
|
139次组卷
|
2卷引用:福建省泉州市培元中学2020-2021学年高二下学期期中考试化学试题



