名校
1 . 下列说法中不正确的是
A. 键比 键比 键重叠程度大,形成的共价键通常更牢固 键重叠程度大,形成的共价键通常更牢固 |
B.两个原子之间形成共价键时,最多有一个 键 键 |
C.气体单质中,一定有 键,可能有 键,可能有 键 键 |
D. 分子中有一个 分子中有一个 键,2个 键,2个 键 键 |
您最近一年使用:0次
2023-04-08更新
|
234次组卷
|
87卷引用:山东省枣庄市第三中学2019-2020学年高二下学期3月网上测试化学试题
山东省枣庄市第三中学2019-2020学年高二下学期3月网上测试化学试题(已下线)2010-2011学年福建省师大附中高二下学期期中考试化学试卷(已下线)2011-2012学年新疆农七师高级中学高二下学期期末考试试化学试卷(已下线)2012-2013学年福建三明泰宁一中高二下第一次阶段考试化学试卷(已下线)2012-2013学年辽宁葫芦岛第一高级中学高二下学期期中考试化学试卷(已下线)2012-2013学年河北省衡水市第十四中学高二下学期期末考试化学试卷(已下线)2012-2013学年湖北省荆州市监利县柘木中学高二下第二次月考化学卷2015-2016学年河北省邢台一中高二上12月月考化学试卷2015-2016学年四川省成都市新都一中高二下4月月考化学试卷福建省福州市八县(市)协作校2016-2017学年高二下学期期中考试化学试题福建省晋江市季延中学2017-2018学年高二上学期期中考试(理)化学试题高中化学人教版 选修三 第2章 分子结构与性质 共价键宁夏吴忠市高二人教版选修3第2章 分子结构与性质综合练习2河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:2.1 第1课时黑龙江省齐齐哈尔市第八中学2017-2018学年高二3月月考化学试题云南省香格里拉县一中2018-2019学年高二上学期期中考试化学试题贵州省普定县一中2018-2019学年高二上学期期中考试化学试题贵州省习水县一中2018-2019学年高二上学期12月份月考化学试题贵州省毕节市黔西县第一中学2018-2019学年高二上学期12月份考试化学试题【全国百强校】河北省衡水市武邑中学2018-2019学年高二12月月考化学试题云南省普洱市景东县第一中学2018-2019学年高二上学期期末考试化学试题云南省玉溪市江川区第二中学2018-2019学年高二上学期期末考试化学试题【全国百强校】山西省实验中学2018-2019学年高二下学期第一次月考化学试题【全国百强校】内蒙古自治区赤峰市第二中学2018-2019学年高二下学期4月月考化学试题河北省唐山市开滦第二中学2018-2019学年高二下学期期中考试化学试题福建省泉州市泉港区第一中学2018-2019学年高二下学期第二次月考化学试题广西蒙山县第一中学2017-2018学年高二下学期期末考试化学试题云南省通海三中2018-2019学年高二下学期6月份考试化学试题吉林省汪清县第六中学2018-2019学年高二6月月考化学试题新疆乌鲁木齐市第四中学2018-2019学年高二下学期期末考试化学试题云南省丘北县第二中学2018-2019学年高二下学期6月份考试化学试题广西壮族自治区蒙山县第一中学2019-2020学年高二下学期期末考试化学试题广西蒙山一中2018-2019学年高二下学期期末考试化学试题(已下线)专题11.2 分子结构与性质(讲)-《2020年高考一轮复习讲练测》云南省玉溪市新平三中2019-2020学年高二上学期12月份月考化学试题江苏省徐州一中2019-2020学年高二上学期期末调研测试化学试题云南省丽江市永胜县第二中学2019—2020学年高二上学期期末考试化学试题河南省洛阳市2019-2020学年高二上学期期末考试化学试题贵州省岑巩县第二中学2019-2020学年高二上学期期末考试化学试题宁夏回族自治区吴忠市吴忠中学2020年高二化学人教版选修3《物质结构与性质》综合测试河北省正定中学2019-2020学年高二3月线上月考化学试题湖北省武汉市武昌区水果湖高中 2019-2020 学年高二下学期期中考试化学试题陕西省宝鸡市渭滨区2018-2019学年高二下学期期末考试化学试题吉林省长春市第二十九中学2019-2020学年高二下学期线上检测化学试题山东省泰安市2020年高二下学期化学期中考试(鲁科版)山西省太原市阳曲县第一中学2019-2020学年高二5月复学检测化学试题河北省沧州市任丘市第一中学2019-2020学年高二6月月考化学试题江苏省东台创新高级中学2019-2020学年高二下学期4月份月检测化学试题新疆生产建设兵团第四师第一中学2019-2020学年高二下学期期中考试化学试题(已下线)练习19 共价键-2020-2021学年【补习教材·寒假作业】高二化学(人教版)黑龙江省哈尔滨市第三十二中学2019-2020学年高二下学期期中考试化学试题(人教版2019)选择性必修2 第二章 分子结构与性质 第一节 共价键 第1课时 共价键鲁科版2019选择性必修2第2章 微粒间相互作用与物质性质 第1节 共价键模型 第1课时 共价键的形成(鲁科版2019)选择性必修2 第2章 微粒间相互作用与物质性质 第1节 共价键模型高二选择性必修2(人教版2019)第二章 分子结构与性质 第一节综合训练(已下线)第2章 微粒间相互作用与物质性质(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版2019选择性必修2)(已下线)模块同步卷11 综合检测卷(基础卷)-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)(已下线)2.1 共价键(A级基础练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)吉林省长春市第二十九中学2020-2021学年高二下学期第一学程考试化学试题新疆维吾尔自治区乌鲁木齐市第四中学2020-2021学年高二年级下学期期中考试化学试题黑龙江省牡丹江市海林市朝鲜族中学2020-2021学年高二下学期4月份月考化学试题甘肃省兰州市第一中学2020-2021学年高二下学期期中考试化学试题吉林省辽源市田家炳高级中学2020-2021学年高二下学期期中化学试题黑龙江省齐齐哈尔市第八中学校2020-2021学年高二下学期期中考试化学试题江苏省南通市如皋中学2020-2021学年高一下学期第二次阶段考试化学试题吉林省乾安县第七中学2020-2021学年高二下学期第六次质量检测化学试题福建省仙游县枫亭中学2020-2021学年高二下学期期中考试化学试题辽宁省鞍山市2020-2021学年高二下学期期末考试化学试题江西省九江市柴桑区第一中学2020-2021学年高二下学期5月月考化学试题(已下线)课时55 分子结构与性质-2022年高考化学一轮复习小题多维练(全国通用)天津市蓟州区燕山中学2021-2022学年高三上学期第一次月考化学试题(已下线)2.1.1 共价键的类型-σ键和π键-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)(已下线)2.1.1 共价键的类型——σ键和π键(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)新疆乌鲁木齐市第四中学2021-2022学年高二下学期期中考试化学试题浙江省台州市三门启超中学等两校2021-2022学年高二下学期期中联考化学试题海南省儋州川绵中学2021-2022学年高二下学期期中考试化学试题内蒙古赤峰二中2021-2022学年高二下学期第二次月考化学试题专题3 微粒间作用力与物质性质 第三单元 共价键共价晶体 第1课时 共价键的形成及类型湖南省长沙市长郡梅溪湖中学2021-2022学年高二下学期入学考试化学试题贵州省凯里学院附属中学2021-2022学年高二下学期3月月考化学试题新疆乌鲁木齐市第101中学2021-2022学年高二下学期期末考试化学试题吉林省吉林市田家炳高级中学2022-2023学年高二上学期期末线上考试化学试题湖北省十堰市普通高中协作体2022-2023学年高二下学期3月月考化学试题广东省惠州市博罗县博师高级中学2022-2023学年高二下学期3月考试化学试题宁夏青铜峡市宁朔中学2022-2023学年高二下学期期中考试化学试题3.3.1共价键的形成和类型 课中湖北省武汉西藏中学2023-2024学年高二下学期4月月考化学试题
2 . 已知原子数和价电子数相同的离子或分子空间结构相似,如 、
、 都是平面三角形结构。那么下列分子或离子中与
都是平面三角形结构。那么下列分子或离子中与 有相似空间结构的是
有相似空间结构的是
 、
、 都是平面三角形结构。那么下列分子或离子中与
都是平面三角形结构。那么下列分子或离子中与 有相似空间结构的是
有相似空间结构的是A. | B. | C. | D. |
您最近一年使用:0次
2022-08-28更新
|
326次组卷
|
3卷引用:山东省枣庄市第三中学2019-2020学年高二下学期3月网上测试化学试题
名校
3 . 前四周期元素X、Y、Z、W核电荷数依次增大,核电荷数之和为58;Y原子的M层p轨道有3个未成对电子;Z与Y同周期,且在该周期中电负性最大;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:2。
(1)写出Z元素在元素周期表中的位置:___________ 。
(2) 与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是
与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是___________  写分子式
写分子式 。
。
(3) 的最高价氧化物的水化物的化学式为
的最高价氧化物的水化物的化学式为___________ ;
(4) 单质
单质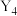 与
与 在一定条件下恰好完全反应生成
在一定条件下恰好完全反应生成 化合物C,一个C分子中所含有的σ键数目为
化合物C,一个C分子中所含有的σ键数目为___________ ;
(5)含W元素的最高化合价的含氧酸根离子是___________ ,该含氧酸根离子在分析化学中有重要作用,在酸性条件下该含氧酸根离子可将 氧化成
氧化成 ,请写出该反应的离子方程式
,请写出该反应的离子方程式___________ 。
(1)写出Z元素在元素周期表中的位置:
(2)
 与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是
与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是 写分子式
写分子式 。
。(3)
 的最高价氧化物的水化物的化学式为
的最高价氧化物的水化物的化学式为(4)
 单质
单质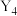 与
与 在一定条件下恰好完全反应生成
在一定条件下恰好完全反应生成 化合物C,一个C分子中所含有的σ键数目为
化合物C,一个C分子中所含有的σ键数目为(5)含W元素的最高化合价的含氧酸根离子是
 氧化成
氧化成 ,请写出该反应的离子方程式
,请写出该反应的离子方程式
您最近一年使用:0次
2021-04-21更新
|
556次组卷
|
5卷引用:山东省滕州市第一中学2019-2020学年高二下学期第二次月考化学试题
解题方法
4 . 人们发现金星大气层有一种称为羰基硫(COS)的分子,其结构与CO2类似,羰基硫是一种与生命密切相关的物质,下列推测不正确的是( )
| A.COS是共价化合物 |
| B.COS为直线形分子 |
C.COS的电子式为: |
| D.COS中所有原子都满足8电子稳定结构 |
您最近一年使用:0次
2020-09-24更新
|
140次组卷
|
2卷引用:鲁科版(2019)高一必修第二册 第2章 化学键 反应规律 第一节 化学键与物质构成 教材帮
5 . 根据等电子原理,由短周期元素组成的粒子,只要其电子总数相同,均可互称为等电子体,等电子体之间结构相似、物理性质也相近,以下各组粒能互称为等电子体的是
A. 和 和 | B. 和 和 | C. 和 和 | D. 和 和 |
您最近一年使用:0次
名校
解题方法
6 . 下列说法不正确的是
| A.气体单质中一定有σ键,可能有π键 |
| B.每一能层的能级总是从s能级开始,且能级数等于该能层序数 |
| C.电子从激发态跃迁到基态时将释放能量,光是电子释放能量的重要形式之一 |
| D.同主族元素的第一电离能随核电荷数的递增依次增大 |
您最近一年使用:0次
名校
解题方法
7 . 下表各组数据中,一定有错误的是
| A | 金刚石硬度:10 | 碳化硅硬度:9 | 晶体硅硬度:7 |
| B | 溴化钾熔点:735℃ | 氯化钠熔点:801℃ | 氧化镁熔点:2800℃ |
| C | 邻羟基苯甲醛沸点:250℃ | 对羟基苯甲醛沸点196℃ | 对甲基苯甲醛沸点:204℃ |
| D | 三氟化硼的键角:120° | 氨分子的键角:120° | 四氯化碳的键角:109.5° |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-07-27更新
|
153次组卷
|
3卷引用:山东省枣庄市2019-2020学年高二下学期期末考试化学试题
名校
解题方法
8 . 下列说法中正确的是( )
| A.NO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8电子稳定结构 |
| B.P4和CH4都是正四面体型分子且键角都为109.5° |
C.NH4+的电子式为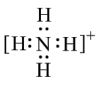 ,离子呈平面正方形结构 ,离子呈平面正方形结构 |
| D.NH3分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强 |
您最近一年使用:0次
2020-06-05更新
|
1320次组卷
|
22卷引用:山东省枣庄市第三中学2019-2020学年高二下学期3月网上测试化学试题
山东省枣庄市第三中学2019-2020学年高二下学期3月网上测试化学试题(已下线)2014届四川省富顺一中高二上学期第一次月考化学试卷2014-2015山西省太原市五中高二4月阶段形成检测化学试卷河南省兰考县第二高级中学2016-2017学年高二下学期期末考试化学试题四川省德阳市第五中学2018-2019学年高二上学期10月月考化学试题贵州省遵义市正安县第一中学2018-2019学年高二上学期期中考试化学试题云南省昭通水田新区中学2018-2019学年高二上学期12月月考化学试题贵州省黄平县且兰高级中学2018-2019学年高二上学期12月份考试化学试题吉林省公主岭市范家屯镇第一中学2018-2019学年高二下学期期中考试化学试题贵州省岑巩县第四中学2019-2020学年高二上学期期末考试化学试题河北省正定中学2019-2020学年高二3月线上月考化学试题辽宁省朝阳市凌源市实验中学2019-2020学年高二下学期4月份月考化学试题山西省太原市阳曲县第一中学2019-2020学年高二5月复学检测化学试题新疆昌吉回族自治州第二中学2019-2020学年高二下学期期中考试化学试题(人教版2019)选择性必修2 第二章 分子结构与性质 第二节 分子的空间结构(鲁科版2019)选择性必修2 第2章 微粒间相互作用与物质性质 第2节 共价键与分子的空间结构(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练湖北省武汉市江夏实验高中2020-2021学年高二下学期3月月考化学试题甘肃省武威第十八中学2020-2021学年高二下学期期中考试化学试题湖北省华中师范大学第一附属中学2020-2021学年高一下学期期末考试化学试题湖南省邵阳市第二中学2021-2022学年高二下学期入学考试化学试题山西省临汾市尧都区山西师范大学实验中学2021-2022学年高二下学期第一次月考化学考试试题
名校
解题方法
9 . 下列对一些实验事实的理论解释正确的是( )
| 选项 | 实验事实 | 理论解释 |
| A | 碘单质在CCl4中溶解度比在水中大 | CCl4和I2都是非极性分子,而H2O是极性分子 |
| B | CO2为直线形分子 | CO2分子中C═O是极性键 |
| C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是共价晶体 |
| D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-04-07更新
|
149次组卷
|
10卷引用:山东省枣庄市第三中学2019-2020学年高二下学期3月网上测试化学试题
山东省枣庄市第三中学2019-2020学年高二下学期3月网上测试化学试题甘肃省兰州市第一中学2017-2018学年高二下学期期中考试化学试题【全国百强校】新疆兵团第二师华山中学2017-2018学年高二下学期期末考试化学试题安徽省淮北师范大学附属实验中学2018-2019学年高二下学期第二次月考化学试题内蒙古包头市包钢第四中学2018-2019学年高二下学期4月月考化学试题辽宁省丹东市第四中学2019-2020学年高二 4 月线上月考化学试题安徽省滁州市明光中学2019-2020学年高二下学期开学考试化学试题安徽省亳州市涡阳县第九中学2019-2020学年高二7月月考化学试题河南省漯河市临颍县南街高中2020-2021学年高二上学期期中考试化学试题四川省南充高级中学2020-2021学年高二下学期入学考试化学试题
名校
解题方法
10 . As2O3(砒霜)是两性氧化物(分子结构如图所示),溶于盐酸生成 AsCl3,AsCl3用 LiAlH4还原生成 AlH3。下列说法正确的是( )


| A.As2O3分子中 As 原子的杂化方式为 sp |
| B.LiAlH4为共价化合物 |
| C.AsCl3空间构型为平面正三角形 |
| D.AlH3分子键角大于 109.5° |
您最近一年使用:0次
2020-04-06更新
|
176次组卷
|
4卷引用:山东省滕州市第一中学2019-2020学年高二下学期第二次月考化学试题



