1 . 下列有关甲醛(HCHO)分子的说法正确的是
| A.其中C原子采取sp即杂化 |
| B.是三角锥形 |
| C.其中H-C-O键的键角大于H-C-H键的键角 |
| D.是手性分子 |
您最近一年使用:0次
2 . 探索 和
和 这类化合物的特征及反应机理,对处理该类化合物的污染问题具有重要意义。回答下列问题:
这类化合物的特征及反应机理,对处理该类化合物的污染问题具有重要意义。回答下列问题:
I.CO可以与 反应制备合成天然气(SNG)。涉及反应如下:
反应制备合成天然气(SNG)。涉及反应如下:
 甲烷化:
甲烷化:
水煤气变换:
(1)反应 的
的
___________  。分别在
。分别在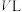 恒温密闭容器
恒温密闭容器 (恒容)、B(恒压,容积可变)中,加入
(恒容)、B(恒压,容积可变)中,加入 和
和 的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是
的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是___________ (填“A”或“B”)。
II. 可发生二聚反应生成
可发生二聚反应生成 ,化学方程式为
,化学方程式为 。该反应达到平衡后,升高温度可使体系颜色加深。
。该反应达到平衡后,升高温度可使体系颜色加深。
(2)已知该反应的正反应速率方程为v正=k正·c2(NO2),逆反应速率方程为v逆=k逆c·(N2O4),其中k正、k逆分别为正、逆反应的速率常数。如图(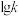 表示速率常数的对数:
表示速率常数的对数: 表示温度的倒数)所示①、②、③、④四条斜线中,
表示温度的倒数)所示①、②、③、④四条斜线中, 随
随 变化关系的是斜线③,则
变化关系的是斜线③,则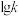 逆随
逆随 变化关系的是斜线
变化关系的是斜线___________ 。

(3)图中A、B、C、D点的纵坐标分别为 ,则
,则 温度时该反应的化学平衡常数
温度时该反应的化学平衡常数
___________  。已知
。已知 温度时,某时刻恒容密闭容器中
温度时,某时刻恒容密闭容器中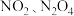 浓度均为
浓度均为 ,此时v正
,此时v正___________ v逆。(填“>”、“=”或“<”)
(4)工业上利用 溶液吸收
溶液吸收 气体,发生反应:
气体,发生反应: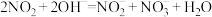 。
。 空间结构为
空间结构为___________ ,比较 与
与 的键角大小,并解释原因:
的键角大小,并解释原因:___________ 。
 和
和 这类化合物的特征及反应机理,对处理该类化合物的污染问题具有重要意义。回答下列问题:
这类化合物的特征及反应机理,对处理该类化合物的污染问题具有重要意义。回答下列问题:I.CO可以与
 反应制备合成天然气(SNG)。涉及反应如下:
反应制备合成天然气(SNG)。涉及反应如下: 甲烷化:
甲烷化:
水煤气变换:

(1)反应
 的
的
 。分别在
。分别在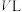 恒温密闭容器
恒温密闭容器 (恒容)、B(恒压,容积可变)中,加入
(恒容)、B(恒压,容积可变)中,加入 和
和 的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是
的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是II.
 可发生二聚反应生成
可发生二聚反应生成 ,化学方程式为
,化学方程式为 。该反应达到平衡后,升高温度可使体系颜色加深。
。该反应达到平衡后,升高温度可使体系颜色加深。(2)已知该反应的正反应速率方程为v正=k正·c2(NO2),逆反应速率方程为v逆=k逆c·(N2O4),其中k正、k逆分别为正、逆反应的速率常数。如图(
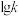 表示速率常数的对数:
表示速率常数的对数: 表示温度的倒数)所示①、②、③、④四条斜线中,
表示温度的倒数)所示①、②、③、④四条斜线中, 随
随 变化关系的是斜线③,则
变化关系的是斜线③,则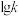 逆随
逆随 变化关系的是斜线
变化关系的是斜线
(3)图中A、B、C、D点的纵坐标分别为
 ,则
,则 温度时该反应的化学平衡常数
温度时该反应的化学平衡常数
 。已知
。已知 温度时,某时刻恒容密闭容器中
温度时,某时刻恒容密闭容器中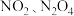 浓度均为
浓度均为 ,此时v正
,此时v正(4)工业上利用
 溶液吸收
溶液吸收 气体,发生反应:
气体,发生反应: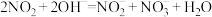 。
。 空间结构为
空间结构为 与
与 的键角大小,并解释原因:
的键角大小,并解释原因:
您最近一年使用:0次
3 . 非金属氮化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态N原子核外电子的运动状态有________ 种。羟胺(NH2OH)的水溶液呈碱性,其碱性原理与氨水相似,同浓度的氨水和羟胺两种溶液的碱性较强的是______ (填“NH2OH"或“NH3”),原因是____________ 。
(2)氟化硝酰(NO2F)可用作火箭推进剂中的氧化剂,上述所涉及元素中,电负性由大到小顺序为_______ ;第一电离能由大到小顺序为_________ 。
(3)气态N2O5的分子结构为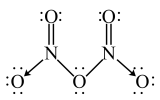 ,而固态N2O5则由
,而固态N2O5则由 与
与 构成。
构成。 的空间构型为
的空间构型为______ , 中N的杂化方式为
中N的杂化方式为________ 。
(4) 和PH3中共价键的键角比较:
和PH3中共价键的键角比较:
_______ PH3(填“>”、“<”或“=”,下同), 和
和 中共价键键角比较:
中共价键键角比较:
_____  。
。
(1)基态N原子核外电子的运动状态有
(2)氟化硝酰(NO2F)可用作火箭推进剂中的氧化剂,上述所涉及元素中,电负性由大到小顺序为
(3)气态N2O5的分子结构为
 ,而固态N2O5则由
,而固态N2O5则由 与
与 构成。
构成。 的空间构型为
的空间构型为 中N的杂化方式为
中N的杂化方式为(4)
 和PH3中共价键的键角比较:
和PH3中共价键的键角比较:
 和
和 中共价键键角比较:
中共价键键角比较:
 。
。
您最近一年使用:0次
解题方法
4 . 下列分子中,键角最小的是
A. | B. | C. | D. |
您最近一年使用:0次
名校
解题方法
5 . 氮、氟及其化合物在生产及生活中有着广泛的用途。请回答下列问题:
(1)氟磷灰石可用于制取磷肥,基态P原子有___________ 个未成对电子, 的中心P原子的杂化方式为
的中心P原子的杂化方式为___________ 。
(2)氟气可以用于制取惰性强于 的保护气
的保护气 ,也可以用于制取聚合反应的催化剂
,也可以用于制取聚合反应的催化剂 ,
, 可以作为工业制取硅单质的中间物质(
可以作为工业制取硅单质的中间物质( )的原料。
)的原料。
① 分子的空间结构为
分子的空间结构为___________ 。
②S、P、Si的第一电离能由大到小的顺序为___________ 。
(3)Na与N形成的 可用于汽车的安全气囊中,其中阴离子的空间结构为
可用于汽车的安全气囊中,其中阴离子的空间结构为___________ 。
(4)键角比较:
___________  (填“>”或“<”),其原因为
(填“>”或“<”),其原因为___________ 。
(1)氟磷灰石可用于制取磷肥,基态P原子有
 的中心P原子的杂化方式为
的中心P原子的杂化方式为(2)氟气可以用于制取惰性强于
 的保护气
的保护气 ,也可以用于制取聚合反应的催化剂
,也可以用于制取聚合反应的催化剂 ,
, 可以作为工业制取硅单质的中间物质(
可以作为工业制取硅单质的中间物质( )的原料。
)的原料。①
 分子的空间结构为
分子的空间结构为②S、P、Si的第一电离能由大到小的顺序为
(3)Na与N形成的
 可用于汽车的安全气囊中,其中阴离子的空间结构为
可用于汽车的安全气囊中,其中阴离子的空间结构为(4)键角比较:

 (填“>”或“<”),其原因为
(填“>”或“<”),其原因为
您最近一年使用:0次
名校
6 . 下列说法中,不正确 的是
A.只能有 、 、 、 、 分子,而不可能有 分子,而不可能有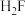 、 、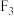 、 、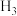 分子,这表明共价键有饱和性 分子,这表明共价键有饱和性 |
| B.电子由低能级跃迁至较高能级时,一定发生的是化学变化 |
C.键能大小: |
| D.通过原子光谱分析可以鉴定某些元素 |
您最近一年使用:0次
名校
解题方法
7 . 下列说法正确的是
A.已知 键的键能为 键的键能为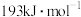 ,故 ,故 键的键能为 键的键能为 |
B. 键的键能为 键的键能为 , , 键的键能为 键的键能为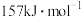 ,故 ,故 比 比 稳定 稳定 |
| C.某元素原子最外层有1个电子,它跟卤素原子相结合时,所形成的化学键一定为离子键 |
D. 、 、 、 、 三种分子的键角依次增大 三种分子的键角依次增大 |
您最近一年使用:0次
名校
解题方法
8 . 已知 。下列有关说法正确的是
。下列有关说法正确的是
 。下列有关说法正确的是
。下列有关说法正确的是A. 的电子式为 的电子式为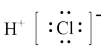 | B.I—I键的键长比 键短 键短 |
C. 分子中只有 分子中只有 键 键 | D. 的酸性比 的酸性比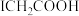 强 强 |
您最近一年使用:0次
2024-01-22更新
|
247次组卷
|
4卷引用:湖南省长沙市明德中学2023-2024学年高二上学期12月月考化学试题
名校
解题方法
9 . 下列说法正确的是

A. 的沸点(1040℃)高于 的沸点(1040℃)高于 (178℃)的沸点,主要与晶体类型有关 (178℃)的沸点,主要与晶体类型有关 |
B.血红蛋白的结构如图所示, 的配位数为4 的配位数为4 |
C.气态 分子的键角小于 分子的键角小于 离子的键角 离子的键角 |
D.吡啶( )在水中的溶解度小于苯在水中的溶解度 )在水中的溶解度小于苯在水中的溶解度 |
您最近一年使用:0次
2024-01-22更新
|
237次组卷
|
2卷引用:湖北省十堰市郧阳区第二中学2023-2024学年高二下学期三月月考化学试题
名校
解题方法
10 . 三氟化氮( )是一种新型电子材料的原料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有
)是一种新型电子材料的原料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有 、
、 和
和 ,请根据要求回答下列问题:
,请根据要求回答下列问题:
(1) 键的键能为
键的键能为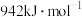 ,
, 单键的键能为
单键的键能为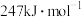 ,说明
,说明 中的
中的_____ (填“ ”或“
”或“ ”)键更稳定。
”)键更稳定。
(2) 的沸点(
的沸点( )比
)比 (
( )低的原因是
)低的原因是_____ 。
(3) 是一种无色、无臭的气体,但
是一种无色、无臭的气体,但 一旦在空气中泄漏,还是易于发现。你判断该气体泄漏时的现象是
一旦在空气中泄漏,还是易于发现。你判断该气体泄漏时的现象是_____ 。
(4) 的电离方程式为
的电离方程式为 ,
, 溶于水后形成
溶于水后形成 的结构是
的结构是_____ 。
(5)斯图杰尔和阿佩里曼成功地在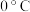 以下将氟化物从细冰末的上面通过,得到毫克量的次氟酸。次氟酸的结构是
以下将氟化物从细冰末的上面通过,得到毫克量的次氟酸。次氟酸的结构是_____ 。次氟酸分子中共价键的键角_____ (填“<”或“=”) 。
。
 )是一种新型电子材料的原料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有
)是一种新型电子材料的原料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有 、
、 和
和 ,请根据要求回答下列问题:
,请根据要求回答下列问题:(1)
 键的键能为
键的键能为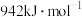 ,
, 单键的键能为
单键的键能为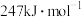 ,说明
,说明 中的
中的 ”或“
”或“ ”)键更稳定。
”)键更稳定。(2)
 的沸点(
的沸点( )比
)比 (
( )低的原因是
)低的原因是(3)
 是一种无色、无臭的气体,但
是一种无色、无臭的气体,但 一旦在空气中泄漏,还是易于发现。你判断该气体泄漏时的现象是
一旦在空气中泄漏,还是易于发现。你判断该气体泄漏时的现象是(4)
 的电离方程式为
的电离方程式为 ,
, 溶于水后形成
溶于水后形成 的结构是
的结构是(5)斯图杰尔和阿佩里曼成功地在
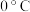 以下将氟化物从细冰末的上面通过,得到毫克量的次氟酸。次氟酸的结构是
以下将氟化物从细冰末的上面通过,得到毫克量的次氟酸。次氟酸的结构是 。
。
您最近一年使用:0次



