名校
1 . 下列说法不正确的是( )
| A.H2O的VSEPR构型和空间构型都是V形 | B.BeCl2是直线形分子 |
| C.SO3的空间构型为平面三角形 | D.SO2中S原子含1对孤电子对 |
您最近一年使用:0次
2019-08-04更新
|
126次组卷
|
2卷引用:山西省原平市范亭中学2018-2019学年高二下学期期末考试化学试题
名校
解题方法
2 . 通常把原子总数和价电子总数相同的分子或离子称为等电子体。人们发现等电子体的空间结构相同,则下列有关说法中正确的是
| A.CH4和NH4+是等电子体,键角均为60° |
| B.H3O+和PCl3是等电子体,均为三角锥形结构 |
| C.NO3﹣和CO32﹣是等电子体,都是平面三角形结构 |
| D.B3N3H6和苯是等电子体,B3N3H6分子中也存在“肩并肩”式重叠的轨道 |
您最近一年使用:0次
解题方法
3 . 下列说法中正确的是( )
| A.PCl3分子是平面三角形,中心原子磷原子是sp2杂化 |
| B.乙炔分子中的C原子是sp2杂化 |
| C.凡中心原子采取sp3杂化的分子,其VSEPR模型都是四面体形 |
| D.NH4Cl中有4种化学键 |
您最近一年使用:0次
名校
4 . 在气相中,关于BeF2和SF2的说法错误的是( )
| A.BeF2分子中,中心原子Be的价层电子对数等于2,成键电子对数也等于2 |
| B.SF2分子中,中心原子S的价层电子对数等于4,其空间排布为四面体,成键电子对数等于2,没有孤电子对 |
| C.BeF2分子的空间构型为直线形 |
| D.在气相中,BeF2是直线形而SF2是V形 |
您最近一年使用:0次
2019-06-23更新
|
79次组卷
|
6卷引用:2014-2015学年陕西省宝鸡中学高二下学期期末化学试卷A
解题方法
5 . A、B、C、D、E、F、G是前四周期的七种元素,其原子序数依次增大。A的基态原子中没有成对电子;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D及其同主族元素的氢化物沸点变化趋势如图(D的氢化物沸点最高);F是地壳中含量最高的金属元素;G与F同主族。请回答下列问题:
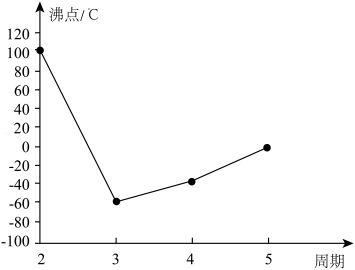
(1)写出F元素基态原子的核外电子排布式:____________ 。
(2)B、C、D三种元素电负性由大到小的顺序是____________ (用元素符号表示)。
(3)有关上述元素的下列说法,正确的是________ (填序号)。
①CA3沸点高于BA4,主要是因为前者相对分子质量较大
②配合物Ni(BD)4常温下为液态,易溶于CCl4、苯等有机溶剂,因此固态Ni(BD)4属于离子晶体
③C的氢化物的中心原子采取sp2杂化
④F单质的熔点高于E单质,是因为F单质的金属键较强
⑤比G的原子序数少1的元素第一电离能高于G
(4)CA3分子的立体构型为________ ,1 mol B2A4分子中含有________ 个σ键;

(1)写出F元素基态原子的核外电子排布式:
(2)B、C、D三种元素电负性由大到小的顺序是
(3)有关上述元素的下列说法,正确的是
①CA3沸点高于BA4,主要是因为前者相对分子质量较大
②配合物Ni(BD)4常温下为液态,易溶于CCl4、苯等有机溶剂,因此固态Ni(BD)4属于离子晶体
③C的氢化物的中心原子采取sp2杂化
④F单质的熔点高于E单质,是因为F单质的金属键较强
⑤比G的原子序数少1的元素第一电离能高于G
(4)CA3分子的立体构型为
您最近一年使用:0次
6 . 设NA为阿伏加 德罗常数的值,下列说法中正确的是
| A.标准状况下,1mol金刚石中含有的C–C键数目为4NA |
| B.1mol SiO2晶体中含有的Si–O键数目为2NA |
| C.63g HNO3,中心原子N的价层电子对中,孤电子对数为NA |
| D.常温常压下,1mol配合物[Cu(NH3)4]SO4中,含有的σ键数目为20NA |
您最近一年使用:0次
2019-06-09更新
|
301次组卷
|
2卷引用:【校级联考】河南省郑州市八校2018-2019学年高二下学期期中联考化学试题
7 . CH 、—CH3、CH
、—CH3、CH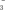 都是重要的有机反应中间体,有关它们的说法错误的是
都是重要的有机反应中间体,有关它们的说法错误的是
 、—CH3、CH
、—CH3、CH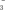 都是重要的有机反应中间体,有关它们的说法错误的是
都是重要的有机反应中间体,有关它们的说法错误的是| A.它们互为等电子体,碳原子均采取sp2杂化 |
B.CH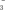 与NH3、H3O+互为等电子体,几何构型均为三角锥形 与NH3、H3O+互为等电子体,几何构型均为三角锥形 |
C.CH 中的碳原子采取sp2杂化,所有原子均共面 中的碳原子采取sp2杂化,所有原子均共面 |
D.两个—CH3或一个CH 和一个CH 和一个CH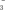 结合均可得到CH3CH3 结合均可得到CH3CH3 |
您最近一年使用:0次
名校
解题方法
8 . 关于CH4、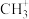 、
、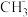 三种粒子的说法,正确的是
三种粒子的说法,正确的是
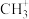 、
、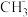 三种粒子的说法,正确的是
三种粒子的说法,正确的是 | A.C原子的杂化类型都相同 |
B.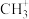 是三角锥形 是三角锥形 |
C.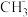 与BCl3构型相同 与BCl3构型相同 |
D.CH4与 互为等电子体 互为等电子体 |
您最近一年使用:0次
2018-07-30更新
|
980次组卷
|
2卷引用:福建省莆田第六中学2017-2018学年高二6月月考化学试题A
名校
9 . 下列说法错误 的是
| A.从CH4、NH4+、SO42-为正四面体结构,可推测PH4+、PO43-也为正四面体结构 |
| B.1mol碳化硅晶体中,平均含有4mol C—Si共价键 |
| C.水的沸点比硫化氢的高,是因为H2O分子间存在氢键,H2S分子间不能形成氢键 |
D.某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE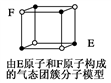 |
您最近一年使用:0次
名校
10 . 下列说法中正确的是
| A.NO2、SO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8e-稳定结构; |
| B.P4和CH4都是正四面体分子且键角都为109o28ˊ; |
| C.CO2、SO2都是直线形的分子 |
| D.CH2=CH2分子中共有五个σ键和一个π键 |
您最近一年使用:0次
2018-01-30更新
|
217次组卷
|
2卷引用:内蒙古赤峰二中2017-2018学年高二上学期期末考试化学试题



