名校
解题方法
1 . 按要求回答下列问题:
(1)A.乙烷 B.乙烯 C.乙炔 D.苯是有机化学中的代表物质,其中:
①既有 键又有
键又有 键的是
键的是_______ (填序号,下同)。
②碳碳键的键长由大到小排序是:_______ 。
③上述分子中所有原子均在同一平面是:_______ 。
(2)含硫元素的微粒有很多,例如 、
、 、
、 、
、 、
、 ,其中
,其中 的分子结构如下图所示,像一顶皇冠,请回答下列问题:
的分子结构如下图所示,像一顶皇冠,请回答下列问题: 中含有的
中含有的 键数目是
键数目是_______ 。
② 中S原子的杂化轨道类型是
中S原子的杂化轨道类型是_______ , 的空间结构是
的空间结构是_______ 。
③ 分子的VSEPR模型是
分子的VSEPR模型是_______ , 是
是_______ (填“极性”或“非极性”)分子。
④沸点:
_______  (填“
(填“ ”、“
”、“ ”或“
”或“ ”),原因是
”),原因是_______ 。
(1)A.乙烷 B.乙烯 C.乙炔 D.苯是有机化学中的代表物质,其中:
①既有
 键又有
键又有 键的是
键的是②碳碳键的键长由大到小排序是:
③上述分子中所有原子均在同一平面是:
(2)含硫元素的微粒有很多,例如
 、
、 、
、 、
、 、
、 ,其中
,其中 的分子结构如下图所示,像一顶皇冠,请回答下列问题:
的分子结构如下图所示,像一顶皇冠,请回答下列问题: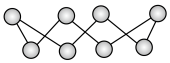
 中含有的
中含有的 键数目是
键数目是②
 中S原子的杂化轨道类型是
中S原子的杂化轨道类型是 的空间结构是
的空间结构是③
 分子的VSEPR模型是
分子的VSEPR模型是 是
是④沸点:

 (填“
(填“ ”、“
”、“ ”或“
”或“ ”),原因是
”),原因是
您最近一年使用:0次
名校
2 . 普通玻璃的主要成分为Na2SiO3、CaSiO3和SiO2,它是以纯碱、石灰石和石英砂(主要成分为SiO2)为原料,经混合,粉碎,在玻璃窑中熔融,发生复杂的物理变化和化学变化制得的。下列说法正确的是
| A.沸点:SiO2<Na2CO3 |
| B.SiO2的VSEPR模型与空间结构均为平面三角形 |
| C.Na2SiO3和CaCO3分别与足量的稀盐酸反应,反应后均无新的沉淀产生 |
| D.0.1 mol SiO2的质量为6 g |
您最近一年使用:0次
名校
解题方法
3 . 燃油汽车尾气中含有CO和氮氧化物,在 的催化作用下,发生反应:
的催化作用下,发生反应: ,可降低污染。其反应历程和相对能量变化如图所示:
,可降低污染。其反应历程和相对能量变化如图所示:不正确 的是
 的催化作用下,发生反应:
的催化作用下,发生反应: ,可降低污染。其反应历程和相对能量变化如图所示:
,可降低污染。其反应历程和相对能量变化如图所示: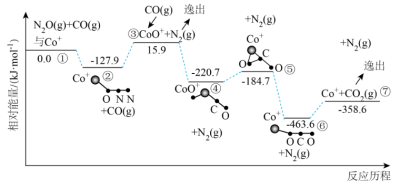
A. 分子的中心原子是N,分子中O—N—N的键角大于 分子的中心原子是N,分子中O—N—N的键角大于 分子中O—N—O的键角 分子中O—N—O的键角 |
| B.历程中决定反应速率的变化过程是②→③ |
C.总反应分两步进行,已知 参与第一步反应,则第二步反应为: 参与第一步反应,则第二步反应为: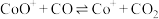 |
D.恒容、绝热下模拟反应: ,体系的温度、 ,体系的温度、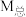 (平均相对分子质量)、压强恒定均能说明反应达到平衡状态 (平均相对分子质量)、压强恒定均能说明反应达到平衡状态 |
您最近一年使用:0次
名校
解题方法
4 . 过渡金属氧化物离子(以MO+表示)在烃类的选择性氧化等方面应用广泛。MO+与CH4反应的过程如下图所示。不正确 的是
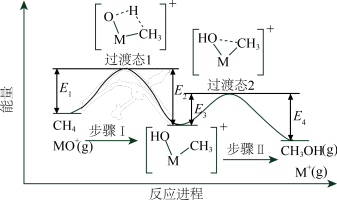
| A.反应速率:步骤I<步骤II |
| B.CH3OH分子中,键角:H—C—H>H—O—C |
| C.若MO+与CH3D反应,生成的氘代甲醇有2种 |
D.CH4(g) + MO+(g)=CH3OH(g) + M+(g)  = E2+E4-E1-E3 = E2+E4-E1-E3 |
您最近一年使用:0次
2024-04-01更新
|
515次组卷
|
5卷引用:江苏省常州市第一中学2023-2024学年高二下学期4月期中考试化学试题
江苏省常州市第一中学2023-2024学年高二下学期4月期中考试化学试题北京市丰台区2023-2024学年高三下学期综合练习(一)化学试题(已下线)通关练08 聚焦反应热、速率及化学平衡-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)化学(天津卷03)-2024年高考化学押题预测卷(已下线)提升练03 反应历程探究与催化原理-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
5 . 下列说法不正确的是
| A.(AlCl3)2中含有配位键 |
| B.NH3的键角大于H2O的键角 |
| C.SiO2中的O—Si—O键角为120° |
| D.H3BO3是弱酸,H3BO3晶体中存在作用力为共价键、氢键和范德华力 |
您最近一年使用:0次
6 . 完成表中内容。
| σ数 | 孤电子对数 | 杂化方式 | VSEPR模型 | 分子空间构型 | |
| CO2 | |||||
| H2O |
您最近一年使用:0次
2024-02-24更新
|
252次组卷
|
3卷引用:黑龙江省佳木斯市三校联考2023-2024学年高二下学期4月期中考试化学试题
名校
7 . 元素是构成我们生活中一切物质的“原材料”。回答下列问题:
(1)(SCN)2中各元素的第一电离能最大的是___________ (填元素符号)。
(2)钛位于元素周期表中的第四周期、第ⅣB族。
①六氟合钛酸钾(K2TiF6)中存在[TiF6]2-,该晶体中不存在的化学键有___________ (填字母序号)。
a.离子键 b.极性键 c.非极性键 d配位键
②纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下:

有机物甲中标“*”碳原子的杂化方式为___________ 。有机物乙的沸点___________ (填“高于”或“低于”)有机物甲,主要原因为___________ 。
(3)在乙醚溶液中,InCl3与LiH反应生成LiInH4和某物质,该反应的化学方程式为___________ ,LiInH4中阴离子的空间结构为___________ 形。
(4)氯化锂的晶胞如图所示,氯化锂晶体密度为ρg/cm3。设NA为阿伏加德罗常数的值,该晶体中相邻锂原子间的最短距离为___________ cm(列出计算式)。

(1)(SCN)2中各元素的第一电离能最大的是
(2)钛位于元素周期表中的第四周期、第ⅣB族。
①六氟合钛酸钾(K2TiF6)中存在[TiF6]2-,该晶体中不存在的化学键有
a.离子键 b.极性键 c.非极性键 d配位键
②纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下:

有机物甲中标“*”碳原子的杂化方式为
(3)在乙醚溶液中,InCl3与LiH反应生成LiInH4和某物质,该反应的化学方程式为
(4)氯化锂的晶胞如图所示,氯化锂晶体密度为ρg/cm3。设NA为阿伏加德罗常数的值,该晶体中相邻锂原子间的最短距离为

您最近一年使用:0次
名校
8 . 稀土是一种重要的战略资源,我国是稀土储量最大的国家。铈( )是一种典型的稀土元素,其在自然界中主要以氟碳铈矿(主要成分为
)是一种典型的稀土元素,其在自然界中主要以氟碳铈矿(主要成分为 )形式存在。工业上利用氟碳铈矿制取
)形式存在。工业上利用氟碳铈矿制取 的一种工艺流程如图:
的一种工艺流程如图:

下列说法错误的是
 )是一种典型的稀土元素,其在自然界中主要以氟碳铈矿(主要成分为
)是一种典型的稀土元素,其在自然界中主要以氟碳铈矿(主要成分为 )形式存在。工业上利用氟碳铈矿制取
)形式存在。工业上利用氟碳铈矿制取 的一种工艺流程如图:
的一种工艺流程如图:
下列说法错误的是
A.倍烧过程中氧化剂与还原剂的物质的量之比为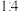 |
B.通过操作Ⅱ(包含酸溶、蒸发结晶)即可得到纯净的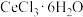 |
| C.酸浸过程中用稀硫酸和双氧水替代盐酸可体现环境友好 |
D. 中阴离子的空间构型为正四面体 中阴离子的空间构型为正四面体 |
您最近一年使用:0次
2024-01-09更新
|
400次组卷
|
4卷引用:上海市宜川中学2023-2024学年高三上学期期中考试卷(化学)
名校
9 . 生成氢气:在恒温恒容的反应器中,将水蒸气通过红热的炭即产生水煤气: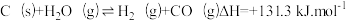 。
。
(1)以上涉及到的元素中,电负性最大的元素为_______。
(2)H2O的价层电子对空间结构为_______ (需过程)
(3)写出该反应的平衡常数表达式_______ 。
(4)下列能作为反应达到平衡的判据是_______。
(5)有利于提高H2平衡产率的条件是_______。
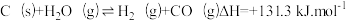 。
。(1)以上涉及到的元素中,电负性最大的元素为_______。
| A.碳 | B.氢 | C.氧 |
(3)写出该反应的平衡常数表达式
(4)下列能作为反应达到平衡的判据是_______。
| A.容器内气体的压强不变 |
| B.K值不变 |
| C.H2O和H2的物质的量之比不变 |
| D.CO和H2的物质的量之比不变 |
| A.低温低压 | B.低温高压 |
| C.高温低压 | D.高温高压 |
您最近一年使用:0次
名校
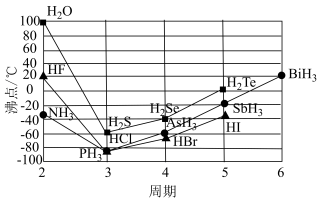
10 . 下图为第ⅤA族、ⅥA、ⅦA族元素简单氢化物沸点随周期数的递变趋势图。
(1)解释第ⅤA族元素氢化物沸点变化的趋势:___________ ,推测ⅣA族 与
与 的沸点大小为
的沸点大小为
___________  (填“>”或“<”)。
(填“>”或“<”)。
(2)接近水的沸点的水蒸气的相对分子质量测定值比按化学式 计算出的相对分子质量大一些,原因为
计算出的相对分子质量大一些,原因为___________ 。
(3) 常用于制备半导体材料,
常用于制备半导体材料, 与足量的
与足量的 加热可反应得到
加热可反应得到 ,写出该反应的化学方程式
,写出该反应的化学方程式___________ 。通过___________ 的实验分析方法可测出 的键长键角信息,下列关于
的键长键角信息,下列关于 分子的说法正确的是
分子的说法正确的是___________ 。
A.中心原子价层电子对数为5对
B.分子的空间构型为正四面体
C.中心原子的杂化方式为 杂化
杂化
(1)解释第ⅤA族元素氢化物沸点变化的趋势:
 与
与 的沸点大小为
的沸点大小为
 (填“>”或“<”)。
(填“>”或“<”)。(2)接近水的沸点的水蒸气的相对分子质量测定值比按化学式
 计算出的相对分子质量大一些,原因为
计算出的相对分子质量大一些,原因为(3)
 常用于制备半导体材料,
常用于制备半导体材料, 与足量的
与足量的 加热可反应得到
加热可反应得到 ,写出该反应的化学方程式
,写出该反应的化学方程式 的键长键角信息,下列关于
的键长键角信息,下列关于 分子的说法正确的是
分子的说法正确的是A.中心原子价层电子对数为5对
B.分子的空间构型为正四面体
C.中心原子的杂化方式为
 杂化
杂化
您最近一年使用:0次
2023-12-27更新
|
226次组卷
|
2卷引用:海南省海口市海南中学2023-2024学年高二上学期期中考试化学试题



