解题方法
1 . 浏阳花炮闻名中外,其以土硝(NaNO3)、硫黄、炭和为主要药剂,采用传统手工技艺制成。下列说法正确的是
| A.32 g S8中含有0.875 mol σ键。 |
| B.土硝中阴离子的空间结构为平面三角形 |
| C.碳有12C、13C、14C等多种同素异形体 |
| D.钾的焰色试验呈紫色是因为电子由低能级跃迁至高能级 |
您最近一年使用:0次
解题方法
2 . 下列说法正确的是
| A.碱金属和碱土金属元素均位于元素周期表的p区 |
B.NaCl中化学键的离子键百分数比 中的低 中的低 |
C. 中存在 中存在 与 与 之间的强烈相互作用 之间的强烈相互作用 |
D. 中 中 的空间结构为三角锥形 的空间结构为三角锥形 |
您最近一年使用:0次
2024-05-14更新
|
215次组卷
|
2卷引用:江苏省南京市2024届高三下学期第二次模拟考试化学试题
解题方法
3 . 黑磷纳米材料可用4-甲氧基重氮苯四氟硼酸盐处理,以保护和控制其性质,该盐的结构如图所示。下列说法正确的是
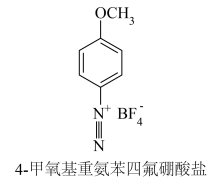
A.电负性: | B.该盐含有离子键、共价键 |
| C.该盐阴离子的空间结构是三角锥形 | D.该盐中含氧官能团名称为羰基 |
您最近一年使用:0次
解题方法
4 . 完成下列问题
(1)水分子中的共价键,依据原子轨道重叠的方式判断,属于___________ 键,水分子的VSEPR模型名称是___________ 。
(2)由铁原子形成的四种微粒,价层电子轨道表示式分别为①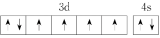 、②
、②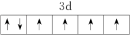 、③
、③ 、④
、④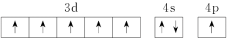 ,有关这些微粒的叙述不正确的是
,有关这些微粒的叙述不正确的是___________ (填字母)。
A.微粒半径:④>①>②
B.电离一个电子所需最低能量:②>①>④
C.微粒③价层电子在简并轨道中单独分占且自旋相同,故不能再继续失电子
(3)用“>”或“<”填空:
①沸点:邻羟基苯甲酸___________ 对羟基苯甲酸。
②pKa:CF3COOH___________ CH3COOH。
(4)填写下列物质所含官能团的名称
①CH3C≡CCH3___________ ;___________ 。
(5)下列化合物中,核磁共振氢谱只出现三组峰且峰面积之比为3:2:2的是___________。
(6)某烃的蒸气对H2的相对密度为21,该烃中碳元素的质量分数为85.7%,则该烃的分子式为___________ ,可能的结构简式为___________ 、___________ 。
(1)水分子中的共价键,依据原子轨道重叠的方式判断,属于
(2)由铁原子形成的四种微粒,价层电子轨道表示式分别为①
 、②
、② 、③
、③ 、④
、④ ,有关这些微粒的叙述不正确的是
,有关这些微粒的叙述不正确的是A.微粒半径:④>①>②
B.电离一个电子所需最低能量:②>①>④
C.微粒③价层电子在简并轨道中单独分占且自旋相同,故不能再继续失电子
(3)用“>”或“<”填空:
①沸点:邻羟基苯甲酸
②pKa:CF3COOH
(4)填写下列物质所含官能团的名称
①CH3C≡CCH3
②
(5)下列化合物中,核磁共振氢谱只出现三组峰且峰面积之比为3:2:2的是___________。
| A.(CH3)2CHCH(CH3)2 | B.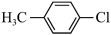 |
C.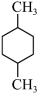 | D.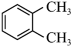 |
您最近一年使用:0次
名校
解题方法
5 . 铁及其化合物在生产、生活中应用广泛。回答下列问题:
(1)基态Fe原子核外电子排布式为___________ 。
(2) 可与
可与 形成配离子
形成配离子 ,
, 可与NO形成配离子
可与NO形成配离子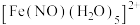 。
。
①S、N、O三种元素第一电离能由大到小的顺序为___________ 。
②每个 中含有σ键的数目是
中含有σ键的数目是___________ 。
(3) 的结构如图1所示。
的结构如图1所示。___________
②H2O中H-O-H键角___________ (填“>”“<”或“=”) 中O-S-O键角。
中O-S-O键角。
(4)由铁铜硫形成的某化合物的晶胞结构如图2所示。___________ 。
②若该晶体的密度为ρ g⋅cm ,则该晶胞的底面边长a=
,则该晶胞的底面边长a=___________ pm( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)基态Fe原子核外电子排布式为
(2)
 可与
可与 形成配离子
形成配离子 ,
, 可与NO形成配离子
可与NO形成配离子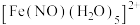 。
。①S、N、O三种元素第一电离能由大到小的顺序为
②每个
 中含有σ键的数目是
中含有σ键的数目是(3)
 的结构如图1所示。
的结构如图1所示。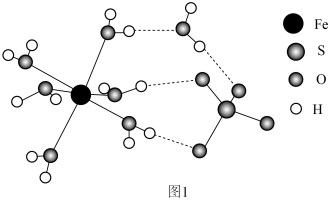
②H2O中H-O-H键角
 中O-S-O键角。
中O-S-O键角。(4)由铁铜硫形成的某化合物的晶胞结构如图2所示。
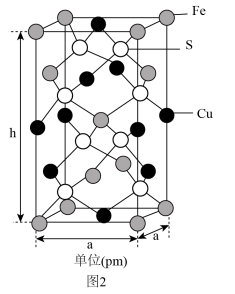
②若该晶体的密度为ρ g⋅cm
 ,则该晶胞的底面边长a=
,则该晶胞的底面边长a= 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解题方法
6 . 制备光气的反应原理为 ,已知:
,已知: 的结构如图所示,下列说法正确的是
的结构如图所示,下列说法正确的是
 ,已知:
,已知: 的结构如图所示,下列说法正确的是
的结构如图所示,下列说法正确的是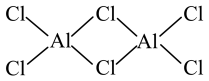
A. 中心原子的VSEPR模型与 中心原子的VSEPR模型与 中心原子的VSEPR模型相同 中心原子的VSEPR模型相同 |
B. 中含有离子键和配位键 中含有离子键和配位键 |
C.熔点的大小顺序为: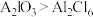 |
| D.第三周期元素中第一电离能小于Al的元素有2种 |
您最近一年使用:0次
解题方法
7 . 某大学教授课题研究组首次合成了石墨二炔—氧化铟(GDY—IO)纳米复合材料,并将其应用于气相光催化还原 制得
制得 碳氢化合物。
碳氢化合物。______ 。
(2)石墨二炔可以被看作是石墨烯中三分之一的C—C中插入两个 (二炔或乙炔)键,石墨二炔(GDY)中C原子的杂化轨道类型有
(二炔或乙炔)键,石墨二炔(GDY)中C原子的杂化轨道类型有______ 。
(3)石墨能与熔融金属钾作用,形成石墨间隙化合物,钾原子填充在石墨各层原子中。较常见的石墨间隙化合物是青铜色的化合物,其化学式可写为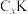 ,其平面图形如图1所示,x的值为
,其平面图形如图1所示,x的值为______ ;在石墨片层结构中,碳原子、C—C键、六元环的个数之比为______ 。 易与铁触媒作用导致其失去催化活性:
易与铁触媒作用导致其失去催化活性: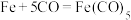 ,
, 又名羟基铁,常温下为黄色油状液体,则
又名羟基铁,常温下为黄色油状液体,则 的晶体类型是
的晶体类型是______ 。
(5)乙烯分子中碳碳双键与碳氢键间的键角大于碳氢键之间的键角,原因是____________ 。
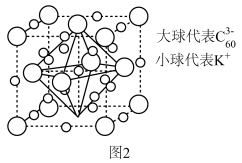
(6)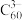 与
与 能形成图2中的超分子加合物,已知晶胞参数为
能形成图2中的超分子加合物,已知晶胞参数为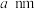 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶胞的密度为
,则该晶胞的密度为______  (列出计算表达式)。
(列出计算表达式)。
 制得
制得 碳氢化合物。
碳氢化合物。
(2)石墨二炔可以被看作是石墨烯中三分之一的C—C中插入两个
 (二炔或乙炔)键,石墨二炔(GDY)中C原子的杂化轨道类型有
(二炔或乙炔)键,石墨二炔(GDY)中C原子的杂化轨道类型有(3)石墨能与熔融金属钾作用,形成石墨间隙化合物,钾原子填充在石墨各层原子中。较常见的石墨间隙化合物是青铜色的化合物,其化学式可写为
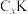 ,其平面图形如图1所示,x的值为
,其平面图形如图1所示,x的值为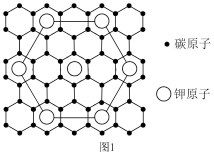
 易与铁触媒作用导致其失去催化活性:
易与铁触媒作用导致其失去催化活性: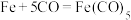 ,
, 又名羟基铁,常温下为黄色油状液体,则
又名羟基铁,常温下为黄色油状液体,则 的晶体类型是
的晶体类型是(5)乙烯分子中碳碳双键与碳氢键间的键角大于碳氢键之间的键角,原因是
(6)
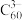 与
与 能形成图2中的超分子加合物,已知晶胞参数为
能形成图2中的超分子加合物,已知晶胞参数为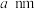 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶胞的密度为
,则该晶胞的密度为 (列出计算表达式)。
(列出计算表达式)。
您最近一年使用:0次
名校
解题方法
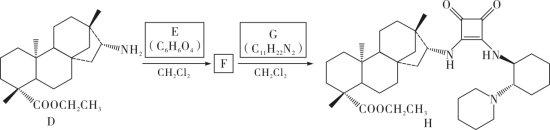
8 . 溶剂是影响化学反应的重要因素之一,当反应在无溶剂条件下进行时,具有操作简单、反应时间短、无溶剂浪费且遵循绿色化学的原理等独特优点。因此,无溶剂不对称催化已成为合成化学中的重要课题。化合物H是一种手性有机催化剂,可无溶剂催化如下迈克尔加成反应(Michael addition reaction): 、R(大)、R′(小)顺时针排列的面称为Re-face(下图左),逆时针排列的面称为Si-face(下图右),—R″进攻不同面β-碳的产物互为手性异构体
、R(大)、R′(小)顺时针排列的面称为Re-face(下图左),逆时针排列的面称为Si-face(下图右),—R″进攻不同面β-碳的产物互为手性异构体
(1)A的化学名称为___________ ;B为反式结构,其结构简式为___________ 。
(2)已知E的核磁共振氢谱只有一个吸收峰。写出D(用 简化表示)与E反应的化学方程式
简化表示)与E反应的化学方程式___________ ,该反应类型为___________ 。
(3)G的同分异构体中,含有碳、氮环状骨架为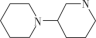 的共有
的共有___________ 种(不含立体异构)。
(4)推测H催化A和B反应的部分机理可能为:A异构化为烯醇(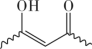 ),再和B与催化剂H结合(如图所示,
),再和B与催化剂H结合(如图所示,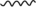 表示链的延长)。反应物与催化剂H结合的作用力主要是下列中的
表示链的延长)。反应物与催化剂H结合的作用力主要是下列中的___________ (填标号)。
a.离子键 b.共价键 c.配位键 d.氢键___________ 。
(5)如果要合成H的类似物H′(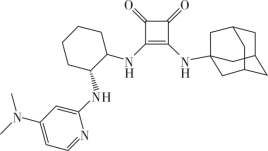 ),参照上述合成路线,写出相应的G′的结构简式
),参照上述合成路线,写出相应的G′的结构简式___________ 。以甲苯为溶剂,H′可催化A与B的迈克尔加成反应,产物主要是___________ (填“C”“C的手性异构体”或“C及其手性异构体各占50%”),判断理由是___________ 。
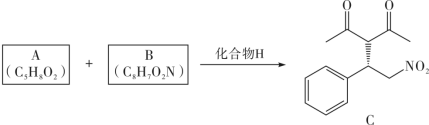
化合物H的合成路线如下( 、
、 分别表示由纸面向内、向外伸展的共价键):
分别表示由纸面向内、向外伸展的共价键):
 、R(大)、R′(小)顺时针排列的面称为Re-face(下图左),逆时针排列的面称为Si-face(下图右),—R″进攻不同面β-碳的产物互为手性异构体
、R(大)、R′(小)顺时针排列的面称为Re-face(下图左),逆时针排列的面称为Si-face(下图右),—R″进攻不同面β-碳的产物互为手性异构体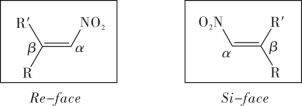
(1)A的化学名称为
(2)已知E的核磁共振氢谱只有一个吸收峰。写出D(用
 简化表示)与E反应的化学方程式
简化表示)与E反应的化学方程式(3)G的同分异构体中,含有碳、氮环状骨架为
 的共有
的共有(4)推测H催化A和B反应的部分机理可能为:A异构化为烯醇(
 ),再和B与催化剂H结合(如图所示,
),再和B与催化剂H结合(如图所示,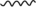 表示链的延长)。反应物与催化剂H结合的作用力主要是下列中的
表示链的延长)。反应物与催化剂H结合的作用力主要是下列中的a.离子键 b.共价键 c.配位键 d.氢键
(5)如果要合成H的类似物H′(
 ),参照上述合成路线,写出相应的G′的结构简式
),参照上述合成路线,写出相应的G′的结构简式
您最近一年使用:0次
解题方法
9 . 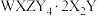 可用作膳食补充剂、药物制剂的压片剂及用于一些旨在消除体味的产品中已知X、Y、Z、W为原子序数依次增大的前20号主族元素,四种元素均位于不同周期。其中X、Y、Z三种元素原子序数为等差数列,基态Y原子s轨道电子数与p轨道电子数相等,基态W原子核外无未成对电子。下列说法正确的是
可用作膳食补充剂、药物制剂的压片剂及用于一些旨在消除体味的产品中已知X、Y、Z、W为原子序数依次增大的前20号主族元素,四种元素均位于不同周期。其中X、Y、Z三种元素原子序数为等差数列,基态Y原子s轨道电子数与p轨道电子数相等,基态W原子核外无未成对电子。下列说法正确的是
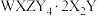 可用作膳食补充剂、药物制剂的压片剂及用于一些旨在消除体味的产品中已知X、Y、Z、W为原子序数依次增大的前20号主族元素,四种元素均位于不同周期。其中X、Y、Z三种元素原子序数为等差数列,基态Y原子s轨道电子数与p轨道电子数相等,基态W原子核外无未成对电子。下列说法正确的是
可用作膳食补充剂、药物制剂的压片剂及用于一些旨在消除体味的产品中已知X、Y、Z、W为原子序数依次增大的前20号主族元素,四种元素均位于不同周期。其中X、Y、Z三种元素原子序数为等差数列,基态Y原子s轨道电子数与p轨道电子数相等,基态W原子核外无未成对电子。下列说法正确的是A.第一电离能: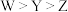 |
B.最简单氢化物的熔、沸点: |
| C.上述化合物的固体为分子晶体 |
| D.Z的最高价氧化物的水化物的阴离子空间结构为正四面体形 |
您最近一年使用:0次
解题方法
10 . 下列根据事实得出的推论正确的是
选项 | 事实 | 推论 |
A | F和I是同主族元素,HF是弱酸 | HI也是弱酸 |
B | 电负性: | 键角: |
C |
| 两者空间结构相同 |
D | 某晶体熔点高、硬度大、不导电 | 该晶体一定是分子晶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

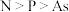
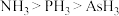
 和
和 均为
均为 型化合物
型化合物

