解题方法
1 . 五羰基铁是一种黄色液体,熔点-20℃,沸点103℃,可以用细铁粉和 制备,流程如下:
制备,流程如下:
 中含有
中含有 键
键_____  ,配位原子为
,配位原子为_____ 。
(2)下列说法正确的是:_____ 。
A. 中
中 的化合价为0价,为离子晶体
的化合价为0价,为离子晶体
B.制备 反应需在隔绝空气下进行
反应需在隔绝空气下进行
C. 的结构可以用X射线衍射进行研究,它的空间结构为三角双锥形
的结构可以用X射线衍射进行研究,它的空间结构为三角双锥形
D.B的分子式为
E.已知在丙酮中 可以被氯化铜完全氧化,推测产物中有
可以被氯化铜完全氧化,推测产物中有 、
、 和
和
(3) 在紫外光作用下可以生成
在紫外光作用下可以生成 和化合物A,已知化合物A的1个分子中含有1个
和化合物A,已知化合物A的1个分子中含有1个 键,和3个成桥的羰基,每个
键,和3个成桥的羰基,每个 被6个
被6个 分子以略变形的八面体所包围,则A的分子式为
分子以略变形的八面体所包围,则A的分子式为_____ 。
(4)写出反应③的方程式:_____ 。
(5)某实验小组预测 隔绝空气加热产物为
隔绝空气加热产物为 和
和 ,如何设计定量实验证明产物,请设计实验方案:(说明主要试剂和方法即可)
,如何设计定量实验证明产物,请设计实验方案:(说明主要试剂和方法即可)_____ 。
 制备,流程如下:
制备,流程如下: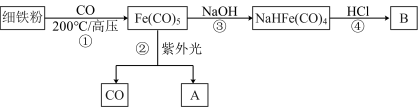

 中含有
中含有 键
键 ,配位原子为
,配位原子为(2)下列说法正确的是:
A.
 中
中 的化合价为0价,为离子晶体
的化合价为0价,为离子晶体B.制备
 反应需在隔绝空气下进行
反应需在隔绝空气下进行C.
 的结构可以用X射线衍射进行研究,它的空间结构为三角双锥形
的结构可以用X射线衍射进行研究,它的空间结构为三角双锥形D.B的分子式为

E.已知在丙酮中
 可以被氯化铜完全氧化,推测产物中有
可以被氯化铜完全氧化,推测产物中有 、
、 和
和
(3)
 在紫外光作用下可以生成
在紫外光作用下可以生成 和化合物A,已知化合物A的1个分子中含有1个
和化合物A,已知化合物A的1个分子中含有1个 键,和3个成桥的羰基,每个
键,和3个成桥的羰基,每个 被6个
被6个 分子以略变形的八面体所包围,则A的分子式为
分子以略变形的八面体所包围,则A的分子式为(4)写出反应③的方程式:
(5)某实验小组预测
 隔绝空气加热产物为
隔绝空气加热产物为 和
和 ,如何设计定量实验证明产物,请设计实验方案:(说明主要试剂和方法即可)
,如何设计定量实验证明产物,请设计实验方案:(说明主要试剂和方法即可)
您最近一年使用:0次
解题方法
2 . 含硅化合物在生活中的应用非常广泛。请回答下列问题:
(1)祖母绿宝石的主要成分化学式为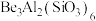 ,
, 与
与 的第一电离能大小关系为:
的第一电离能大小关系为:
___________ 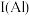 。
。
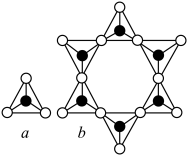
(2)硅酸盐的阴离子结构丰富多样,有些是有限数目的硅氧四面体构建的简单阴离子,如图所示,最简单的硅酸盐阴离子a的化学式为 ,则六元环状硅酸盐阴离子b的化学式是
,则六元环状硅酸盐阴离子b的化学式是___________ (不能用最简式表示)。
(3)工业制备高纯硅,先用焦炭在电炉中将石英还原为粗硅,再将粗硅与 在300℃反应生成
在300℃反应生成 ,氯原子的价层电子排布式为
,氯原子的价层电子排布式为___________ , 的空间构型为
的空间构型为___________ 。
(4)硅的各种卤化物的沸点如下表,沸点依次升高的原因是___________ 。
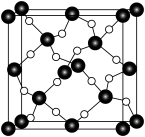
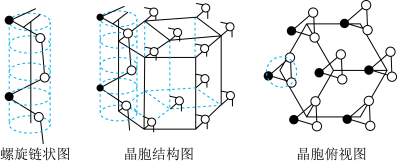
(5)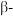 石英是晶质石英(
石英是晶质石英( )的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为
)的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为___________ ,请用价层电子对互斥模型解释图中键角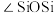 并不是
并不是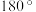 的原因是
的原因是___________ 。
(1)祖母绿宝石的主要成分化学式为
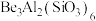 ,
, 与
与 的第一电离能大小关系为:
的第一电离能大小关系为:
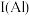 。
。(2)硅酸盐的阴离子结构丰富多样,有些是有限数目的硅氧四面体构建的简单阴离子,如图所示,最简单的硅酸盐阴离子a的化学式为
 ,则六元环状硅酸盐阴离子b的化学式是
,则六元环状硅酸盐阴离子b的化学式是
(3)工业制备高纯硅,先用焦炭在电炉中将石英还原为粗硅,再将粗硅与
 在300℃反应生成
在300℃反应生成 ,氯原子的价层电子排布式为
,氯原子的价层电子排布式为 的空间构型为
的空间构型为(4)硅的各种卤化物的沸点如下表,沸点依次升高的原因是
 |  | 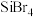 |  | |
| 沸点/K | 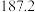 | 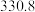 | 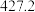 | 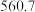 |
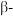 石英是晶质石英(
石英是晶质石英( )的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为
)的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为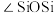 并不是
并不是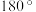 的原因是
的原因是
您最近一年使用:0次
名校
解题方法
3 . 关于物质结构与性质的内在联系,请回答下列问题:
(1)已知Se与O同族,基态Se原子价层电子的运动状态有______ 种,基态O原子的电子排布式不能表示为1s22s22p 2p
2p ,因为这违背了
,因为这违背了______ (填选项)。
A.能量最低原理 B.泡利不相容原理 C.洪特规则
(2)已知液态的二氧化硫可以发生类似的水自身电离反应:2SO2(l) SO2++SO
SO2++SO 。SO2+中的σ键和π键数目之比为
。SO2+中的σ键和π键数目之比为______ ,SO2的空间构型为______ 。
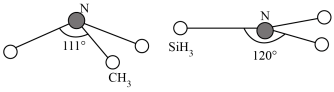
(3)由于硅的价层有d轨道可以利用,而碳没有,因此它们的化合物结构和性质存在较大差异。化合物N(CH3)3(三角锥形)和N(SiH3)3(平面形)的结构如图所示,则二者中N的杂化方式分别为______ 。更易形成配合物的是______ 。______ 。______ g•cm-3(用含NA、a、b的式子表示)。
(1)已知Se与O同族,基态Se原子价层电子的运动状态有
 2p
2p ,因为这违背了
,因为这违背了A.能量最低原理 B.泡利不相容原理 C.洪特规则
(2)已知液态的二氧化硫可以发生类似的水自身电离反应:2SO2(l)
 SO2++SO
SO2++SO 。SO2+中的σ键和π键数目之比为
。SO2+中的σ键和π键数目之比为(3)由于硅的价层有d轨道可以利用,而碳没有,因此它们的化合物结构和性质存在较大差异。化合物N(CH3)3(三角锥形)和N(SiH3)3(平面形)的结构如图所示,则二者中N的杂化方式分别为
您最近一年使用:0次
名校
解题方法
4 . 氮的相关化合物在材料等方面有重要用途。回答下列问题:
(1)在第二周期中,第一电离能比N高的主族元素是_______ 。氮原子的电子排布图表示的状态中,能量由低到高的顺序是_______ (填序号)。
A. B.
B.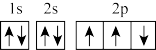
C.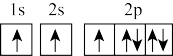 D.
D.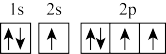
(2)科学家从(NH4)2SO4中检出一种组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以SO 和N4H
和N4H 两种离子的形式存在。N4H
两种离子的形式存在。N4H 的空间构型与NH
的空间构型与NH 相同,则1个N4H
相同,则1个N4H 中含有
中含有_______ 个σ键。
(3)科学家合成了一种阳离子为“N ”,其结构是对称的,5个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N
”,其结构是对称的,5个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N ”化学式为N8的离子晶体,其阳离子电子式为
”化学式为N8的离子晶体,其阳离子电子式为_______ ,阴离子的空间构型为_______ 。
(4)GaN、GaP、GaAs熔融状态均不导电,熔点如表所示。其中GaN晶胞如图所示,结构可看作金刚石晶胞内部的碳原子被N原子代替(如b),顶点和面心的碳原子被Ga原子代替(如a)。

①试分析GaN、GaP、GaAs熔点依次降低的原因:_______ ;
②GaN晶胞中与Ga原子周围与它最近且相等距离的Ga原子有_______ 个。
(1)在第二周期中,第一电离能比N高的主族元素是
A.
 B.
B.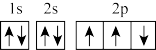
C.
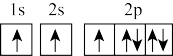 D.
D.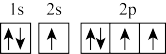
(2)科学家从(NH4)2SO4中检出一种组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以SO
 和N4H
和N4H 两种离子的形式存在。N4H
两种离子的形式存在。N4H 的空间构型与NH
的空间构型与NH 相同,则1个N4H
相同,则1个N4H 中含有
中含有(3)科学家合成了一种阳离子为“N
 ”,其结构是对称的,5个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N
”,其结构是对称的,5个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N ”化学式为N8的离子晶体,其阳离子电子式为
”化学式为N8的离子晶体,其阳离子电子式为(4)GaN、GaP、GaAs熔融状态均不导电,熔点如表所示。其中GaN晶胞如图所示,结构可看作金刚石晶胞内部的碳原子被N原子代替(如b),顶点和面心的碳原子被Ga原子代替(如a)。

| 物质 | GaN | GaP | GaAs |
| 熔点/℃ | 1700 | 1480 | 1238 |
②GaN晶胞中与Ga原子周围与它最近且相等距离的Ga原子有
您最近一年使用:0次
2022-12-22更新
|
535次组卷
|
3卷引用:浙江省金华第一中学等四校2022-2023学年高三上学期12月联考化学试题
名校
解题方法
5 . NaH和NaAlH4都是重要的还原剂,一定条件下金属钠和H2反应生成NaH。NaH与水反应可生成H2,NaH与AlCl3反应可得到NaAlH4。下列说法错误的是
| A.NaAlH4中阴离子空间构型为正四面体 |
| B.NaH与AlCl3得到NaAlH4的反应属于氧化还原反应 |
| C.NaH在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3) |
| D.金属钠和H2反应生成NaH的反应体系需要控制无氧、无水和无酸等条件 |
您最近一年使用:0次
2020-12-06更新
|
876次组卷
|
5卷引用:解密03 氧化还原反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)
(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)山东省青岛市黄岛区2021届高三上学期期中考试化学试题(已下线)练习14 分子的空间结构-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练河北省石家庄市第一中学2020-2021学年高二下学期学情反馈(一)化学试题



