名校
解题方法
1 . 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
(1)请根据对角线规则写出Be与NaOH 溶液反应的化学方程式___________ 。
(2)D的气态氢化物的VSEPR模型为___________ ,其中心原子的杂化类型为___________ 。
(3)G、H和Ⅰ的第一电离能数值由大到小的顺序为:___________ (用元素符号作答)。
(4)C原子在形成化合物时,可采取多种杂化方式。杂化轨道中s轨道成分越多,C元素的电负性越强,连接在该C原子上的H原子越容易电离。下列化合物中,最有可能在碱性体系中形成阴离子的是___________(填编号)。
(5)要证明太阳上是否含有R元素,可采用的方法是___________ 。
(6)与M同周期的所有元素的基态原子中最外层电子数与M原子相同的元素还有___________ (填元素符号)。
(7)C元素是形成有机物的主要元素,下列分子中含有sp和 杂化方式的是
杂化方式的是___________ (填字母)。
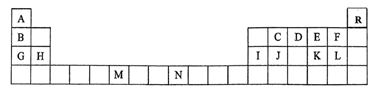
(1)请根据对角线规则写出Be与NaOH 溶液反应的化学方程式
(2)D的气态氢化物的VSEPR模型为
(3)G、H和Ⅰ的第一电离能数值由大到小的顺序为:
(4)C原子在形成化合物时,可采取多种杂化方式。杂化轨道中s轨道成分越多,C元素的电负性越强,连接在该C原子上的H原子越容易电离。下列化合物中,最有可能在碱性体系中形成阴离子的是___________(填编号)。
A. | B. | C. | D.苯 |
(6)与M同周期的所有元素的基态原子中最外层电子数与M原子相同的元素还有
(7)C元素是形成有机物的主要元素,下列分子中含有sp和
 杂化方式的是
杂化方式的是a.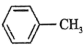 b.
b. c.
c. d.
d.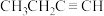
您最近一年使用:0次
名校
解题方法
2 .  均是铬的重要化合物,回答下列问题:
均是铬的重要化合物,回答下列问题:
(1)基态 原子有
原子有___________ 种能量不同的电子,价电子排布式为___________ 。
(2)已知电子亲和能(E)是基态的气态原子得到电子变为气态阴离子所放出的能量, ,氧的第一电子亲和能
,氧的第一电子亲和能 为
为___________  ;
; ,其原因是
,其原因是___________ 。
(3)雷氏盐的化学式为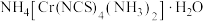 。
。
①H、C、N、O四种元素的电负性由大到小的顺序为___________ 。
②雷氏盐中所含化学键类型___________ 。
A.离子键 B.共价键 C.配位键 D.金属键 E.氢键
③配体之一 分子的立体构型为
分子的立体构型为___________ ,与配体 互为等电子体的分子和离子有
互为等电子体的分子和离子有___________ (各写1种)。
(4)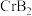 的晶体密度为
的晶体密度为 ,晶体结构(如图)为六棱柱,底边边长为
,晶体结构(如图)为六棱柱,底边边长为 ,高为
,高为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则
,则
___________ (列出计算式)。

 均是铬的重要化合物,回答下列问题:
均是铬的重要化合物,回答下列问题:(1)基态
 原子有
原子有(2)已知电子亲和能(E)是基态的气态原子得到电子变为气态阴离子所放出的能量,
 ,氧的第一电子亲和能
,氧的第一电子亲和能 为
为 ;
; ,其原因是
,其原因是(3)雷氏盐的化学式为
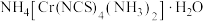 。
。①H、C、N、O四种元素的电负性由大到小的顺序为
②雷氏盐中所含化学键类型
A.离子键 B.共价键 C.配位键 D.金属键 E.氢键
③配体之一
 分子的立体构型为
分子的立体构型为 互为等电子体的分子和离子有
互为等电子体的分子和离子有(4)
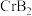 的晶体密度为
的晶体密度为 ,晶体结构(如图)为六棱柱,底边边长为
,晶体结构(如图)为六棱柱,底边边长为 ,高为
,高为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则
,则

您最近一年使用:0次
2024-04-04更新
|
439次组卷
|
2卷引用:四川省绵阳市绵阳中学2024届高三一模理综-化学试题
名校
解题方法
3 . Co元素的某些化合物在电池、光电材料、催化剂等方面有广泛应用。回答下列问题:
(1)一种具有光催化作用的配合物A结构简式如图所示:
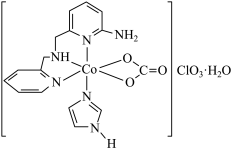
①基态Co原子价电子排布图为___________ 。
②外界 的空间构型为
的空间构型为___________ ,钴元素价态为___________ 。
③配合物A配位数为___________ ,中心离子的杂化方式为___________ (填标号)。
A.sp3 B.dsp2 C.d2sp3 D.sp3d
④咪唑( )具有类似苯环的结构,①号N比②号N更易与钴形成配位键的原因是
)具有类似苯环的结构,①号N比②号N更易与钴形成配位键的原因是_________ 。
(2)Co的一种化合物为六方晶系晶体,晶胞结构如图所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数体标。

已知晶胞含对称中心,其中1号氧原子的分数坐标为(0.6667,0.6667,0.6077),则2号氧原子的分数坐标为___________ ;NA为阿伏加德罗常数的值,该晶体的密度为___________ g/cm3(用计算式表示)。
(1)一种具有光催化作用的配合物A结构简式如图所示:

①基态Co原子价电子排布图为
②外界
 的空间构型为
的空间构型为③配合物A配位数为
A.sp3 B.dsp2 C.d2sp3 D.sp3d
④咪唑(
 )具有类似苯环的结构,①号N比②号N更易与钴形成配位键的原因是
)具有类似苯环的结构,①号N比②号N更易与钴形成配位键的原因是(2)Co的一种化合物为六方晶系晶体,晶胞结构如图所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数体标。

已知晶胞含对称中心,其中1号氧原子的分数坐标为(0.6667,0.6667,0.6077),则2号氧原子的分数坐标为
您最近一年使用:0次
2024-01-29更新
|
496次组卷
|
2卷引用:四川省成都市第七中学(林荫校区)2024届高三二诊热身考试理综-化学试题
名校
解题方法
4 . 锗(Ge)、碲化镉(CdTe)等是优良的半导体材料。回答下列问题:
(1)Ge在元素周期表中的位置___________ ,Ge的逐级电离能I4≪I5的原因是___________ 。
(2)经X射线衍射实验证明在碲酸( )分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为
)分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为___________ 。
(3)锗可以形成无机化合物 ,化合物中阴离子的空间构型为
,化合物中阴离子的空间构型为___________ ,锗也可以形成类似于烷烃结构的 (n一般小于5),化合物中Ge的杂化类型为
(n一般小于5),化合物中Ge的杂化类型为___________ , 该分子中含有的
该分子中含有的 键数目为
键数目为___________ 。
(4)锗的氯化物 常温下为无色液体,其沸点高于
常温下为无色液体,其沸点高于 ,原因是
,原因是___________ , 晶体采用ABC式的密堆积方式,则距离一个
晶体采用ABC式的密堆积方式,则距离一个 最近且等距离的
最近且等距离的 有
有___________ 个。
(5)CdTe的晶胞属立方晶系,晶胞如图所示,Te原子填充在Cd原子围成的空隙中该空隙的类型为___________ 空隙(填几何构型名称),若CdTe的摩尔质量为 ,该晶体的密度为
,该晶体的密度为 ,阿伏伽德罗常数为
,阿伏伽德罗常数为 ,则最近的两个Te原子的距离
,则最近的两个Te原子的距离___________ nm。(用含M、 、
、 的代数式表示)
的代数式表示)

(1)Ge在元素周期表中的位置
(2)经X射线衍射实验证明在碲酸(
 )分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为
)分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为(3)锗可以形成无机化合物
 ,化合物中阴离子的空间构型为
,化合物中阴离子的空间构型为 (n一般小于5),化合物中Ge的杂化类型为
(n一般小于5),化合物中Ge的杂化类型为 该分子中含有的
该分子中含有的 键数目为
键数目为(4)锗的氯化物
 常温下为无色液体,其沸点高于
常温下为无色液体,其沸点高于 ,原因是
,原因是 晶体采用ABC式的密堆积方式,则距离一个
晶体采用ABC式的密堆积方式,则距离一个 最近且等距离的
最近且等距离的 有
有(5)CdTe的晶胞属立方晶系,晶胞如图所示,Te原子填充在Cd原子围成的空隙中该空隙的类型为
 ,该晶体的密度为
,该晶体的密度为 ,阿伏伽德罗常数为
,阿伏伽德罗常数为 ,则最近的两个Te原子的距离
,则最近的两个Te原子的距离 、
、 的代数式表示)
的代数式表示)
您最近一年使用:0次
12-13高二上·四川遂宁·期中
名校
解题方法
5 . 下列说法错误的是
A.从CH4、 、 、 为正四面体结构,可推测PH 为正四面体结构,可推测PH 、 、 也为正四面体结构 也为正四面体结构 |
| B.1mol金刚石晶体中,平均含有2molC-C键 |
| C.水的沸点比硫化氢的高,是因为H2O分子间存在氢键,H2S分子间不能形成氢键 |
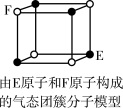
| D.某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE |
您最近一年使用:0次
2022-10-31更新
|
245次组卷
|
8卷引用:2012-2013学年四川省遂宁二中高二上学期期中考试化学试卷
真题
名校
6 . 三磷酸腺苷(ATP) 和活性氧类(如 H2O2和O )可在细胞代谢过程中产生。
)可在细胞代谢过程中产生。
(1)ATP 的分子式为C10H16N5O13P3,其中电负性最大的元素是_______ ,基态 N原子的电子排布图为_______ 。
(2)H2O2 分子的氧原子的杂化轨道类型为:_______ ;H2O2和H2O能以任意比例互溶的原因是_______ 。
(3)O3分子的立体构型为_______ 。根据表中数据判断氧原子之间的共价键最稳定的粒子是_______ 。
(4)研究发现纳米CeO2可催化O 分解,CeO2晶体属立方CaF2型晶体结构如图所示。
分解,CeO2晶体属立方CaF2型晶体结构如图所示。_______ nm。
②以晶胞参数为单位长度建立的中标系可以表示晶胞中的原子位置,称作原子分数坐标。A离子的坐标为(0, ,
, ),则B离子的坐标为
),则B离子的坐标为_______ 。
③纳米CeO2中位于晶粒表面的Ce4+能发挥催化作用,在边长为2 a nm的立方体晶粒中位于表面的Ce4+最多有_______ 个。
 )可在细胞代谢过程中产生。
)可在细胞代谢过程中产生。(1)ATP 的分子式为C10H16N5O13P3,其中电负性最大的元素是
(2)H2O2 分子的氧原子的杂化轨道类型为:
(3)O3分子的立体构型为
| 粒子 | O2 | O | O3 |
| 键长/pm | 121 | 126 | 128 |
(4)研究发现纳米CeO2可催化O
 分解,CeO2晶体属立方CaF2型晶体结构如图所示。
分解,CeO2晶体属立方CaF2型晶体结构如图所示。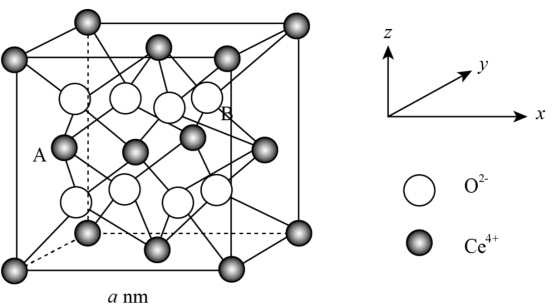
②以晶胞参数为单位长度建立的中标系可以表示晶胞中的原子位置,称作原子分数坐标。A离子的坐标为(0,
 ,
, ),则B离子的坐标为
),则B离子的坐标为③纳米CeO2中位于晶粒表面的Ce4+能发挥催化作用,在边长为2 a nm的立方体晶粒中位于表面的Ce4+最多有
您最近一年使用:0次
2022-05-27更新
|
4930次组卷
|
5卷引用:四川省内江市第六中学2022-2023学年高二下学期期中考试化学试题
四川省内江市第六中学2022-2023学年高二下学期期中考试化学试题重庆市2021年高考真题化学试题(已下线)专题20 结构与性质(已下线)专题20 结构与性质宁夏回族自治区石嘴山市平罗中学2023-2024学年高三上学期第四次月考理科综合试题
名校
解题方法
7 . 氧族元素是元素周期表中第VIA族元素,包含氧(O)、硫(S)、硒(Se)、碲(Te)、钋(Po)五种元素,它们及其化合物在生产、生活中有着广泛的应用。请回答下列问题:
(1)基态 原子的核外电子排布式为
原子的核外电子排布式为____ 。
(2)H2O、H2S、H2Se、H2Te的沸点由高到低的顺序为____ ,原因是____ 。
(3)SO 与SO
与SO 相比,键角较小的是
相比,键角较小的是___ (填离子符号),原因是____ 。
(4)依布硒是一种有机硒化物,具有良好的抗炎活性,其结构简式为 。依布硒分子中
。依布硒分子中 、C原子的杂化类型分别为
、C原子的杂化类型分别为____ 、____ 。
(5)国家速滑馆又称为“冰丝带”,所用的碲化镉(CdTe)“发电玻璃”被誉为“挂在墙上的油田”。碲化镉立方晶胞结构如图。

①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。已知晶胞中A、B原子的分数坐标分别为A(0,0,0)、B( ,
, ,
, ),则C点原子的分数坐标为
),则C点原子的分数坐标为____ 。
②碲化镉晶体的密度为ρg•cm-3,设NA为阿伏加德罗常数的值,则其晶胞边长为a=____ 。
(1)基态
 原子的核外电子排布式为
原子的核外电子排布式为(2)H2O、H2S、H2Se、H2Te的沸点由高到低的顺序为
(3)SO
 与SO
与SO 相比,键角较小的是
相比,键角较小的是(4)依布硒是一种有机硒化物,具有良好的抗炎活性,其结构简式为
 。依布硒分子中
。依布硒分子中 、C原子的杂化类型分别为
、C原子的杂化类型分别为(5)国家速滑馆又称为“冰丝带”,所用的碲化镉(CdTe)“发电玻璃”被誉为“挂在墙上的油田”。碲化镉立方晶胞结构如图。

①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。已知晶胞中A、B原子的分数坐标分别为A(0,0,0)、B(
 ,
, ,
, ),则C点原子的分数坐标为
),则C点原子的分数坐标为②碲化镉晶体的密度为ρg•cm-3,设NA为阿伏加德罗常数的值,则其晶胞边长为a=
您最近一年使用:0次
2022-05-26更新
|
367次组卷
|
4卷引用:四川省雅安中学2022-2023学年高二上学期期中考试化学试题
四川省雅安中学2022-2023学年高二上学期期中考试化学试题河北省沧衡八校联盟2021-2022学年高二下学期期中考试化学试题河北省沧州市任丘第一中学2021-2022学年高二下学期阶段考试(二)化学试题(已下线)期中模拟预测卷03(测试范围:选择性必修2+选择性必修3第1-2章)-2022-2023学年高二化学下学期期中期末考点大串讲(人教版2019)
名校
解题方法
8 . 金属元素Mg、Al、Ti、Fe、Cu等在电池、储氢材料、催化剂等方面都有广泛应用。请回答下列问题:
(1)Ti(BH4)2是一种储氢材料。BH 的空间构型是
的空间构型是____ ,H、B、Ti的电负性由小到大的顺序为____ 。
(2)原子核外运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用—
表示,与之相反的用— 表示,
表示,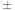
 即称为电子的自旋磁量子数。对于基态Fe原子,其价电子自旋磁量子数的代数和为
即称为电子的自旋磁量子数。对于基态Fe原子,其价电子自旋磁量子数的代数和为____ 。
(3)Cu(NO3)2是有机催化剂,其水溶液为天蓝色。使溶液呈现天蓝色的四水合铜离子,其空间构型为平面正方形,则Cu2+的杂化轨道类型为____ (填标号)。
A.dsp2 B.sp C.sp2 D.sp3
如图为一种Cu2+形成的配离子的结构,加热时该离子先失去的配位体是____ (填化学式),此时生成的配离子溶液的颜色为____ 色。

(4)已知Mg、A1、O三种元素组成的晶体结构如图所示,其晶胞由4个A型小晶格和4个B型小晶格构成,其中A13+和O2-都在小晶格内部,Mg2+部分在小晶格内部,部分在小晶格顶点。

该物质的化学式为____ ,Mg2+的配位数为____ ,两个Mg2+之间最近的距离是____ pm。
(1)Ti(BH4)2是一种储氢材料。BH
 的空间构型是
的空间构型是(2)原子核外运动的电子有两种相反的自旋状态,若一种自旋状态用+
 表示,与之相反的用—
表示,与之相反的用— 表示,
表示,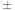
 即称为电子的自旋磁量子数。对于基态Fe原子,其价电子自旋磁量子数的代数和为
即称为电子的自旋磁量子数。对于基态Fe原子,其价电子自旋磁量子数的代数和为(3)Cu(NO3)2是有机催化剂,其水溶液为天蓝色。使溶液呈现天蓝色的四水合铜离子,其空间构型为平面正方形,则Cu2+的杂化轨道类型为
A.dsp2 B.sp C.sp2 D.sp3
如图为一种Cu2+形成的配离子的结构,加热时该离子先失去的配位体是

(4)已知Mg、A1、O三种元素组成的晶体结构如图所示,其晶胞由4个A型小晶格和4个B型小晶格构成,其中A13+和O2-都在小晶格内部,Mg2+部分在小晶格内部,部分在小晶格顶点。

该物质的化学式为
您最近一年使用:0次
2022-05-24更新
|
805次组卷
|
4卷引用:四川省成都市第七中学2022-2023学年高二上学期期末质量检测化学试题
四川省成都市第七中学2022-2023学年高二上学期期末质量检测化学试题四川省成都市第七中学2022-2023学年高二上学期期末考试化学试卷山东省济宁市2022届高三下学期第三次模拟考试化学试题(已下线)2022年山东省高考真题变式题(非选择题)
名校
解题方法
9 . 2022年春晚节目《只此青绿》取材于宋代名画《千里江山图》,该画描绘了山清水秀的美丽景色,历经千年色彩依然,其中青色来自蓝铜矿颜料[主要成分为Cu3(CO3)2(OH)2]。请回答下列问题:
(1)基态铜原子价电子排布式为_______ 。从原子结构角度分析,第二电离能I2(Fe)与I2(Cu)的关系是I2(Fe)_______ I2(Cu) (填“>”“<”或“=”),并解释有关原因_______ 。
(2) 的空间构型为
的空间构型为_______ 。
(3)我国科学家制取了一种铜的配合物如图所示,该配合物中四种非金属元素电负性由大到小的顺序是_______ (填元素符号),该配合物中采用sp2杂化的碳原子与sp3杂化的碳原子个数比为_______ 。
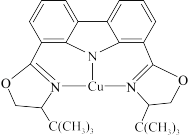
(4)黄铜矿是主要的炼铜原料,晶胞结构如下图1所示,晶胞中S原子的投影位置如图2所示。
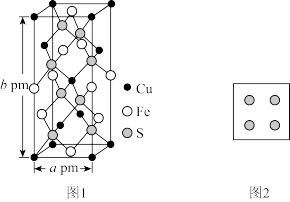
①Fe3+周围距离最近的S2-的个数为_______ 。
②该晶胞上下底面均为正方形,侧面与底面垂直,晶胞参数如图所示,晶胞的密度为ρ g/cm3,则阿伏加德罗常数(NA)为_______ mol-1(用a、b、ρ表示,并化成最简)。
(1)基态铜原子价电子排布式为
(2)
 的空间构型为
的空间构型为(3)我国科学家制取了一种铜的配合物如图所示,该配合物中四种非金属元素电负性由大到小的顺序是

(4)黄铜矿是主要的炼铜原料,晶胞结构如下图1所示,晶胞中S原子的投影位置如图2所示。

①Fe3+周围距离最近的S2-的个数为
②该晶胞上下底面均为正方形,侧面与底面垂直,晶胞参数如图所示,晶胞的密度为ρ g/cm3,则阿伏加德罗常数(NA)为
您最近一年使用:0次
2022-05-04更新
|
733次组卷
|
4卷引用:四川省南充高级中学2021-2022学年高二下学期期中考试化学试题
四川省南充高级中学2021-2022学年高二下学期期中考试化学试题安徽省淮北市2022届高三第二次模拟考试理科综合化学试题(已下线)专项17 物质结构与性质综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)山东省菏泽市单县第二中学2021-2022学年高二下学期慧光班段考化学试题
名校
解题方法
10 . 主族元素N、F、Si、As、Se、Cl等的某些化合物对工农业生产意义重大,回答下列问题:
(1)Si3N4陶瓷是世界上最坚硬的物质之一,具有高强度、低密度、耐高温等性质,其属于_______ 晶体;SiCl4中Si采取的杂化类型为_______ 。
(2)O、F、Cl电负性由大到小的顺序为_______ ;OF2分子的空间构型为_______ ;OF2的熔、沸点低于Cl2O,原因是_______ 。
(3)Se元素基态原子的原子核外电子排布式为_______ ;As的第一电离能比Se的第一电离能大的原因为_______ 。
(4)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有_______ 个XeF2分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为( ,
, ,
, )。已知Xe-F键长为rpm,则B点原子的分数坐标为
)。已知Xe-F键长为rpm,则B点原子的分数坐标为_______ ;晶胞中A、B间距离d=_______ pm。
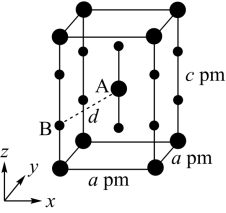
(1)Si3N4陶瓷是世界上最坚硬的物质之一,具有高强度、低密度、耐高温等性质,其属于
(2)O、F、Cl电负性由大到小的顺序为
(3)Se元素基态原子的原子核外电子排布式为
(4)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有
 ,
, ,
, )。已知Xe-F键长为rpm,则B点原子的分数坐标为
)。已知Xe-F键长为rpm,则B点原子的分数坐标为
您最近一年使用:0次
2022-05-02更新
|
860次组卷
|
7卷引用:四川省绵阳南山中学2022-2023学年高三上学期入学考试理综化学试题
四川省绵阳南山中学2022-2023学年高三上学期入学考试理综化学试题陕西省汉中市2022届高三教学质量第二次检测考试理科综合能力测试化学试题(已下线)专项17 物质结构与性质综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)(已下线)专题18物质结构与性质(选修)-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题17物质结构与性质(综合题)-2022年高考真题+模拟题汇编(全国卷)(已下线)专题18物质结构与性质(选修)-五年(2018~2022)高考真题汇编(全国卷)山东省枣庄市第三中学2022-2023学年高三上学期期中考试化学试题



