1 . 2020年,智能材料已大量涌现,为生物医疗、国防军事以及航空航天等领域发展提供支撑。
(1)快离子导体是具有优良离子导电能力的固体电解质。反应 的产物分子中形成配位键提供孤电子对的配位原子名称是
的产物分子中形成配位键提供孤电子对的配位原子名称是______ 。
(2)第三代半导体材料氮化镓(GaN)适合于制作高温、高频、抗辐射及大功率器件,通常称为高温半导体材料。基态Ga原子价电子排布图为______ ,第一电离能介于硼和氮之间的第二周期元素有______ 种。
(3)金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”。钛(Ti)在元素周期表中位于______ (周期,族,区),钛(Ti)的基态原子M能层中有______ 种空间运动状态的电子。
(4)镍能形成多种配合物,如正四面体形的 和正方形的
和正方形的 、正八面体形的
、正八面体形的 等。下列说法正确的有
等。下列说法正确的有______ (填标号)。
A.CO与 互为等电子体,其中CO分子内
互为等电子体,其中CO分子内 键和
键和 键个数之比为1∶2
键个数之比为1∶2
B. 在形成配合物时,其配位数只能为4
在形成配合物时,其配位数只能为4
C.沸点: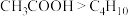 ,因为
,因为 分子间范德华力更强
分子间范德华力更强
D.键角: ,因为
,因为 的成键电子对间的排斥力更大
的成键电子对间的排斥力更大
E.极性:F―C>Cl―C,因此酸性
(5)一种四方结构( )的超导化合物汞钡铜氧晶体的晶胞如图所示。
)的超导化合物汞钡铜氧晶体的晶胞如图所示。______  (设
(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)快离子导体是具有优良离子导电能力的固体电解质。反应
 的产物分子中形成配位键提供孤电子对的配位原子名称是
的产物分子中形成配位键提供孤电子对的配位原子名称是(2)第三代半导体材料氮化镓(GaN)适合于制作高温、高频、抗辐射及大功率器件,通常称为高温半导体材料。基态Ga原子价电子排布图为
(3)金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”。钛(Ti)在元素周期表中位于
(4)镍能形成多种配合物,如正四面体形的
 和正方形的
和正方形的 、正八面体形的
、正八面体形的 等。下列说法正确的有
等。下列说法正确的有A.CO与
 互为等电子体,其中CO分子内
互为等电子体,其中CO分子内 键和
键和 键个数之比为1∶2
键个数之比为1∶2B.
 在形成配合物时,其配位数只能为4
在形成配合物时,其配位数只能为4C.沸点:
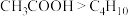 ,因为
,因为 分子间范德华力更强
分子间范德华力更强D.键角:
 ,因为
,因为 的成键电子对间的排斥力更大
的成键电子对间的排斥力更大E.极性:F―C>Cl―C,因此酸性

(5)一种四方结构(
 )的超导化合物汞钡铜氧晶体的晶胞如图所示。
)的超导化合物汞钡铜氧晶体的晶胞如图所示。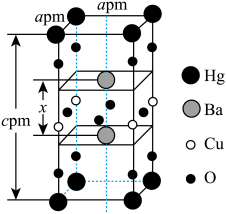
 (设
(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
名校
2 .  为阿伏加德罗常数的值。下列叙述错误的是
为阿伏加德罗常数的值。下列叙述错误的是
 为阿伏加德罗常数的值。下列叙述错误的是
为阿伏加德罗常数的值。下列叙述错误的是A.1mol 中 中 键的个数为 键的个数为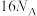 |
B.46g 中 中 杂化的碳原子数为 杂化的碳原子数为 |
C.1L 的HCN溶液中, 的HCN溶液中,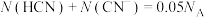 |
D.1mol 晶体中含有 晶体中含有 共价键 共价键 |
您最近一年使用:0次
3 . 已知 可形成配离子
可形成配离子 、
、 、
、 。在试管中进行下列实验:
。在试管中进行下列实验:
 可形成配离子
可形成配离子 、
、 、
、 。在试管中进行下列实验:
。在试管中进行下列实验:
A.上述三种配离子中 的配位数不完全相同 的配位数不完全相同 |
B. 和 和 中配位原子均为N 中配位原子均为N |
C.溶度积常数: |
D.稳定性: |
您最近一年使用:0次
名校
解题方法
4 . W、X、Y、Z为元素周期表中的前四周期元素,原子的最外层电子数之和为12。W与X同周期相邻,X的基态原子价层电子排布为 ;Y与Z同周期,
;Y与Z同周期,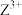 的
的 轨道半充满;四种元素可形成化合物
轨道半充满;四种元素可形成化合物 。回答下列问题:
。回答下列问题:
(1)W的三种单质分别是共价晶体、分子晶体、混合型晶体,则三种单质分别是___________ 、___________ 、___________ 。
(2)单质 化学性质很稳定,其原因是
化学性质很稳定,其原因是___________ 。 分子中
分子中 键与
键与 键的数目之比为
键的数目之比为___________ 。
(3)阴离子 的结构如图所示,五个X原子位于同一平面,则X原子均采用
的结构如图所示,五个X原子位于同一平面,则X原子均采用___________ 杂化,每个X原子未参与杂化的___________ 轨道垂直于五元环平面,相互平行重叠形成大 键,
键, 中的
中的 键总数为
键总数为___________ 个,形成大 键的电子共有
键的电子共有___________ 个。 的化学式为
的化学式为___________ ,它在水中可以电离出配离子 。该配离子的中心离子是
。该配离子的中心离子是___________ ,配位数是___________ 。
(5) 有剧毒,但
有剧毒,但 却允许用作食盐的抗结剂,其最大使用量为
却允许用作食盐的抗结剂,其最大使用量为 (以配离子计),原因是
(以配离子计),原因是___________ 。
 ;Y与Z同周期,
;Y与Z同周期,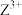 的
的 轨道半充满;四种元素可形成化合物
轨道半充满;四种元素可形成化合物 。回答下列问题:
。回答下列问题:(1)W的三种单质分别是共价晶体、分子晶体、混合型晶体,则三种单质分别是
(2)单质
 化学性质很稳定,其原因是
化学性质很稳定,其原因是 分子中
分子中 键与
键与 键的数目之比为
键的数目之比为(3)阴离子
 的结构如图所示,五个X原子位于同一平面,则X原子均采用
的结构如图所示,五个X原子位于同一平面,则X原子均采用 键,
键, 中的
中的 键总数为
键总数为 键的电子共有
键的电子共有
 的化学式为
的化学式为 。该配离子的中心离子是
。该配离子的中心离子是(5)
 有剧毒,但
有剧毒,但 却允许用作食盐的抗结剂,其最大使用量为
却允许用作食盐的抗结剂,其最大使用量为 (以配离子计),原因是
(以配离子计),原因是
您最近一年使用:0次
名校
解题方法
5 . 下列有关物质结构和性质的说法错误的是
| A.有机物分子中手性碳所连4个原子一定不同 |
| B.互为手性异构体的两种药物,其药效差异可能很大 |
| C.邻羟基苯甲酸的沸点低于对羟基苯甲酸是因为二者形成的氢键不同 |
D.“杯酚”与 通过分子间作用力形成超分子可实现“分子识别” 通过分子间作用力形成超分子可实现“分子识别” |
您最近一年使用:0次
6 . 铁及其化合物在生产生活中应用广泛。回答下列问题:
(1)基态Fe原子的价电子排布式是___________ 。
(2) 溶液与KSCN溶液混合,溶液呈红色,常用于检验
溶液与KSCN溶液混合,溶液呈红色,常用于检验 。
。
①基态K、S、N原子第一电离能大小顺序是___________ , 的空间构型是
的空间构型是___________ 。
②从结构角度分析 易被氧化成
易被氧化成 的原因:
的原因:___________ 。
(3)邻二氮菲( )与
)与 形成图1所示的红色配合物离子,常用于测定
形成图1所示的红色配合物离子,常用于测定 的浓度。
的浓度。___________ 。
②与邻二氮菲相比,配合物离子中∠CNC较___________ (填“大”“小”或“相同”),原因是___________ 。
③测定 浓度时,加入盐酸使溶液pH不断减小,红色逐渐变浅。从化学键角度分析原因:
浓度时,加入盐酸使溶液pH不断减小,红色逐渐变浅。从化学键角度分析原因:___________ 。
(4)铁和碳能形成图2所示的晶胞。该晶胞可以看成是在铁晶胞中插入若干碳原子,但晶胞体积不变。铁碳晶体的化学式是___________ ,铁晶体转化为铁碳晶体时晶体密度净增___________ %(结果保留2位有效数字)。
(1)基态Fe原子的价电子排布式是
(2)
 溶液与KSCN溶液混合,溶液呈红色,常用于检验
溶液与KSCN溶液混合,溶液呈红色,常用于检验 。
。①基态K、S、N原子第一电离能大小顺序是
 的空间构型是
的空间构型是②从结构角度分析
 易被氧化成
易被氧化成 的原因:
的原因:(3)邻二氮菲(
 )与
)与 形成图1所示的红色配合物离子,常用于测定
形成图1所示的红色配合物离子,常用于测定 的浓度。
的浓度。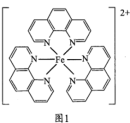
②与邻二氮菲相比,配合物离子中∠CNC较
③测定
 浓度时,加入盐酸使溶液pH不断减小,红色逐渐变浅。从化学键角度分析原因:
浓度时,加入盐酸使溶液pH不断减小,红色逐渐变浅。从化学键角度分析原因:(4)铁和碳能形成图2所示的晶胞。该晶胞可以看成是在铁晶胞中插入若干碳原子,但晶胞体积不变。铁碳晶体的化学式是

您最近一年使用:0次
解题方法
7 . 氟及其化合物用途非常广泛,自然界中氟多以化合态形式存在,形成的化合物有:N2F2、HBF4、 等。回答下列问题:
等。回答下列问题:
(1)氟元素基态原子最高能级电子的电子云形状为___________ ,下列为氟原子激发态的电子排布式的是___________ (填序号)。
A.1s22s22p43s1 B.1s22s22p6 C.1s22s22p5 D.1s22s12p6
(2)F与N可形成化合物N2F2,分子中各原子均满足8电子稳定结构。
①分子中氮原子的杂化方式为___________ 。
②N2F2结构式为___________ ,其分子中 键与
键与 键的数目之比为
键的数目之比为___________ 。
(3)氟硼酸(HBF4,属于强酸)可由HF和BF3化合生成,常用于替代浓硫酸作铅蓄电池的电解质溶液,从化学键形成角度分析HF与BF3能化合的原因___________ 。
(4)石墨与F2在450℃反应,石墨层间插入F得到层状结构化合物 ,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比,
,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比, 的导电性
的导电性___________ (填“增强”或“减弱”), 中C-C键的键长比石墨中C-C键的
中C-C键的键长比石墨中C-C键的___________ (填“长”或“短”)。___________ ,设NA为阿伏加德罗常数的值则该晶体的密度为___________  (列出计算式)。
(列出计算式)。
 等。回答下列问题:
等。回答下列问题:(1)氟元素基态原子最高能级电子的电子云形状为
A.1s22s22p43s1 B.1s22s22p6 C.1s22s22p5 D.1s22s12p6
(2)F与N可形成化合物N2F2,分子中各原子均满足8电子稳定结构。
①分子中氮原子的杂化方式为
②N2F2结构式为
 键与
键与 键的数目之比为
键的数目之比为(3)氟硼酸(HBF4,属于强酸)可由HF和BF3化合生成,常用于替代浓硫酸作铅蓄电池的电解质溶液,从化学键形成角度分析HF与BF3能化合的原因
(4)石墨与F2在450℃反应,石墨层间插入F得到层状结构化合物
 ,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比,
,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比, 的导电性
的导电性 中C-C键的键长比石墨中C-C键的
中C-C键的键长比石墨中C-C键的
 (列出计算式)。
(列出计算式)。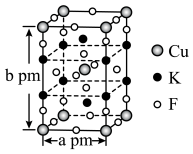
您最近一年使用:0次
名校
解题方法
8 . 秦始皇帝陵博物院首次在兵马俑的彩绘中发现了古人人工合成的“中国蓝”“中国紫”颜料。通过对这些颜料的研究发现,其成分主要是钡和铜的硅酸盐(BaCuSixOy) 。
回答下列问题:
(1)“中国蓝”的发色与硫酸铜溶液呈天蓝色类似,都是由于形成了[Cu(H2O)4]2+,该配离子中Cu2+提供_______ ,配位原子是_______ ,1 mol [Cu(H2O)4]2+中σ键的数目为_________ 。
(2)写出向硫酸铜溶液里逐滴加入氨水过程中沉淀溶解的离子方程式_______________ ,再向溶液中加入乙醇,会析出深蓝色晶体____________ (写出化学式)。
(3)“中国蓝”“中国紫”中存在 四面体结构,其中Si原子采取的杂化方式为
四面体结构,其中Si原子采取的杂化方式为_______ 。
(4)BaO的熔沸点_____ MgO(填“>”“<”“=”),原因是______________ 。
(5)立方CuO晶胞结构如图所示。其中Cu2+的配位数为_______ 。NA代表阿伏加德罗常数的值,晶胞参数为a pm,则其晶体密度为___________ g·cm-3。
回答下列问题:
(1)“中国蓝”的发色与硫酸铜溶液呈天蓝色类似,都是由于形成了[Cu(H2O)4]2+,该配离子中Cu2+提供
(2)写出向硫酸铜溶液里逐滴加入氨水过程中沉淀溶解的离子方程式
(3)“中国蓝”“中国紫”中存在
 四面体结构,其中Si原子采取的杂化方式为
四面体结构,其中Si原子采取的杂化方式为(4)BaO的熔沸点
(5)立方CuO晶胞结构如图所示。其中Cu2+的配位数为

您最近一年使用:0次
名校
9 . 某种新型储氢材料(摩尔质量为188g∙mol–1)的立方晶胞如图,该晶胞可储存6个氢原子。已知M核内中子数比质子数多4,标准状况下氢气的密度为ρg∙cm–3,NA表示阿伏加德罗常数的值。下列说法正确的是

| A.晶胞中[M(NH3)6]n+和[BH4]–的配位数相同 |
| B.M离子最外层电子排布式为3d64s2 |
C.在晶胞体对角线的一维空间上会出现 的排布规律 的排布规律 |
D.该材料的储氢能力[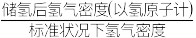 ]为 ]为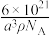 |
您最近一年使用:0次
解题方法
10 . X、Y、Z、R、W为原子序数依次增大的前20号主族元素,X元素原子失去一个电子后是“裸露”质子;R原子最外层电子数是其内层电子总数的一半;X、Y、Z、R形成的化合物表示为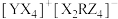 ;W是前20号元素中金属性最强的,下列正确的是
;W是前20号元素中金属性最强的,下列正确的是
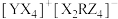 ;W是前20号元素中金属性最强的,下列正确的是
;W是前20号元素中金属性最强的,下列正确的是
A.离子半径: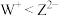 |
| B.元素X、Y、Z形成的化合物可能属于离子化合物 |
C.简单氢化物的沸点: |
D.如上图所示,该物质中,冠醚和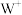 之间的配位键是离子键 之间的配位键是离子键 |
您最近一年使用:0次



