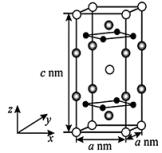
1 . 原子序数依次增大的前四周期元素X、Y、Z、W、T可形成如图所示的化合物。其中仅有Y和Z位于同一周期,且基态Z原子核外有3个未成对电子;W元素形成的单质在常温下为气体;T位于周期表中ds区,其单质在常温下为红色固体。下列说法正确的是

| A.第一电离能:Y>Z>T |
| B.电负性:Z>Y>X |
| C.该化合物中存在配位键,由T提供孤电子对 |
| D.图示结构中的两个六元环和两个五元环均为平面结构 |
您最近一年使用:0次
名校
解题方法
2 . 我国学者最近研发出一种以铝为负极、石墨烯薄膜( )为正极的新型铝-石墨烯电池,
)为正极的新型铝-石墨烯电池,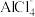 可在石墨烯薄膜上嵌入或脱嵌,离子液体
可在石墨烯薄膜上嵌入或脱嵌,离子液体 作电解质,阴离子有
作电解质,阴离子有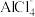 、
、 ,阳离子为
,阳离子为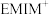 (
(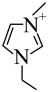 ),放电机理如图所示。下列说法错误的是
),放电机理如图所示。下列说法错误的是

A.放电时正极的电极反应: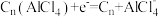 |
B.该离子液体可用于钢制品上电镀铝,阴极的电极反应为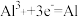 |
C. 中存在配位键 中存在配位键 |
D.离子液体中的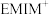 不参与反应,只起传递离子的作用 不参与反应,只起传递离子的作用 |
您最近一年使用:0次
3 . 无水三氯化铬( )是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧化。实验室利用反应
)是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧化。实验室利用反应 制取
制取 的
的 (俗称光气)有毒,遇水发生水解,实验所需装置如图所示。
(俗称光气)有毒,遇水发生水解,实验所需装置如图所示。
(1)上述装置的正确连接顺序为___________ (填字母,按气流方向从左到右)。
(2)装置A中所盛放的试剂是___________ ,装置A中竖直长玻璃管的作用是___________ 。装置D中n瓶的作用是___________ 。实验过程中为了避免装置A中长玻璃管中液面上升,可以采用的方法为___________ (填序号)。
①对m处导管进行加热 ②将m处导管加粗 ③持续通入氮气
(3)装置E中发生反应的离子方程式为___________ 。无水 的作用是
的作用是___________ 。
(4)已知 分子中各原子均满足最外层8电子稳定结构,则1mol
分子中各原子均满足最外层8电子稳定结构,则1mol 含有
含有 键的个数为
键的个数为___________ ( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(5) 的结构有三种,且铬的配位数均为6,等物质的量的三种物质电离出的氯离子数目之比为3∶2∶1,对应的颜色分别为紫色、浅绿色和蓝绿色。其中浅绿色的结构中配离子的化学式为
的结构有三种,且铬的配位数均为6,等物质的量的三种物质电离出的氯离子数目之比为3∶2∶1,对应的颜色分别为紫色、浅绿色和蓝绿色。其中浅绿色的结构中配离子的化学式为___________ 。哈勃-韦斯(Haber-Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。则
___________ (填“能”或“不能”)催化双氧水分解。
 )是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧化。实验室利用反应
)是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧化。实验室利用反应 制取
制取 的
的 (俗称光气)有毒,遇水发生水解,实验所需装置如图所示。
(俗称光气)有毒,遇水发生水解,实验所需装置如图所示。
(1)上述装置的正确连接顺序为
(2)装置A中所盛放的试剂是
①对m处导管进行加热 ②将m处导管加粗 ③持续通入氮气
(3)装置E中发生反应的离子方程式为
 的作用是
的作用是(4)已知
 分子中各原子均满足最外层8电子稳定结构,则1mol
分子中各原子均满足最外层8电子稳定结构,则1mol 含有
含有 键的个数为
键的个数为 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。(5)
 的结构有三种,且铬的配位数均为6,等物质的量的三种物质电离出的氯离子数目之比为3∶2∶1,对应的颜色分别为紫色、浅绿色和蓝绿色。其中浅绿色的结构中配离子的化学式为
的结构有三种,且铬的配位数均为6,等物质的量的三种物质电离出的氯离子数目之比为3∶2∶1,对应的颜色分别为紫色、浅绿色和蓝绿色。其中浅绿色的结构中配离子的化学式为
您最近一年使用:0次
名校
解题方法
4 . 葡萄糖的银镜反应需要配制银氨溶液,具体步骤如下:
步骤1:向试管中加入1 mL2%AgNO3溶液,边振荡边滴加2%氨水,观察到有白色沉淀产生并迅速转化为灰褐色。
步骤2:向试管中继续滴加2%氨水,观察到沉淀完全溶解。
步骤1:向试管中加入1 mL2%AgNO3溶液,边振荡边滴加2%氨水,观察到有白色沉淀产生并迅速转化为灰褐色。
步骤2:向试管中继续滴加2%氨水,观察到沉淀完全溶解。

A.步骤1产生白色沉淀的离子反应方程式为 |
| B.图中所示银的晶胞中Ag原子周围等距且紧邻的Ag原子有12个 |
C.步骤2中沉淀溶解是因为生成了银氨配合物, 中含有 中含有 键 键 |
D.经过步骤1步骤2两步之后, 一共消耗 一共消耗 |
您最近一年使用:0次
名校
解题方法
5 . 按要求回答下列问题:
(1)基态钛原子核外共有________ 种空间运动状态不相同的电子。Cu在周期表中的位置为________________________ ,基态Ni2+的价层电子排布式为________________________ ,Zn位于元素周期表的________________ 区。
(2)分子极性:CH4________ NH3(填“>”或“<”),熔沸点:CH4________ NH3(填“>”或“<”),键角:CH4________ NH3(填“>”或“<”)。
(3)组成为 ,配位数为6的晶体有两种。其中一种物质X呈绿色。实验表明,
,配位数为6的晶体有两种。其中一种物质X呈绿色。实验表明, 恰好与
恰好与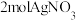 反应生成沉淀。则X的化学式为
反应生成沉淀。则X的化学式为________ 。(表示出内界和外界)
(1)基态钛原子核外共有
(2)分子极性:CH4
(3)组成为
 ,配位数为6的晶体有两种。其中一种物质X呈绿色。实验表明,
,配位数为6的晶体有两种。其中一种物质X呈绿色。实验表明, 恰好与
恰好与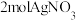 反应生成沉淀。则X的化学式为
反应生成沉淀。则X的化学式为
您最近一年使用:0次
名校
解题方法
6 . 某溶液吸收CO的反应为[Cu(NH3)2]++CO+NH3 [Cu(NH3)3CO]+,下列说法错误的是
[Cu(NH3)3CO]+,下列说法错误的是
 [Cu(NH3)3CO]+,下列说法错误的是
[Cu(NH3)3CO]+,下列说法错误的是| A.Cu位于周期表的ds区 |
| B.1mol[Cu(NH3)2]+中含有6molσ键 |
| C.[Cu(NH3)3CO]+中H—N—H的键角比NH3中的大 |
D.[Cu(NH3)3CO]+的结构表示为 |
您最近一年使用:0次
名校
解题方法
7 . 下列关于物质结构和性质的叙述错误的是
| A.利用杯酚分离C60和C70,借助的是分子间作用力形成超分子 |
| B.石墨C原子所有p轨道相互平行重叠,电子可自由移动,因此石墨有类似金属晶体的导电性 |
| C.化学式为[TiCl(H2O)5]Cl2·H2O的配合物,中心离子Ti3+的配位数为6 |
D.已知二茂铁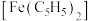 熔点是 熔点是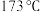 (在 (在 时开始升华),沸点是 时开始升华),沸点是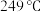 ,不溶于水,易溶于苯等非极性溶剂,在二茂铁结构中, ,不溶于水,易溶于苯等非极性溶剂,在二茂铁结构中,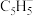 与 与 之间是以离子键相结合 之间是以离子键相结合 |
您最近一年使用:0次
名校
解题方法
8 . 磷化铟晶体属于立方晶系,其晶胞结构如图1所示,晶胞参数为a nm,晶胞中所有原子沿y轴的投影如图2所示,设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是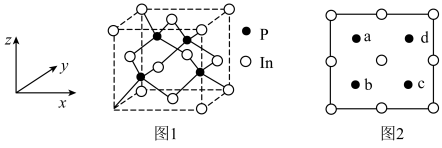
| A.该晶体的化学式为InP | B.晶体中In的配位数为4 |
C.晶体密度为 | D.晶胞中,a、b原子间间距与a、c不等 |
您最近一年使用:0次
名校
9 . 关于晶体中作用力的叙述,错误的是
| A.共价晶体中可以同时存在范德华力、共价键和配位键 |
| B.分子晶体中可以同时存在范德华力、氢键和共价键 |
| C.混合晶体中可以同时存在共价键、范德华力和类似金属键的作用力 |
| D.离子晶体中可能同时存在离子键、共价键、氢键、配位键和范德华力 |
您最近一年使用:0次
10 . 铁及其化合物在生活、生产中有重要应用。回答下列问题:
(1)乳酸亚铁 是一种常用的补铁剂。
是一种常用的补铁剂。
① 的价层电子排布式是
的价层电子排布式是___________ 。
②乳酸分子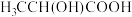 中
中 的杂化方式为
的杂化方式为___________ ;该分子中有多种 键,其中极性最强的是
键,其中极性最强的是___________ 。
A.C-C键 B. 键 C.
键 C. 键 D.
键 D. 键
键
(2)某含 的结晶水合物的结构片段如图所示(球与球之间的短线代表单键或双键)。
的结晶水合物的结构片段如图所示(球与球之间的短线代表单键或双键)。___________ ,其中 和
和 之间的作用力类型为
之间的作用力类型为___________ 。
(3)南开大学某课题组成功合成无机二茂铁的配离子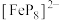 ,其中环状配体
,其中环状配体 (4个
(4个 原子共平面)以
原子共平面)以 电子参与配位,结构如图。配体
电子参与配位,结构如图。配体 形成的大
形成的大 键可表示为
键可表示为___________ , 原子的价层孤电子对占据
原子的价层孤电子对占据___________ (填标号)。 杂化轨道 B.
杂化轨道 B. 杂化轨道 C.3p轨道 D.
杂化轨道 C.3p轨道 D. 轨道
轨道
(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。由铁、钾、硒形成的一种超导材料的晶胞结构如下图所示,晶胞棱边夹角均为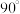 ,晶胞中部分原子的分数坐标如下表所示。
,晶胞中部分原子的分数坐标如下表所示。
距离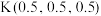 最近的
最近的 的数目为
的数目为___________ ,该晶胞在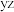 平面投影为
平面投影为___________ (填标号)。
(1)乳酸亚铁
 是一种常用的补铁剂。
是一种常用的补铁剂。①
 的价层电子排布式是
的价层电子排布式是②乳酸分子
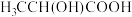 中
中 的杂化方式为
的杂化方式为 键,其中极性最强的是
键,其中极性最强的是A.C-C键 B.
 键 C.
键 C. 键 D.
键 D. 键
键(2)某含
 的结晶水合物的结构片段如图所示(球与球之间的短线代表单键或双键)。
的结晶水合物的结构片段如图所示(球与球之间的短线代表单键或双键)。
 和
和 之间的作用力类型为
之间的作用力类型为(3)南开大学某课题组成功合成无机二茂铁的配离子
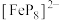 ,其中环状配体
,其中环状配体 (4个
(4个 原子共平面)以
原子共平面)以 电子参与配位,结构如图。配体
电子参与配位,结构如图。配体 形成的大
形成的大 键可表示为
键可表示为 原子的价层孤电子对占据
原子的价层孤电子对占据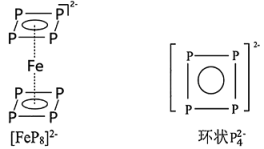
 杂化轨道 B.
杂化轨道 B. 杂化轨道 C.3p轨道 D.
杂化轨道 C.3p轨道 D. 轨道
轨道(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。由铁、钾、硒形成的一种超导材料的晶胞结构如下图所示,晶胞棱边夹角均为
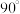 ,晶胞中部分原子的分数坐标如下表所示。
,晶胞中部分原子的分数坐标如下表所示。| 原子坐标 | x | y | z |
|
| K | 0.5 | 0.5 | 0.5 | |
| Fe | 0 | 0.5 | m | |
| Se | 0 | 0 | n | |
| 注:m、n均≠0 | ||||
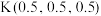 最近的
最近的 的数目为
的数目为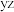 平面投影为
平面投影为A.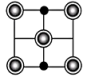 B.
B.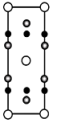 C.
C.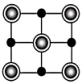 D.
D.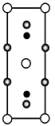
您最近一年使用:0次