解题方法
1 . 下列有关化学键类型的判断不正确的是
| A.s—sσ键与s—pσ键的对称性不同 |
| B.分子极性:H—F>H—Cl>H—Br>H—I |
C. 只有s—sp3σ键,其空间构型是三角锥形 只有s—sp3σ键,其空间构型是三角锥形 |
| D.H—F键是s—pσ键 |
您最近一年使用:0次
2 . 某种镁盐具有良好的电化学性能,其阴离子结构如下图所示。W、X、Y、Z、Q是核电荷数依次增大的短周期元素,W、Y原子序数之和等于Z,Y原子价电子数是Q原子价电子数的2倍。下列说法错误的是
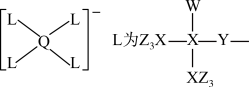
| A.W与X的化合物为极性分子 | B.第一电离能Z>X>Y |
| C.Q的氧化物是两性氧化物 | D.该阴离子中含有配位键 |
您最近一年使用:0次
3 . X、Y、Z、W、Q为原子序数依次增大的短周期主族元素,X的原子半径小于Y的原子半径,Z基态原子核外有3个未成对电子,Y的核外电子数与Z的价层电子数相等,Q2是氧化性最强的单质,下列说法正确的是
| A.键能:Z2<W2<Q2 | B.YQ3、ZQ3 均为非极性分子 |
| C.沸点:X2W<XQ | D.同周期中第一电离能介于Y和Z之间的元素有3种 |
您最近一年使用:0次
2024-03-09更新
|
352次组卷
|
4卷引用:山东省烟台市2023-2024学年高三上学期期末考试化学试题
4 . 短周期元素X、Y、Z、W原子序数依次增大.基态X、Z、W原子均有两个未成对电子,W与Z同主族.下列说法错误的是
| A.第三电离能:Z>Y>X | B.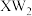 、 、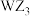 均为非极性分子 均为非极性分子 |
| C.Y、Z形成的化合物只有5种 | D.最高价含氧酸的酸性W大于X |
您最近一年使用:0次
名校
5 . 下列说法正确的是
A.电子排布式(22Ti) 违反了洪特规则 违反了洪特规则 |
B.因为共价键的键能 ,所以沸点 ,所以沸点 |
| C.HCHO为非极性分子 |
D.乙烯分子中,碳原子的 杂化轨道形成 杂化轨道形成 键,未杂化的 键,未杂化的 轨道形成 轨道形成 键 键 |
您最近一年使用:0次
2024-02-27更新
|
205次组卷
|
2卷引用:山东省青岛第五十八中学2023-2024学年高二上学期期末化学试卷
解题方法
6 . BF3与一定量的水形成(H2O)2•BF3,一定条件下(H2O)2•BF3可发生如图转化,下列说法正确的是
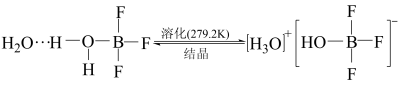
A.BF3和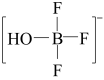 中B原子均采用sp2杂化轨道成键 中B原子均采用sp2杂化轨道成键 |
| B.(H2O)2•BF3分子中存在氢键和配位键 |
| C.(H2O)2•BF3中的所有元素都位于元素周期表中的p区 |
| D.BF3、NF3分子中的原子个数比相同,两者都是极性分子 |
您最近一年使用:0次
2024-02-26更新
|
350次组卷
|
4卷引用:山东省聊城颐中外国语学校2023-2024学年高二下学期第一次质量检测化学试题
解题方法
7 . 三氟化氯(ClF3)是极强助燃剂,能自耦电离:2ClF3 ClF
ClF +ClF
+ClF ,其分子空间结构如图。下列推测合理的是
,其分子空间结构如图。下列推测合理的是
 ClF
ClF +ClF
+ClF ,其分子空间结构如图。下列推测合理的是
,其分子空间结构如图。下列推测合理的是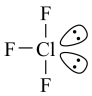
| A.ClF3分子是含有极性键的非极性分子 |
| B.BrF3比ClF3更易发生自耦电离 |
| C.ClF3水解反应的产物为HCl和HFO |
D.ClF 与H2O、ClF 与H2O、ClF 与CCl4的空间结构分别相同 与CCl4的空间结构分别相同 |
您最近一年使用:0次
解题方法
8 . 下列属于既含极性键又含非极性键的极性分子是
A. | B. | C. | D. |
您最近一年使用:0次
名校
9 . 对下列一些实验事实的理论解释,错误的是
| 选项 | 实验事实 | 理论解释 |
| A | P原子的第一电离能大于S原子 | 磷原子的半径比硫原子的半径大 |
| B | 乙烯的化学性质比乙烷活泼 | 乙烯分子结构中存在π键 |
| C | 向加入过量氨水的硫酸铜溶液中加入乙醇,将析出深蓝色晶体 | 乙醇的加入降低了[Cu(NH3)4]SO4·H2O的溶解度 |
| D | HCl气体极易溶于水 | HCl和H2O均为极性分子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 二茂铁是由环戊二烯阴离子( ,平面结构)与
,平面结构)与 形成的分子,其结构如下图所示。下列说法正确的是
形成的分子,其结构如下图所示。下列说法正确的是

 ,平面结构)与
,平面结构)与 形成的分子,其结构如下图所示。下列说法正确的是
形成的分子,其结构如下图所示。下列说法正确的是
A.铁元素位于 区 区 |
B.二茂铁中 与环戊二烯阴离子之间为离子键 与环戊二烯阴离子之间为离子键 |
| C.二茂铁易溶于苯、乙醚等有机溶剂 |
D.环戊二烯阴离子中碳原子的杂化方式有 和 和 |
您最近一年使用:0次
2024-02-02更新
|
162次组卷
|
2卷引用:山东省济南市2023-2024学年高二上学期1月期末化学试题



