1 . 对下列事实的解释不正确 的是
| 选项 | 事实 | 解释 |
| A | 气态氢化物稳定性: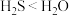 |  分子间存在氢键, 分子间存在氢键, 分子间不存在氢键 分子间不存在氢键 |
| B | 熔点:石英>干冰 | 石英是共价晶体,干冰是分子晶体;共价键比分子间作用力强 |
| C | 酸性: |  的电负性大于 的电负性大于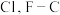 的极性大于 的极性大于 ,使 ,使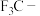 的极性大于 的极性大于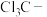 的极性,导致分子中 的极性,导致分子中 极性: 极性: |
| D |  分子中的共价键是 分子中的共价键是 键 键 |  价电子排布为 价电子排布为 原子结合为 原子结合为 时,两个原子的 时,两个原子的 轨道“头碰头”重叠 轨道“头碰头”重叠 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 .  是9种中学化学中常见的元素。
是9种中学化学中常见的元素。
(1)原子结构与元素性质
①基态氢原子中,核外电子的电子云轮廓图形状为________ 。
②3种元素 中,离子半径最小的是
中,离子半径最小的是______ (填离子符号)。
③基态 的价层电子轨道表示式为
的价层电子轨道表示式为________ 。
(2)微粒间相互作用与物质性质
①胆矾( )的结构示意图如下所示。
)的结构示意图如下所示。 与
与 与
与 的作用力分别为
的作用力分别为______ 和______ 。
② 的VSEPR模型为
的VSEPR模型为______ , 的分子空间构型为
的分子空间构型为________ , 是
是________ (填“极性”或“非极性”)分子。
③写出 电子式:
电子式:________ , 形成过程的电子式:
形成过程的电子式:______ 。
④比较 分子中的键角大小并给出相应解释:
分子中的键角大小并给出相应解释:_______ 。
⑤相同条件下, 在水中的溶解度大于
在水中的溶解度大于 的,理由是
的,理由是_________ 。
 是9种中学化学中常见的元素。
是9种中学化学中常见的元素。(1)原子结构与元素性质
①基态氢原子中,核外电子的电子云轮廓图形状为
②3种元素
 中,离子半径最小的是
中,离子半径最小的是③基态
 的价层电子轨道表示式为
的价层电子轨道表示式为(2)微粒间相互作用与物质性质
①胆矾(
 )的结构示意图如下所示。
)的结构示意图如下所示。
 与
与 与
与 的作用力分别为
的作用力分别为②
 的VSEPR模型为
的VSEPR模型为 的分子空间构型为
的分子空间构型为 是
是③写出
 电子式:
电子式: 形成过程的电子式:
形成过程的电子式:④比较
 分子中的键角大小并给出相应解释:
分子中的键角大小并给出相应解释:⑤相同条件下,
 在水中的溶解度大于
在水中的溶解度大于 的,理由是
的,理由是
您最近一年使用:0次
名校
解题方法
3 . 下列说法中,正确的是
| A.s区元素全部是金属元素 |
| B.共价化合物中电负性大的成键元素表现为负价 |
| C.含有非极性键的分子一定是非极性分子 |
| D.非极性分子中一定含有非极性键 |
您最近一年使用:0次
名校
解题方法
4 . 下列各种物质中,都是由极性键构成的非极性分子的是
| A.NH3和CH4 | B.CO2和CCl4 | C.CH3Cl和BF3 | D.SO3和PCl3 |
您最近一年使用:0次
名校
解题方法
5 . 物质性质与其结构密切相关,下列比较中不正确 的是
A.在 中的溶解性: 中的溶解性: |
B.熔点: |
| C.硬度:晶体硅>碳化硅 |
D.物质的酸性: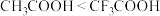 |
您最近一年使用:0次
名校
解题方法
6 . 工业合成 :
: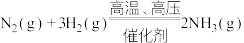
 。下列分析正确的是
。下列分析正确的是
 :
: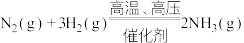
 。下列分析正确的是
。下列分析正确的是| A.虽然反应为放热反应,但在工业中仍然使用高温,是因为催化剂活性在高温下较好,且生产速率较快 |
B.若在容器中投入1mol 和3mol 和3mol ,最终反应放出热量akJ ,最终反应放出热量akJ |
C. 、 、 、 、 都为非极性分子 都为非极性分子 |
| D.在恒容恒温的容器中,若体系的密度不在变化,说明反应已经达到平衡状态 |
您最近一年使用:0次
2023-11-25更新
|
101次组卷
|
2卷引用:北京市第六十五中学2023-2024学年高三上学期期中达标测试化学试题
名校
解题方法
7 . 关于 、
、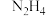 和
和 的结构与性质,下列说法
的结构与性质,下列说法不正确 的是
 、
、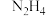 和
和 的结构与性质,下列说法
的结构与性质,下列说法A. 为极性分子 为极性分子 |
B. 空间结构为平面形 空间结构为平面形 |
C. 的沸点高于 的沸点高于 的原因是 的原因是 分子间氢键数目更多 分子间氢键数目更多 |
D. 和 和 中C、O、N杂化方式均相同 中C、O、N杂化方式均相同 |
您最近一年使用:0次
2023-11-23更新
|
187次组卷
|
2卷引用:北京市首都师范大学附属中学2022-2023学年高三上学期开学测试化学试题
名校
解题方法
8 . BeCl2可以以单体、二聚体和多聚体的形式存在。下列关于BeCl2的说法不正确 的是
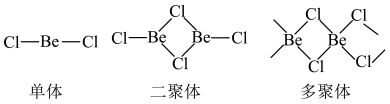

| A.单体是非极性分子 | B.二聚体的沸点比单体更高 |
| C.多聚体是平面结构 | D.二聚体和多聚体中均存在配位键 |
您最近一年使用:0次
2023-11-02更新
|
396次组卷
|
5卷引用:北京市海淀区2023-2024学年高三上学期期中测试化学试题
北京市海淀区2023-2024学年高三上学期期中测试化学试题 北京市第十四中学2023-2024学年高三上学期12月月考化学试题(已下线)北京市第四中学2023-2024学年高二上学期期末考试化学试题河南省漯河市2023-2024学年高三上学期期末质量监测化学试题(已下线)热点09 配合物和超分子
9 . 下列实验方案、现象、结论的对应关系正确的是
| 选项 | 操作 | 现象 | 解释 |
| A | 用毛皮摩擦过的带电橡胶棒靠近 液流 液流 |  液流方向不改变 液流方向不改变 |  中不含非极性键 中不含非极性键 |
| B | 将含有稀硫酸的蔗糖溶液水浴加热后,加入新制氢氧化铜悬浊液并加热 | 没有产生砖红色沉淀 | 蔗糖未水解 |
| C | 向酸性 溶液中加入甲苯 溶液中加入甲苯 | 溶液褪色 | 苯环对甲基有影响 |
| D | 向 溶液里逐滴加入 溶液里逐滴加入 氨水至过量 氨水至过量 | 先形成蓝色沉淀,后溶解得到深蓝色溶液 | 沉淀溶解时主要反应: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 由氧元素形成的常见物质有 、
、 、
、 和
和 等。
等。
(1)基态氧原子的电子排布式是___________ 。
(2)水分子的VSEPR模型是___________ 形。
(3)对 分子结构的研究,曾有以下甲、乙两种推测:
分子结构的研究,曾有以下甲、乙两种推测:

①根据测定 分子中
分子中___________ (填字母序号),确定其结构一定不是甲。
a.H-O键长 b.O-O键能 c.H-O-O键角
② 的结构如图丙。
的结构如图丙。 中的O-O比
中的O-O比 中的更
中的更___________ (填“难”或“易”)断裂。

③由于 不稳定,很难得到晶体。20世纪40年代初,卢嘉锡等化学家用尿素(
不稳定,很难得到晶体。20世纪40年代初,卢嘉锡等化学家用尿素( )与
)与 形成较稳定的尿素过氧化氢复合物晶体,进而测得
形成较稳定的尿素过氧化氢复合物晶体,进而测得 结构为乙。上述晶体中尿素与
结构为乙。上述晶体中尿素与 分子交替排列且二者中的O均与另外分子的H之间形成氢键。
分子交替排列且二者中的O均与另外分子的H之间形成氢键。
a. 为
为___________ (填“极性”或“非极性”)分子
b.用“X-H∙∙∙Y”表示出上述晶体中形成的氢键:___________ 。
(4) 的晶胞为立方体(边长为
的晶胞为立方体(边长为 ),结构如下。根据图中信息,可计算
),结构如下。根据图中信息,可计算 晶体密度是
晶体密度是___________  (
( 表示阿伏伽德罗常数的值。)
表示阿伏伽德罗常数的值。)

(5)已知 分子的空间结构为V形,中心O为
分子的空间结构为V形,中心O为 杂化。除σ键外,
杂化。除σ键外, 分子中还形成了含4个电子的大π键。每个
分子中还形成了含4个电子的大π键。每个 分子中用于成键的电子总数是
分子中用于成键的电子总数是___________ 个,中心O提供参与成键的电子数是___________ 个。
 、
、 、
、 和
和 等。
等。(1)基态氧原子的电子排布式是
(2)水分子的VSEPR模型是
(3)对
 分子结构的研究,曾有以下甲、乙两种推测:
分子结构的研究,曾有以下甲、乙两种推测:
①根据测定
 分子中
分子中a.H-O键长 b.O-O键能 c.H-O-O键角
②
 的结构如图丙。
的结构如图丙。 中的O-O比
中的O-O比 中的更
中的更
③由于
 不稳定,很难得到晶体。20世纪40年代初,卢嘉锡等化学家用尿素(
不稳定,很难得到晶体。20世纪40年代初,卢嘉锡等化学家用尿素( )与
)与 形成较稳定的尿素过氧化氢复合物晶体,进而测得
形成较稳定的尿素过氧化氢复合物晶体,进而测得 结构为乙。上述晶体中尿素与
结构为乙。上述晶体中尿素与 分子交替排列且二者中的O均与另外分子的H之间形成氢键。
分子交替排列且二者中的O均与另外分子的H之间形成氢键。a.
 为
为b.用“X-H∙∙∙Y”表示出上述晶体中形成的氢键:
(4)
 的晶胞为立方体(边长为
的晶胞为立方体(边长为 ),结构如下。根据图中信息,可计算
),结构如下。根据图中信息,可计算 晶体密度是
晶体密度是 (
( 表示阿伏伽德罗常数的值。)
表示阿伏伽德罗常数的值。)
(5)已知
 分子的空间结构为V形,中心O为
分子的空间结构为V形,中心O为 杂化。除σ键外,
杂化。除σ键外, 分子中还形成了含4个电子的大π键。每个
分子中还形成了含4个电子的大π键。每个 分子中用于成键的电子总数是
分子中用于成键的电子总数是
您最近一年使用:0次



