解题方法
1 . 硼是一种用途广泛的工业原料,除了用于生产硼砂、硼酸和硼的各种化合物外,在制备储氢材料方面也有重要的用途,试回答下列问题:
(1)Ti(BH4)3是一种储氢材料,由TiCl4和LiBH4反应制得。基态Ti原子的核外电子排布式为___________ , 的价层电子对数是
的价层电子对数是___________ 。
(2)过渡金属Q与镧形成的合金是一种储氢材料,其中基态Q原子的价电子排布式为nd2n+2(n+1)sn-1,则Q元素的名称为___________ ;基态Q原子核外成对电子数和未成对电子数之比为___________ 。
(3)氨硼烷(NH3BH3)含氢量高,热稳定性好,是一种具有潜力的固体储氢材料,在四氢呋喃(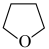 )作溶剂的条件下可合成氨硼烷:
)作溶剂的条件下可合成氨硼烷: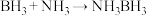 。
。
①测定晶体结构最常用的方法为___________ 。
②常温下,四氢呋喃在水中的溶解度大于环戊烷,其原因可能是___________ 。_
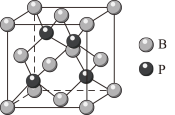
③硼与磷形成的一种晶体结构如图,晶体中离B原子最近的P原子有___________ 个;每个晶胞中的原子总数为___________ 。
(1)Ti(BH4)3是一种储氢材料,由TiCl4和LiBH4反应制得。基态Ti原子的核外电子排布式为
 的价层电子对数是
的价层电子对数是(2)过渡金属Q与镧形成的合金是一种储氢材料,其中基态Q原子的价电子排布式为nd2n+2(n+1)sn-1,则Q元素的名称为
(3)氨硼烷(NH3BH3)含氢量高,热稳定性好,是一种具有潜力的固体储氢材料,在四氢呋喃(
 )作溶剂的条件下可合成氨硼烷:
)作溶剂的条件下可合成氨硼烷: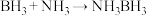 。
。①测定晶体结构最常用的方法为
②常温下,四氢呋喃在水中的溶解度大于环戊烷,其原因可能是
③硼与磷形成的一种晶体结构如图,晶体中离B原子最近的P原子有

您最近一年使用:0次
2 . 下列有关元素及其化合物性质的说法中正确的是
A. 与 与 发生水解反应,水解产物中都有HI 发生水解反应,水解产物中都有HI |
| B.ⅣA族元素单质的晶体类型相同 |
C.N的电负性比P大,可推断 分子的极性比 分子的极性比 分子的极性大 分子的极性大 |
D. 的熔沸点高于HF,可推断 的熔沸点高于HF,可推断 分子间氢键比HF分子间氢键多 分子间氢键比HF分子间氢键多 |
您最近一年使用:0次
解题方法
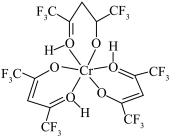
3 . 铬元素是哺乳类代谢过程中必需的微量元素,目前六氟代乙酰丙酮铬(Ⅲ)螯合物(其结构如图)的检出极限已达到 。下列有关说法错误的是
。下列有关说法错误的是
 。下列有关说法错误的是
。下列有关说法错误的是
A.简单氢化物的稳定性: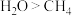 |
B.与基态 具有相同未成对电子数的同周期基态原子的元素有3种 具有相同未成对电子数的同周期基态原子的元素有3种 |
| C.Cr的配位数为6 |
D. 是含有极性键的极性分子 是含有极性键的极性分子 |
您最近一年使用:0次
名校
解题方法
4 . 氮化硼(BN)是一种重要的功能陶瓷材料,以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如图所示,下列叙述正确的是


| A.NH3与BF3都是由极性键构成的极性分子 |
| B.六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,立方氮化硼晶胞中含有8个氮原子、8个硼原子 |
| C.NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一,1molNH4BF4含有配位键的数目为2NA |
| D.立方氮化硼和半导体材料氮化铝的结构均类似于金刚石,立方氮化硼的熔点小于氮化铝 |
您最近一年使用:0次
2024-03-21更新
|
242次组卷
|
2卷引用:河北省石家庄市第二十四中学2023-2024高二上学期期末考试化学试题
5 . 设NA为阿伏伽德罗常数的值,下列说法正确的是
| A.25℃时,100mLpH=13的NaOH溶液中滴加醋酸溶液至中性,溶液中醋酸根离子和钠离子的总数为0.02NA |
| B.电解精炼铜,当精炼初始的10分钟内阳极共减重16g,则该10分钟内电路中通过的电子数为0.5NA |
| C.标准状况下,22.4LO3中含有的非极性共价键的数量为2NA |
| D.0.1mol·L-1的Na2SO3溶液中,含S微粒的总数为0.1NA |
您最近一年使用:0次
名校
解题方法
6 . “肼合成酶”以其中的Fe2+配合物为催化中心,可将NH2OH与NH3转化为肼(NH2NH2),其反应历程如下所示。
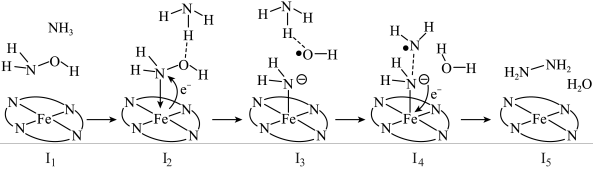
| A.I1中H-N-O的键角小于I2中H-N-O的键角 | B.NH2OH、NH3和H2O均为极性分子 |
| C.反应涉及非极性键的断裂和生成 | D.I3中催化中心离子为Fe3+ |
您最近一年使用:0次
2024-03-04更新
|
183次组卷
|
4卷引用:河北省石家庄市第二中学2023-2024学年高二下学期3月月考化学试题
7 . 下列说法正确的是
| A.基态氮原子有7种空间运动状态3种能量不同的电子 |
| B.B元素和Cl元素的电负性差值大于N元素和Cl元素的电负性差值,故:BCl3分子的极性大于NCl3 |
| C.某元素的M能层有2个未成对电子且无空轨道,其最高价氧化物对应水化物为强酸 |
| D.已知冰的熔化热为6.0kJ/mol,冰中氢键键能为20kJ/mol。假如每摩尔冰的熔化热完全用于打破冰的氢键,则最多只能破坏冰中15%的氢键 |
您最近一年使用:0次
名校
解题方法
8 . 臭氧通常存在于距离地面25km左右的高层大气中,它能有效阻挡紫外线,保护人类健康。但是在近地面,臭氧却是一种污染物。下列说法错误的是
| A.O3分子的空间构型为V形 |
| B.O3是由非极性键构成的极性分子 |
| C.O3在四氯化碳中的溶解度高于在水中的溶解度 |
| D.同周期主族元素中第一电离能比O大的有2种元素 |
您最近一年使用:0次
名校
解题方法
9 . NCl3和SiCl4均可发生水解反应,其中NCl3的水解机理示意图如下:
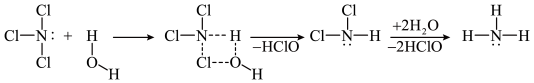
下列说法正确的是

下列说法正确的是
| A.NCl3和SiCl4均为极性分子 | B.NCl3和NH3中的N均为sp2杂化 |
| C.SiCl4中原子均满足8电子稳定结构 | D.NH4Cl和NH3均能与H2O形成氢键 |
您最近一年使用:0次
解题方法
10 . BF3与一定量的水形成(H2O)2•BF3,一定条件下(H2O)2•BF3可发生如图转化,下列说法正确的是
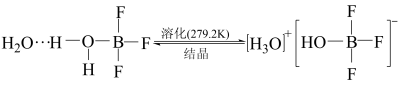
A.BF3和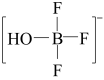 中B原子均采用sp2杂化轨道成键 中B原子均采用sp2杂化轨道成键 |
| B.(H2O)2•BF3分子中存在氢键和配位键 |
| C.(H2O)2•BF3中的所有元素都位于元素周期表中的p区 |
| D.BF3、NF3分子中的原子个数比相同,两者都是极性分子 |
您最近一年使用:0次
2024-02-26更新
|
350次组卷
|
4卷引用:河北省石家庄市辛集中学、衡水中学2023-2024高三上学期期末联考化学试题



