1 . 观察下列模型并结合有关信息,判断有关说法不正确的是
| B12结构单元 | SF6分子 | S8分子 | HCN | |
| 结构示意图 |  |  |  | 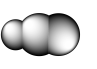 |
| 备注 | 熔点1873K | / | 易溶于CS2 | / |
| A.单质B结构单元中含有30个B﹣B键,含20个正三角形 |
| B.HCN为直线形 |
| C.SF6是由极性键构成的非极性分子 |
| D.固态硫S8中S原子为sp2杂化 |
您最近一年使用:0次
2021-03-18更新
|
354次组卷
|
5卷引用:青海省湟川中学2019-2020学年高二下学期期中考试化学试题
解题方法
2 . 请填写下表:
 | 空间构型 | 杂化方式 | 分子类型(极性或非极性) |
| 二氧化硫 | |||
| 氨气 | |||
| 三氧化硫 |
您最近一年使用:0次
名校
3 . 膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,电石气的杂质中常含有磷化氢。以下关于PH3的叙述正确的是
| A.PH3分子中有未成键的孤对电子 |
| B.PH3是非极性分子 |
| C.PH3分子的VSEPR模型是三角锥形 |
| D.PH3分子的P-H键是非极性键 |
您最近一年使用:0次
2020-11-01更新
|
269次组卷
|
3卷引用:内蒙古自治区呼伦贝尔市阿荣旗第一中学2019-2020学年高二下学期3月月考化学试题
内蒙古自治区呼伦贝尔市阿荣旗第一中学2019-2020学年高二下学期3月月考化学试题(已下线)专题11 物质结构与性质——备战2021年高考化学纠错笔记河北省沧州市吴桥县吴桥中学2023-2024学年高二下学期3月月考化学试题
4 . 有关乙烯分子的描述不正确的是
| A.两个碳原子采用sp杂化方式 |
| B.分子中既有极性键又有非极性键 |
| C.分子中既有σ键又有π键 |
| D.乙烯分子为非极性分子 |
您最近一年使用:0次
解题方法
5 . 在极性分子中,正电荷重心同负电荷重心间的距离称偶极长,通常用d表示。极性分子的极性强弱同偶极长和正(或负)电荷重心的电量(q)有关,一般用偶极矩(μ)来衡量。分子的偶极矩定义为偶极长和偶极上一端电荷电量的乘积,即μ=d·q。试回答以下问题:
(1)HCl、CS2、H2S、SO2四种分子中μ=0的是__________________ ;
(2)实验测得:μ(PF3)=1.03、μ(BF3)=0。由此可知,PF3分子构型是___________________ ,BF3分子构型是 __________________ 。
(3)治癌药Pt(NH3)2Cl2具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个角上。已知该化合物有两种异构体,A:棕黄色者μ>0,B:淡黄色者μ=0。在水中溶解度较大的是______________________ (填序号)。
(1)HCl、CS2、H2S、SO2四种分子中μ=0的是
(2)实验测得:μ(PF3)=1.03、μ(BF3)=0。由此可知,PF3分子构型是
(3)治癌药Pt(NH3)2Cl2具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个角上。已知该化合物有两种异构体,A:棕黄色者μ>0,B:淡黄色者μ=0。在水中溶解度较大的是
您最近一年使用:0次
名校
解题方法
6 . 现代无机化学对硫—氮化合物的研究是最为活跃的领域之一。其中如图是已经合成的最著名的硫—氮化合物的分子结构。下列说法正确的是
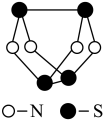

| A.该物质的分子式为SN |
| B.该物质的分子中既有极性键又有非极性键 |
| C.该物质的分子是非极性分子 |
| D.该物质与化合物S2N2互为同素异形体 |
您最近一年使用:0次
2020-07-29更新
|
142次组卷
|
3卷引用:内蒙古自治区包头市北方重工业集团有限公司第三中学2019-2020学年高二下学期期中考试化学试题
内蒙古自治区包头市北方重工业集团有限公司第三中学2019-2020学年高二下学期期中考试化学试题(已下线)第35讲 分子结构与性质-2021年高考化学一轮复习名师精讲练新疆哈密市第八中学2019-2020学年高二下学期期末考试化学试题
名校
7 . 已知H2O2分子的空间结构可在二面角中如图所示,下列有关H2O2结构的说法正确的是( )
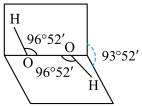
| A.H2O2中有3个σ键、1个π键 |
| B.H2O2为非极性分子 |
| C.H2O2中氧原子为sp杂化 |
| D.H2O2沸点高达158 ℃,可推测H2O2分子间可形成氢键 |
您最近一年使用:0次
2019-04-21更新
|
647次组卷
|
12卷引用:【全国百强校】内蒙古自治区赤峰市第二中学2018-2019学年高二下学期4月月考化学试题
【全国百强校】内蒙古自治区赤峰市第二中学2018-2019学年高二下学期4月月考化学试题天津市静海区第一中学2019-2020学年高二下学期3月学生学业能力调研考试化学试题河南省林州市第一中学2019-2020学年高二4月月考(实验班)化学试题福建省莆田第一中学2019-2020学年高二下学期期中考试化学试题江苏省常熟市2019-2020学年高二下学期期中考试化学试题四川省遂宁市安居区2020-2021学年高二上学期期中考试化学试题四川省遂宁市第二中学2020-2021学年高二上学期期中考试化学试题湖北省沙市第五中学2020-2021学年高二下学期3月月考化学试题福建省福清西山学校高中部2020-2021学年高二下学期期中考试化学试题第三节 分子结构与物质的性质 第2课时 分子间作用力 分子的手性云南省昆明市官渡区尚品书院学校2022-2023学年高二下学期3月月考化学试题四川省成都高新实验中学2023-2024学年高二下学期3月月考化学试卷
名校
8 . 化合物NH3与BF3可以通过配位键形成NH3·BF3,下列说法正确的是( )
| A.NH3与BF3都是三角锥形 | B.NH3与BF3都是极性分子 |
| C.NH3·BF3中各原子都达到8电子稳定结构 | D.NH3·BF3中,NH3提供孤电子对,BF3提供空轨道 |
您最近一年使用:0次
2019-04-21更新
|
756次组卷
|
14卷引用:【全国百强校】内蒙古自治区赤峰市第二中学2018-2019学年高二下学期4月月考化学试题
【全国百强校】内蒙古自治区赤峰市第二中学2018-2019学年高二下学期4月月考化学试题福建省永春县第一中学2018-2019学年高二下学期期中考试化学试题沪科版高中化学拓展课程第2章《化学键与晶体结构》检测题四川省蓬溪县蓬南中学2019-2020学年高二上学期第四次月考化学试题山东省枣庄市第三中学2019-2020学年高二下学期3月网上测试化学试题江苏省苏州市相城区陆慕高级中学2019-2020高二下学期4月质量检测化学试题安徽省安庆市太湖县2019-2020学年高二下学期期中质量调研考试化学试题福建省福州第一中学2019-2020学年高二下学期期末考试化学试题福建省漳州市正兴学校2020-2021学年高二下学期期末考试化学试题2021年山东高考化学试题变式题1-10山西省太原市英才学校2022-2023学年高二下学期3月阶段测试化学试题四川省广元市苍溪中学校2022-2023学年高二下学期5月期中考试化学试题2.3离子键、配位键与金属键(课前)-鲁科版选择性必修2湖北省武汉西藏中学2023-2024学年高二下学期4月月考化学试题
名校
9 . 下列模型分别表示C2H2、S8、SF6的结构,下列说法错误的是( )


| A.32 g S8分子中含有0.125 mol σ键 |
| B.SF6是由极性键构成的分子 |
| C.1 mol C2H2分子中有3 mol σ键和2 mol π键 |
| D.S8中S的杂化方式为sp3杂化 |
您最近一年使用:0次
2019-04-08更新
|
218次组卷
|
3卷引用:内蒙古自治区第一机械制造(集团)有限公司第一中学2018-2019学年高二下学期期中考试化学试题
名校
10 . 下列说法中,不正确的是( )
| A.光谱分析可用于元素检测,稀有气体He就是在分析太阳光谱时发现的 |
| B.X射线衍射实验是区别晶体与非晶体的最科学的方法 |
| C.等电子体具有相同的价电子总数,导致它们具有相同的化学性质 |
| D.分子中只含极性键的分子不一定是极性分子。 |
您最近一年使用:0次
2019-03-16更新
|
377次组卷
|
7卷引用:内蒙古包头市第四中学2018-2019学年高二下学期第一次月考(3月)化学试题



