名校
解题方法
1 . 下列叙述正确的是
| A.NH3是极性分子,分子中N原子处在3个H原子所组成的三角形的中心 |
| B.CC14是非极性分子,分子中C原子处在4个C1原子所组成的正方形的中心 |
| C.H2O是极性分子,分子中O原子处在2个H原子所连成的直线的中央 |
| D.CO2是非极性分子,分子中C原子处在2个O原子所连成的直线的中央 |
您最近一年使用:0次
2021-03-25更新
|
392次组卷
|
8卷引用:江苏省南京市2019-2020学年高二下学期期末考试化学试卷A卷
名校
2 . 按要求填空:
地球上的物质不断变化,数10亿年来大气的成分也发生了很大的变化。下表是原始大气和目前空气的主要成分:
分析上表所涉及的分子,填写下列空白。
(1)VSEPR模型为正四面体的分子有(填化学式,下同)__ ;
(2)由极性键构成的非极性分子有__ ;
(3)沸点最高的物质是H2O,1mol水最多可形成__ mol氢键;
(4)CO的结构可表示为O C,与CO结构最相似的分子是
C,与CO结构最相似的分子是__ ;
(5)以上分子有多种含有氧原子,请写出基态氧原子的价层电子轨道表达式__ 。
地球上的物质不断变化,数10亿年来大气的成分也发生了很大的变化。下表是原始大气和目前空气的主要成分:
| 目前空气的成分 | N2、O2、CO2、水蒸气及稀有气体(如He、Ne等) |
| 原始大气的主要成分 | CH4、NH3、CO、CO2等 |
(1)VSEPR模型为正四面体的分子有(填化学式,下同)
(2)由极性键构成的非极性分子有
(3)沸点最高的物质是H2O,1mol水最多可形成
(4)CO的结构可表示为O
 C,与CO结构最相似的分子是
C,与CO结构最相似的分子是(5)以上分子有多种含有氧原子,请写出基态氧原子的价层电子轨道表达式
您最近一年使用:0次
3 . 已知A、B、C、D、E、F为前4周期的6种元素,原子序数依次增大,其中A位于周期表中s区,其原子中电子层数和未成对电子数相同;B原子价电子排布式为nsnnpn,B和E同主族,D原子的最外层电子数是其内层电子数的3倍;F元素位于元素周期表的第4行、第11列。试回答下列问题:
(1)基态F原子的核外电子排布式为___ 。
(2)下列关于B2A2的说法中正确的是___ (填选项序号)
①B2A2中的所有原子都满足8电子稳定结构
②每个B2A2分子中σ键和π键数目比为1:1
③B2A2是含极性键和非极性键的非极性分子
④B2A2中心原子的杂化类型为sp杂化
(3)B、C、D三种元素第一电离能由大到小的顺序为___ (用元素符号表示)。
(4)C的简单气态氢化物与C的最高价氧化物对应的水化物反应生成一种盐H,H晶体中存在的化学键类型有___ (填选项符号)
①离子键 ②共价键 ③氢键 ④配位键 ⑤金属键
(5)基态E原子的最高能层具有的原子轨道数为___ ;B和E的最高价氧化物中,熔沸点较高的是___ (写化学式)。
(6)F单质的晶体堆积方式为面心立方最密堆积,其配位数为___ ;若F的相对原子质量为M,它的晶胞棱长为acm,则F晶体的密度为___ g·cm-3。(阿伏加 德罗常数为NA)
(1)基态F原子的核外电子排布式为
(2)下列关于B2A2的说法中正确的是
①B2A2中的所有原子都满足8电子稳定结构
②每个B2A2分子中σ键和π键数目比为1:1
③B2A2是含极性键和非极性键的非极性分子
④B2A2中心原子的杂化类型为sp杂化
(3)B、C、D三种元素第一电离能由大到小的顺序为
(4)C的简单气态氢化物与C的最高价氧化物对应的水化物反应生成一种盐H,H晶体中存在的化学键类型有
①离子键 ②共价键 ③氢键 ④配位键 ⑤金属键
(5)基态E原子的最高能层具有的原子轨道数为
(6)F单质的晶体堆积方式为面心立方最密堆积,其配位数为
您最近一年使用:0次
2020-09-05更新
|
63次组卷
|
2卷引用:陕西省洛南中学2021届高三上学期第一次模拟化学试题
解题方法
4 . 下列各分子中,属于含极性键的非极性分子的是
| A.P4 | B.CO2 | C.H2S | D.NH3 |
您最近一年使用:0次
名校
解题方法
5 . 下列说法错误的是
| A.原子间通过共用电子对所形成的化学键叫共价键 |
| B.两个成键原子间的核间距离叫键长,键长越短,化学键越牢固 |
| C.极性分子中一定含有极性键 |
| D.离子化合物中不可能含有非极性键 |
您最近一年使用:0次
2020-06-21更新
|
387次组卷
|
2卷引用:陕西省榆林市绥德县绥德中学2019-2020学年高二上学期第二次阶段检测化学试题
名校
解题方法
6 . 下列关于粒子结构的描述正确的是
| A.NF3和BF3是中心原子杂化类型相同的极性分子 |
| B.CH2Cl2和C2H4是空间构型不同的非极性分子 |
| C.在SiO2晶体中,Si原子与Si—O键数目比为1︰2 |
| D.CF4和CO2是含极性键的非极性分子 |
您最近一年使用:0次
2020-06-11更新
|
643次组卷
|
3卷引用:陕西省咸阳市实验中学2019-2020学年高二上学期第一次月考化学试题
陕西省咸阳市实验中学2019-2020学年高二上学期第一次月考化学试题(已下线)第二单元 化学键与分子间作用力(能力提升卷)-2020-2021学年高二化学单元测试定心卷(鲁科版选修3)河南省辉县市一中2020-2021学年高二下学期第二次阶段性考试化学试题
7 . 碳、氮元素及其化合物与生产、生活密切相关,回答下列问题。
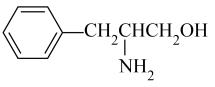
(1)某有机物的结构简式如图。该有机物分子是___ (填“极性”或“非极性”)分子,该有机物分子中电负性最大的原子为___ 。
(2)乙二胺(H2NCH2CH2NH2)分子中氮原子杂化类型为___ ,乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高很多,原因是__ 。
(1)某有机物的结构简式如图。该有机物分子是

(2)乙二胺(H2NCH2CH2NH2)分子中氮原子杂化类型为
您最近一年使用:0次
2019高三·全国·专题练习
解题方法
8 . 已知H和O可以形成H2O和H2O2两种化合物,试根据有关信息完成下列问题:
(1)水是维持生命活动所必需的一种物质。
①1 mol冰中有________ mol氢键。
②用球棍模型表示的水分子结构是____________ 。

(2)已知H2O2分子的结构如图所示:H2O2分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角为93°52′,而两个O—H键与O—O键的夹角均为96°52′。

试回答:
①H2O2分子的电子式是_____________________________ ,结构式是______________ 。
②H2O2分子是含有________ 键和________ 键的______________ (填“极性”或“非极性”)分子。
③H2O2难溶于CS2,简要说明理由:_______________ 。
④H2O2中氧元素的化合价是__________ ,简要说明原因_________________ 。
(1)水是维持生命活动所必需的一种物质。
①1 mol冰中有
②用球棍模型表示的水分子结构是

(2)已知H2O2分子的结构如图所示:H2O2分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角为93°52′,而两个O—H键与O—O键的夹角均为96°52′。

试回答:
①H2O2分子的电子式是
②H2O2分子是含有
③H2O2难溶于CS2,简要说明理由:
④H2O2中氧元素的化合价是
您最近一年使用:0次
9 . 下列分子中,属于极性分子的是( )
| A.CO2 | B.BeCl2 | C.BBr3 | D.COCl2 |
您最近一年使用:0次
2019-07-02更新
|
153次组卷
|
5卷引用:陕西省黄陵中学高新部2018-2019学年高二下学期期末考试化学试题
12-13高三·甘肃天水·阶段练习
名校
10 . S2Cl2是橙黄色液体,少量泄漏会产生窒息性气体,喷水雾可减慢其挥发,并产生酸性悬浊液。其分子结构如图所示。下列关于S2Cl2的说法中错误的是
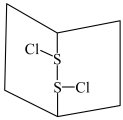

| A.S2Cl2为非极性分子 |
| B.分子中既含有极性键又含有非极性键 |
| C.与S2Br2结构相似,熔、沸点S2Br2>S2Cl2 |
| D.与水反应的化学方程式可能为2S2Cl2+2H2O===SO2↑+3S↓+4HCl |
您最近一年使用:0次
2019-03-29更新
|
1236次组卷
|
26卷引用:陕西省榆林市第十二中学2019-2020学年高二下学期期中考试化学试题
陕西省榆林市第十二中学2019-2020学年高二下学期期中考试化学试题(已下线)2013届甘肃省甘谷一中高三第五次检测化学试卷(已下线)同步君 选修3 第二章 第三节 键的极性和分子的极性高中化学人教版 选修三 第2章 分子结构与性质 键的极性和分子的极性【全国百强校】宁夏银川唐徕回民中学2017-2018学年高二下学期期中考试化学试题河南省开封市兰考县第一高级中学2018-2019学年高二下学期3月月考化学试题江苏省南京市南京师I范大学附属中学 2019-2020 学年高二下学期期中考试化学试题四川省邛崃市高埂中学2019-2020学年度高二下学期期中考试化学试题辽宁省开原市第二高级中学2021届高三第三次模拟考试化学试题陕西省宝鸡市长岭中学2021-2022学年高二下学期期中考试化学试题福建省建瓯市芝华中学2020-2021学年高二下学期第一阶段考试化学试题吉林省松原市乾安县第七中学2020-2021学年高二下学期第五次质量检测化学试题吉林省延边朝鲜族自治州延边二中北校区2020-2021学年高二下学期第一次月考化学试题福建省漳州市正兴学校2020-2021学年高二下学期期末考试化学试题广东省东莞市新世纪英才学校2021-2022学年高二上学期第一次教学质量检测化学试题四川省广安市第二中学2021-2022学年高二下学期第一次月考化学试题甘肃省兰州第一中学2021-2022学年高二下学期4月月考化学试题河南省驻马店市环际大联考2021-2022学年高二下学期期中考试化学试题新疆乌鲁木齐市第四中学2021-2022学年高二下学期期末考试化学试题福建省龙岩市长汀县第一中学2021-2022学年高二下学期第一次月考化学试题山东省青岛第二中学2020-2021学年高二上学期期末化学试题 四川省广安市第二中学校2022-2023学年高二下学期第一次月考化学试题河南省洛阳市2022-2023学年高二下学期期中考试化学试题黑龙江省牡丹江市第二高级中学2022-2023学年高二下学期7月期末化学试题湖北省武汉西藏中学2023-2024学年高二下学期4月月考化学试题江西省南昌市第十九中学2022-2023学年高二下学期3月第一次月考化学试卷



