名校
1 . 某有机物结构如下图,关于该有机分子,下列说法不正确的是
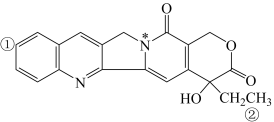
A. 键极性强于 键极性强于 键 键 |
| B.①号碳原子和②号碳原子杂化类型相同 |
| C.该分子中含有手性碳原子 |
D.带*的氮原子能与 以配位键结合 以配位键结合 |
您最近一年使用:0次
2023-05-15更新
|
116次组卷
|
2卷引用:黑龙江省哈尔滨市第九中学校2022-2023学年高二下学期期中考试化学试题
名校
解题方法
2 . 下列与分子性质有关的说法正确的是
A. 是非极性分子,Xe原子成键后不含孤电子对 是非极性分子,Xe原子成键后不含孤电子对 |
B. 的酸性强于 的酸性强于 是因为F的电负性大,使 是因为F的电负性大,使 中O-H极性强 中O-H极性强 |
C.C的电负性强于Si,所以 的熔沸点高于 的熔沸点高于 |
D.尿素 不溶于水,易溶于有机溶剂 不溶于水,易溶于有机溶剂 |
您最近一年使用:0次
名校
解题方法
3 . 解释下列现象的原因不正确的是
| 选项 | 现象 | 原因 |
| A |  中含有共价键 中含有共价键 | Al与Cl元素间的电负性差值小于1.7 |
| B | 碘在 中的溶解度比在水中大 中的溶解度比在水中大 | 碘和 均为非极性分子,水是极性分子 均为非极性分子,水是极性分子 |
| C | 对羟基苯甲醛的熔沸点比邻羟基苯甲醛的高 | 对羟基苯甲醛形成分子间氢键,而邻羟基苯甲醛形成分子内氢键 |
| D | HF的稳定性强于HCl | HF分子之间除了范德华力以外还存在氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 下列说法正确的是
A.由沸点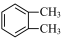 > >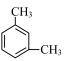 > >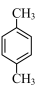 可知分子的极性: 可知分子的极性: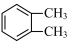 < <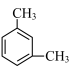 < <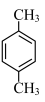 |
| B.NH3、AsH3的空间结构均呈三角锥形,由于电负性N>As可知键角:∠H-N-H∠H-As-H |
C.BF 的VSEPR模型为正四面体形,用“→”表示其结构中的配位键 的VSEPR模型为正四面体形,用“→”表示其结构中的配位键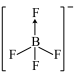 |
D.可用“相似相溶”规律解释硫单质( )易溶于CS2 )易溶于CS2 |
您最近一年使用:0次
名校
5 . 根据“相似相溶”规律,你认为下列物质在水中溶解度较大的是
| A.乙烯 | B.二氧化碳 | C.氨 | D.氢气 |
您最近一年使用:0次
名校
6 . 下列分子中,属于含有极性共价键的非极性分子的是
| A.H2O | B.Cl2 | C.NH3 | D.CCl4 |
您最近一年使用:0次
名校
解题方法
7 . 氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如图1所示。下列叙述正确的是
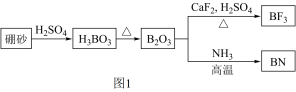



| A.NH3与BF3都是由极性键构成的极性分子 |
| B.立方氮化硼和半导体材料氮化铝的结构均类似于金刚石,立方氮化硼的熔点小于氮化铝 |
| C.NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一,lmolNH4BF4含有配位键的数目为NA |
D.立方BN晶体晶胞结构如图2所示,设晶胞中最近的B、N原子之间的距离为anm,阿佛加德罗常数的值为NA,则晶体的密度为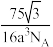 ×1021g•cm-3 ×1021g•cm-3 |
您最近一年使用:0次
名校
解题方法
8 . 化合物T是一种用于合成药物的重要试剂,其结构简式如图所示。已知X、Y、Z、M、N为原子序数依次增大的前四周期主族元素,Z、M位于同一主族,X、Y、N的最外层电子数之和等于Z的最外层电子数。下列有关叙述正确的是


| A.原子半径:M>N>Z |
| B.简单氢化物稳定性和沸点均为:Z>M |
| C.化合物YM2与YZM均为非极性分子 |
| D.化合物T中所有原子均满足8电子相对稳定结构 |
您最近一年使用:0次
名校
9 . 按要求填空:
(1)在①N2②CS2③H2Se④AsH3⑤(CN)2⑥HCHO⑦CH2Cl2⑧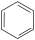 ⑨BF3⑩H2O2中,仅由
⑨BF3⑩H2O2中,仅由 极性键构成的极性分子有
极性键构成的极性分子有_____ ;含有π键,且属于非极性分子的是_____ ;既含有极性键又含有非极性键的分子为_____ ;⑩为_____ (填”极性”或“非极性”)分子。
(2)已知下列四种酸①CH3CBr2COOH②CH3CF2COOH③CH3CH2COOH④CH3COOH酸性由弱到强的顺序为_____ 。
(3)已知BF3和过量NaF作用可生成NaBF4,BF 的空间结构为
的空间结构为_____ ;NaBF4的电子式为_____ 。
(1)在①N2②CS2③H2Se④AsH3⑤(CN)2⑥HCHO⑦CH2Cl2⑧
 ⑨BF3⑩H2O2中,仅由
⑨BF3⑩H2O2中,仅由 极性键构成的极性分子有
极性键构成的极性分子有(2)已知下列四种酸①CH3CBr2COOH②CH3CF2COOH③CH3CH2COOH④CH3COOH酸性由弱到强的顺序为
(3)已知BF3和过量NaF作用可生成NaBF4,BF
 的空间结构为
的空间结构为
您最近一年使用:0次
名校
解题方法
10 . 按要求回答下列问题。
(1)H3O+中心原子采用______ 杂化,其键角比H2O中键角______ (填“大”或“小”)。
(2)有如下分子:①PCl5②PCl3③BF3④BeCl2⑤NF3⑥CO2⑦HCl⑧H2O2⑨CH4⑩C2H4
①上述分子中每个原子周围都满足8电子结构的是______ (填序号)。
②CO2分子中σ键和π键个数之比为______ 。
③含有极性键的极性分子有_____ (填序号)。
④空间结构为三角锥形的分子是______ (填序号)。
(1)H3O+中心原子采用
(2)有如下分子:①PCl5②PCl3③BF3④BeCl2⑤NF3⑥CO2⑦HCl⑧H2O2⑨CH4⑩C2H4
①上述分子中每个原子周围都满足8电子结构的是
②CO2分子中σ键和π键个数之比为
③含有极性键的极性分子有
④空间结构为三角锥形的分子是
您最近一年使用:0次
2023-05-07更新
|
198次组卷
|
3卷引用:黑龙江省牡丹江市第三高级中学2022-2023学年高二下学期期中考试化学试题



