名校
1 . 对尼古丁和苯并芘的性质推测可能错误的是
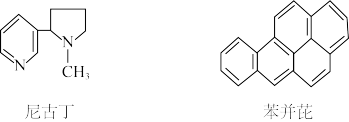

| A.尼古丁分子中的氮原子能与水中H+结合形成配位键,其水溶液可能呈碱性 |
| B.尼古丁可能既溶于水又溶于有机溶剂,苯并芘只溶于有机溶剂而不溶于水 |
| C.两者固态都属分子晶体,尼古丁分子间存在氢键,熔沸点较高 |
| D.尼古丁分子中的所有碳原子可能不在同一平面,苯并芘分子中的所有氢原子都在同一平面上 |
您最近一年使用:0次
名校
2 . 下列说法正确的是
A. 很稳定,与水分子间存在氢键有关 很稳定,与水分子间存在氢键有关 |
| B.HCl中,每个原子的最外层都具有8电子稳定结构 |
| C.熔融状态下能导电的物质一定是离子化合物 |
| D.NaOH溶于水的过程,破坏了离子键 |
您最近一年使用:0次
2021-12-28更新
|
119次组卷
|
3卷引用:浙江省精诚联盟2021-2022学年高一上学期12月普通高中学考适应性测试化学试题
名校
3 . 请回答以下问题:
(1)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),而与其原子总数相等的等电子体CH3CH3相比,NH3BH3熔点比CH3CH3高,其原因是__ 。
(2)已知高温下,冰晶石密度为2.1g/cm3,铝单质的密度为2.3g/cm3,工业上电解法制单质铝的过程中,冰晶石起到哪些作用__ 。
(1)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),而与其原子总数相等的等电子体CH3CH3相比,NH3BH3熔点比CH3CH3高,其原因是
(2)已知高温下,冰晶石密度为2.1g/cm3,铝单质的密度为2.3g/cm3,工业上电解法制单质铝的过程中,冰晶石起到哪些作用
您最近一年使用:0次
4 . 填空。
(1)H2O分子的空间构型是___________ ;H2O的沸点高于HF的可能原因___________ 。
(2)已知原子排列越规则原子层与层之间越容易滑动,金属铝和铝合金的原子结构排列图如下所示。请说明铝合金硬度大于金属铝的原因___________ 。

(1)H2O分子的空间构型是
(2)已知原子排列越规则原子层与层之间越容易滑动,金属铝和铝合金的原子结构排列图如下所示。请说明铝合金硬度大于金属铝的原因

您最近一年使用:0次
5 . 如图是石膏的部分层状结构,中间的虚线代表层与层的分界线。已知: 。下列说法不正确的是
。下列说法不正确的是

 。下列说法不正确的是
。下列说法不正确的是
| A.层与层之间通过氢键连在一起 |
B.每个H2O连接在Ca2+和相邻两层各1个 的O上 的O上 |
| C.无水CaSO4可用作吸水剂 |
| D.加热图示所示石膏,只破坏层与层之间的作用力 |
您最近一年使用:0次
6 . 完成下列填空
(1)沸点:
___________ 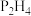 (填“>”或“<”),判断依据是
(填“>”或“<”),判断依据是___________ 。
(2)高铁酸盐是公认的绿色消毒净水剂,请简要解释其原理___________ 。
(1)沸点:

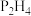 (填“>”或“<”),判断依据是
(填“>”或“<”),判断依据是(2)高铁酸盐是公认的绿色消毒净水剂,请简要解释其原理
您最近一年使用:0次
7 . 下列有关物理量大小比较正确的是
A.相同温度和压强下,熵值: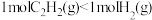 |
B.分子间氢键数量: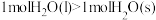 |
C.水溶性: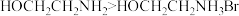 |
D.已知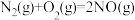  ; ;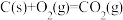  ,则 ,则 |
您最近一年使用:0次
2021-12-16更新
|
182次组卷
|
4卷引用: 浙江省金丽衢十二校2021-2022学年高三上学期第一次联考化学试题
浙江省金丽衢十二校2021-2022学年高三上学期第一次联考化学试题(已下线)解密09 化学反应速率与化学平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)三轮冲刺卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(浙江专用)江西省宁冈中学2022-2023学年高二下学期6月期末化学试题
解题方法
8 . 填空。
(1)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是___________ 。
(2)已知有关氨、磷的单键和三键的键能(kJ∙mol-1)如表:
从能量角度看,氮以N2、而白磷以P4(结构式可表示为 )形式存在的原因是
)形式存在的原因是___________ 。
(1)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是
(2)已知有关氨、磷的单键和三键的键能(kJ∙mol-1)如表:
| N-N | N≡N | P-P | P≡P |
| 193 | 946 | 197 | 489 |
从能量角度看,氮以N2、而白磷以P4(结构式可表示为
 )形式存在的原因是
)形式存在的原因是
您最近一年使用:0次
解题方法
9 . 回答下列问题:
(1)已知三种晶体的熔点数据如表:
氮化铝的熔点明显高于Mg3N2的原因是___ 。
(2)NaHS2是离子化合物,写出其电子式:___ 。
(3)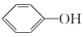 常温下微溶于水而CH3CH2OH常温下与水任意比互溶,试分析可能原因:
常温下微溶于水而CH3CH2OH常温下与水任意比互溶,试分析可能原因:___ 。
(1)已知三种晶体的熔点数据如表:
| 化合物 | Mg3N2 | AlN | Si3N4 |
| 熔点 | 800℃ | 2249℃ | 1800℃以上 |
氮化铝的熔点明显高于Mg3N2的原因是
(2)NaHS2是离子化合物,写出其电子式:
(3)
 常温下微溶于水而CH3CH2OH常温下与水任意比互溶,试分析可能原因:
常温下微溶于水而CH3CH2OH常温下与水任意比互溶,试分析可能原因:
您最近一年使用:0次
解题方法
10 . 下列“类比”合理的是
| A.Fe3O4中Fe元素显+2、+3价,则Pb3O4中Pb显+2、+3价 |
| B.SiH4的沸点比CH4高,则PH3的沸点比NH3高 |
| C.向Fe(OH)3中加入盐酸生成Fe3+,则向Fe(OH)3中加入氢溴酸也生成Fe3+ |
| D.Na2O2与CO2反应生成Na2CO3和O2,则Na2O2与SO2反应生成Na2SO3和O2 |
您最近一年使用:0次



