名校
解题方法
1 . 氟化镁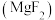 晶体广泛应用在光学、冶金、国防、医疗等领域。
晶体广泛应用在光学、冶金、国防、医疗等领域。
Ⅰ.氟化镁晶胞是长方体,其结构如下图所示:_______ 区。
(2) 晶胞示意图中:
晶胞示意图中:
a.○表示_______ (填离子符号)。
b.离子半径: ,结合离子结构示意图解释原因:
,结合离子结构示意图解释原因:_______ 。
(3)已知 晶胞体积为
晶胞体积为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则其晶体密度
,则其晶体密度
____  (用代数式表示)。
(用代数式表示)。
Ⅱ.一种由 制备
制备 的工艺流程如下:
的工艺流程如下:
已知:i. 易溶于甲醇。
易溶于甲醇。
ii. ,
,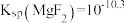 ,
, 。
。
(4)上述流程中,可循环利用的物质是_______ 。
(5)比较相同条件下化学反应速率的大小:① 与
与 ;②
;② 与
与 。
。
a.小组同学预测化学反应速率:①<②,理由是甲基为_____ 基团,导致 键极性:
键极性: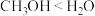 。
。
b.实验表明化学反应速率:①>②,分析其原因可能是_______ 。
(6)上述流程中 开始转化为
开始转化为 所需氟化物的浓度:
所需氟化物的浓度: 。结合沉淀溶解平衡分析原因:
。结合沉淀溶解平衡分析原因:_______ 。
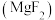 晶体广泛应用在光学、冶金、国防、医疗等领域。
晶体广泛应用在光学、冶金、国防、医疗等领域。Ⅰ.氟化镁晶胞是长方体,其结构如下图所示:

(2)
 晶胞示意图中:
晶胞示意图中:a.○表示
b.离子半径:
 ,结合离子结构示意图解释原因:
,结合离子结构示意图解释原因:(3)已知
 晶胞体积为
晶胞体积为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则其晶体密度
,则其晶体密度
 (用代数式表示)。
(用代数式表示)。Ⅱ.一种由
 制备
制备 的工艺流程如下:
的工艺流程如下:
已知:i.
 易溶于甲醇。
易溶于甲醇。ii.
 ,
,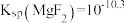 ,
, 。
。(4)上述流程中,可循环利用的物质是
(5)比较相同条件下化学反应速率的大小:①
 与
与 ;②
;② 与
与 。
。a.小组同学预测化学反应速率:①<②,理由是甲基为
 键极性:
键极性: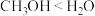 。
。b.实验表明化学反应速率:①>②,分析其原因可能是
(6)上述流程中
 开始转化为
开始转化为 所需氟化物的浓度:
所需氟化物的浓度: 。结合沉淀溶解平衡分析原因:
。结合沉淀溶解平衡分析原因:
您最近一年使用:0次
解题方法
2 . 青蒿素(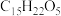 )是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
)是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
在浸取、蒸馏过程中,发现用沸点比乙醇低的乙醚( )提取,效果更好。
)提取,效果更好。
①乙醚沸点低于乙醇,原因是___________ 。
②用乙醚提取效果更好,原因是___________ 。
(2)确定结构
①测量晶胞中各处电子云密度大小,可确定原子的位置、种类。比较青蒿素分子中 、
、 、
、 的原子核附近电子云密度大小:
的原子核附近电子云密度大小:___________ 。
②图中晶胞的棱长分别为 、
、 、
、 ,晶体的密度为
,晶体的密度为___________  。(用
。(用 表示阿伏加德罗常数;
表示阿伏加德罗常数; ;青蒿素的相对分子质量为282)
;青蒿素的相对分子质量为282)
③能确定晶体中哪些原子间存在化学键、并能确定键长和键角,从而得出分子空间结构的一种方法是___________ 。
a.质谱法 b.X射线衍射 c.核磁共振氢谱 d.红外光谱
(3)修饰结构,提高疗效
一定条件下,用 将青蒿素选择性还原生成双氢青蒿素。
将青蒿素选择性还原生成双氢青蒿素。___________ 。
② 的空间结构为
的空间结构为___________ 。
③青蒿素与双氢青蒿素中相同的官能团是___________ 和___________ 。
双氢青蒿素比青蒿素水溶性更好,治疗疟疾的效果更好。
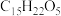 )是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
)是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
在浸取、蒸馏过程中,发现用沸点比乙醇低的乙醚(
 )提取,效果更好。
)提取,效果更好。①乙醚沸点低于乙醇,原因是
②用乙醚提取效果更好,原因是
(2)确定结构
①测量晶胞中各处电子云密度大小,可确定原子的位置、种类。比较青蒿素分子中
 、
、 、
、 的原子核附近电子云密度大小:
的原子核附近电子云密度大小:②图中晶胞的棱长分别为
 、
、 、
、 ,晶体的密度为
,晶体的密度为 。(用
。(用 表示阿伏加德罗常数;
表示阿伏加德罗常数; ;青蒿素的相对分子质量为282)
;青蒿素的相对分子质量为282)③能确定晶体中哪些原子间存在化学键、并能确定键长和键角,从而得出分子空间结构的一种方法是
a.质谱法 b.X射线衍射 c.核磁共振氢谱 d.红外光谱
(3)修饰结构,提高疗效
一定条件下,用
 将青蒿素选择性还原生成双氢青蒿素。
将青蒿素选择性还原生成双氢青蒿素。
②
 的空间结构为
的空间结构为③青蒿素与双氢青蒿素中相同的官能团是
双氢青蒿素比青蒿素水溶性更好,治疗疟疾的效果更好。
您最近一年使用:0次
3 . 氟化镁( )晶体广泛应用在光学、冶金、国防、医疗等领域。
)晶体广泛应用在光学、冶金、国防、医疗等领域。
(1)镁元素位于元素周期表_______ 区(填“s”“p”“d或“ds”)。
(2) 晶胞示意图中:a.○表示
晶胞示意图中:a.○表示_______ (填离子符号)。b.离子半径: 结合离子结构示意图解释原因:
结合离子结构示意图解释原因:______________ 。
(3)已知 晶胞体积为
晶胞体积为 啊伏伽德罗常数的值为
啊伏伽德罗常数的值为 ,则其晶体密度=
,则其晶体密度=_______  (用代数式表示)。
(用代数式表示)。
Ⅱ.一种由 制备
制备 的工艺流程如下
的工艺流程如下
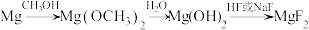
已知:i.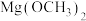 易溶于甲醇;
易溶于甲醇;
ii. ,
,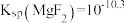 ,
,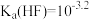
(4)上述流程中,可循环利用的物质是_______ 。
(5)比较相同条件下化学反应速率的大小:① 与
与 ;②
;② 与
与 。
。
a.小组同学预测化学反应速率:①<②,理由是甲基为_______ 基团,导致 键极性:
键极性: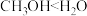 。
。
b.实验表明化学反应速率:①>②,分析其原因可能是:______________ 。
(6)上述流程中 开始转化为
开始转化为 所需氟化物的浓度:
所需氟化物的浓度: 。结合沉淀溶解平衡分析原因:
。结合沉淀溶解平衡分析原因:__________ 。
 )晶体广泛应用在光学、冶金、国防、医疗等领域。
)晶体广泛应用在光学、冶金、国防、医疗等领域。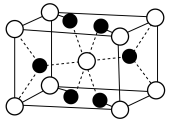
(1)镁元素位于元素周期表
(2)
 晶胞示意图中:a.○表示
晶胞示意图中:a.○表示 结合离子结构示意图解释原因:
结合离子结构示意图解释原因:(3)已知
 晶胞体积为
晶胞体积为 啊伏伽德罗常数的值为
啊伏伽德罗常数的值为 ,则其晶体密度=
,则其晶体密度= (用代数式表示)。
(用代数式表示)。Ⅱ.一种由
 制备
制备 的工艺流程如下
的工艺流程如下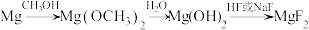
已知:i.
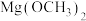 易溶于甲醇;
易溶于甲醇;ii.
 ,
,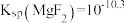 ,
,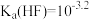
(4)上述流程中,可循环利用的物质是
(5)比较相同条件下化学反应速率的大小:①
 与
与 ;②
;② 与
与 。
。a.小组同学预测化学反应速率:①<②,理由是甲基为
 键极性:
键极性: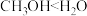 。
。b.实验表明化学反应速率:①>②,分析其原因可能是:
(6)上述流程中
 开始转化为
开始转化为 所需氟化物的浓度:
所需氟化物的浓度: 。结合沉淀溶解平衡分析原因:
。结合沉淀溶解平衡分析原因:
您最近一年使用:0次
名校
4 . 硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物。
(1)基态硒原子的价层电子排布式为___________ ;As的第一电离能比Se的第一电离能大的原因为___________ 。
(2) 中心原子的杂化类型是:
中心原子的杂化类型是:___________ , 的立体构型是
的立体构型是___________ 。
(3) 属于
属于___________ (填“极性”或“非极性”)分子;比较 与
与 沸点高低,并说明原因:
沸点高低,并说明原因:___________ 。
(4)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为___________ ;若该晶胞密度为ρg⋅cm ,硒化锌的摩尔质量为Mg⋅mol
,硒化锌的摩尔质量为Mg⋅mol ,
, 代表阿伏加德罗常数的值,则晶胞参数(边长)a为
代表阿伏加德罗常数的值,则晶胞参数(边长)a为___________ 。
(1)基态硒原子的价层电子排布式为
(2)
 中心原子的杂化类型是:
中心原子的杂化类型是: 的立体构型是
的立体构型是(3)
 属于
属于 与
与 沸点高低,并说明原因:
沸点高低,并说明原因:(4)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为
 ,硒化锌的摩尔质量为Mg⋅mol
,硒化锌的摩尔质量为Mg⋅mol ,
, 代表阿伏加德罗常数的值,则晶胞参数(边长)a为
代表阿伏加德罗常数的值,则晶胞参数(边长)a为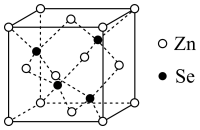
您最近一年使用:0次
2024-05-03更新
|
390次组卷
|
2卷引用:北京市大兴区第一中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
5 . 我国科学家合成了以 、
、 、
、 为核心元素的催化剂实现高效硝酸盐电还原为氨。催化剂晶体的典型晶胞结构如下图所示。下列说法正确的是
为核心元素的催化剂实现高效硝酸盐电还原为氨。催化剂晶体的典型晶胞结构如下图所示。下列说法正确的是
 、
、 、
、 为核心元素的催化剂实现高效硝酸盐电还原为氨。催化剂晶体的典型晶胞结构如下图所示。下列说法正确的是
为核心元素的催化剂实现高效硝酸盐电还原为氨。催化剂晶体的典型晶胞结构如下图所示。下列说法正确的是
A.基态 原子的价层电子排布式为 原子的价层电子排布式为 |
B.晶胞(a)中共有6个 原子 原子 |
C.晶体(b)的化学式为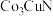 |
D.晶胞(a)中离 原子最近且等距的 原子最近且等距的 原子数目为8 原子数目为8 |
您最近一年使用:0次
2024-05-02更新
|
153次组卷
|
2卷引用:北京市顺义牛栏山第一中学2023-2024学年高二下学期4月月考化学试题
6 . 设 为阿伏加德罗常数的值,图1和图2分别为氧化镁和氯化铯的晶胞结构模型.下列有关说法中
为阿伏加德罗常数的值,图1和图2分别为氧化镁和氯化铯的晶胞结构模型.下列有关说法中不正确 的是
 为阿伏加德罗常数的值,图1和图2分别为氧化镁和氯化铯的晶胞结构模型.下列有关说法中
为阿伏加德罗常数的值,图1和图2分别为氧化镁和氯化铯的晶胞结构模型.下列有关说法中
| A.氯化铯熔点比氧化镁低 |
| B.利用X射线衍射可确定两种晶体的结构 |
C.每个氧化镁晶胞的质量为 g g |
| D.两种晶胞中每个阳离子周围与它最近且等距的阴离子数目相同 |
您最近一年使用:0次
2024-04-23更新
|
59次组卷
|
4卷引用:北京师范大学附属实验中学2023-2024学年高二下学期第一次测练化学试题
北京师范大学附属实验中学2023-2024学年高二下学期第一次测练化学试题北京市第一○一中学2022-2023学年高二下学期期末考试化学试题福建省厦门第六中学2023-2024学年高二下学期4月月考化学试卷(已下线)专题01 物质的结构与性质-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(人教版2019)
7 . 将钴酞菁和三氯化铝复合嵌接在碳纳米管上,制得一种高效催化还原二氧化碳的催化剂。回答下列问题:
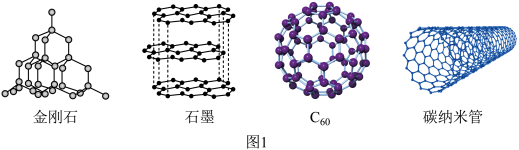
(1)碳的几种单质如图1所示。___________ 。
②金刚石晶体中C原子数与C-C键数的比为___________ 。
③石墨可以导电的原因是___________ 。
(2)C60的晶胞如图2所示。___________ 。
②1个C60晶胞中含有___________ 个原子。
③世界上第一辆单分子“纳米小车”的四个轮子是C60,小车运行情况如图所示,从a处化学键的特点说明其运动原因:___________ 。___________ 。
②钴酞菁分子中能形成配位键的原因是___________ 。
(4)气态AlCl3通常以二聚体Al2Cl6的形式存在,其空间结构如图4所示。AlF3结构属立方晶系,晶胞如图5所示。___________ 。
②AlF3的熔点为1090℃,远高于AlCl3的熔点192℃,原因是___________ 。
③AlF3晶体距离F-最近的阳离子有___________ 个。
④AlF3的晶胞形状为正方体,边长为anm,该晶体密度为___________ g·cm-3。(列出计算式,阿伏加德罗常数用NA表示,1nm=10-7cm)
(1)碳的几种单质如图1所示。
②金刚石晶体中C原子数与C-C键数的比为
③石墨可以导电的原因是
(2)C60的晶胞如图2所示。
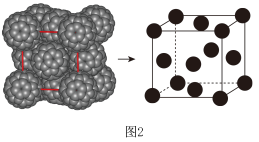
②1个C60晶胞中含有
③世界上第一辆单分子“纳米小车”的四个轮子是C60,小车运行情况如图所示,从a处化学键的特点说明其运动原因:
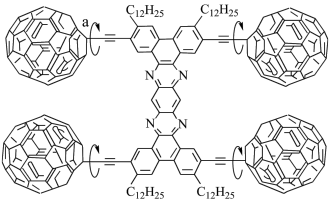

②钴酞菁分子中能形成配位键的原因是
(4)气态AlCl3通常以二聚体Al2Cl6的形式存在,其空间结构如图4所示。AlF3结构属立方晶系,晶胞如图5所示。
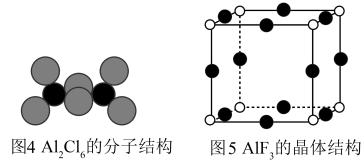
②AlF3的熔点为1090℃,远高于AlCl3的熔点192℃,原因是
③AlF3晶体距离F-最近的阳离子有
④AlF3的晶胞形状为正方体,边长为anm,该晶体密度为
您最近一年使用:0次
名校
解题方法
8 . 铜及其化合物具有广泛的用途。
(一) 广泛应用于太阳能电池领域。以
广泛应用于太阳能电池领域。以 、
、 和抗坏血酸为原料,可制备
和抗坏血酸为原料,可制备 。
。
(1) 基态核外电子排布式为
基态核外电子排布式为___________ 。
(2)抗坏血酸的分子结构如图1所示。推测抗坏血酸在水中的溶解性:___________ (填“难溶于水”或“易溶于水”),理由是:___________ 。 晶胞(见图2)中,晶胞中
晶胞(见图2)中,晶胞中 离子的数目为
离子的数目为___________ 。 和
和 的熔点比较,熔点较高的是
的熔点比较,熔点较高的是___________ ,解释原因___________ 。
(二) 是叶绿素的必要成分,叶绿素的结构如图3,请回答相关问题:
是叶绿素的必要成分,叶绿素的结构如图3,请回答相关问题: 与
与 原子之间形成的化学键称为
原子之间形成的化学键称为___________ 。
(6)构成叶绿素的非金属元素中, 和
和 第一电离能较大的为
第一电离能较大的为___________ ,请从原子结构角度解释原因___________ 。
(一)
 广泛应用于太阳能电池领域。以
广泛应用于太阳能电池领域。以 、
、 和抗坏血酸为原料,可制备
和抗坏血酸为原料,可制备 。
。(1)
 基态核外电子排布式为
基态核外电子排布式为(2)抗坏血酸的分子结构如图1所示。推测抗坏血酸在水中的溶解性:

 晶胞(见图2)中,晶胞中
晶胞(见图2)中,晶胞中 离子的数目为
离子的数目为
 和
和 的熔点比较,熔点较高的是
的熔点比较,熔点较高的是(二)
 是叶绿素的必要成分,叶绿素的结构如图3,请回答相关问题:
是叶绿素的必要成分,叶绿素的结构如图3,请回答相关问题:
 与
与 原子之间形成的化学键称为
原子之间形成的化学键称为(6)构成叶绿素的非金属元素中,
 和
和 第一电离能较大的为
第一电离能较大的为
您最近一年使用:0次
名校
解题方法
9 . 磷酸亚铁锂( )可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用
)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用 、
、 、
、 和苯胺等作为原料制备。回答下列问题:
和苯胺等作为原料制备。回答下列问题:
(1)在周期表中,与 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是___________ ,该元素基态原子核外M层电子的自旋状态___________ (填“相同”或“相反”)。
(2)苯胺( )含有的官能团的名称是
)含有的官能团的名称是___________ ,其晶体类型是___________ 。苯胺与甲苯( )的相对分子质量相近,但苯胺的熔点(
)的相对分子质量相近,但苯胺的熔点( )、沸点(
)、沸点( )分别高于甲苯的熔点(
)分别高于甲苯的熔点( )、沸点(
)、沸点( ),原因是
),原因是___________ 。
(3)基态 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为___________ 。
(4)在磷酸根离子(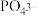 )中,中心原子的价层电子对数为
)中,中心原子的价层电子对数为___________ 。
(5)比较 与
与 的半径大小关系:
的半径大小关系:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(6) 的晶胞结构示意图如(a)所示。其中
的晶胞结构示意图如(a)所示。其中 围绕
围绕 和
和 分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有
分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有 的单元数有
的单元数有___________ 个。 脱出部分
脱出部分 ,形成
,形成 ,结构示意图如(b)所示,则
,结构示意图如(b)所示,则
___________ ,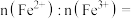
___________ 。
 )可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用
)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用 、
、 、
、 和苯胺等作为原料制备。回答下列问题:
和苯胺等作为原料制备。回答下列问题:(1)在周期表中,与
 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是(2)苯胺(
 )含有的官能团的名称是
)含有的官能团的名称是 )的相对分子质量相近,但苯胺的熔点(
)的相对分子质量相近,但苯胺的熔点( )、沸点(
)、沸点( )分别高于甲苯的熔点(
)分别高于甲苯的熔点( )、沸点(
)、沸点( ),原因是
),原因是(3)基态
 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为(4)在磷酸根离子(
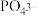 )中,中心原子的价层电子对数为
)中,中心原子的价层电子对数为(5)比较
 与
与 的半径大小关系:
的半径大小关系:
 (填“>”或“<”)。
(填“>”或“<”)。(6)
 的晶胞结构示意图如(a)所示。其中
的晶胞结构示意图如(a)所示。其中 围绕
围绕 和
和 分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有
分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有 的单元数有
的单元数有
 脱出部分
脱出部分 ,形成
,形成 ,结构示意图如(b)所示,则
,结构示意图如(b)所示,则
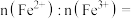
您最近一年使用:0次
名校
解题方法
10 . 高二化学组组织同学们制作晶体模型。8班张宇涵同学提交了金刚石的晶体结构模型,17班路雪同学提交了氯化钠的晶胞模型,如下图所示。下列说法不正确的是


A.金刚石晶体中,碳原子采取 杂化轨道成键,形成共价键三维骨架网络 杂化轨道成键,形成共价键三维骨架网络 |
B. 金刚石晶体中含 金刚石晶体中含 键 键 |
C.氯化钠晶体中,1个 周围有12个距离最近且相等的 周围有12个距离最近且相等的 |
D.氯化钠晶胞为立方体,若棱长为 ,则晶体密度为 ,则晶体密度为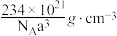 |
您最近一年使用:0次



