1 . 下列有关晶体的叙述中,错误的是
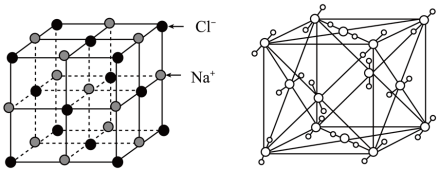

| A.氯化钠晶体中,每个Na+周围距离最近且相等的Na+共有6个 |
| B.金属晶体中,自由电子为所有金属离子所共有 |
| C.干冰晶体中,每个CO2分子周围距离最近且相等的CO2分子共有12个 |
| D.金刚石网状结构中,每个碳原子与4个碳原子形成共价键 |
您最近一年使用:0次
名校
解题方法
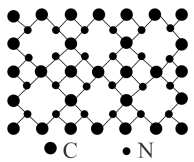
2 . 氮化碳结构如下图所示,其硬度超过金刚石晶体,成为首屈一指的超硬新材料。下列有关氮化碳的说法正确的是


| A.氮化碳属于分子晶体 | B.氮化碳中碳显-4价,氮显+3价 |
| C.氮化碳的化学式为C3N4 | D.每个碳原子与两个氮原子相连,每个氮原子与三个碳原子相连 |
您最近一年使用:0次
2022-06-13更新
|
345次组卷
|
4卷引用:黑龙江省双鸭山市第一中学2021-2022学年高二6月月考化学试题
解题方法
3 . 单质硼的硬度近似于金刚石,有很高的电阻。但它的导电率随温度的升高而增大,高温时为良导体。硼在自然界中主要以硼酸和硼酸盐的形式存在。
(1)基态硼原子的价电子排布式为_______ ,晶体硼的熔沸点_______ (填“高于”或“低于”)金刚石,原因是_______ 。
(2)硼酸与氢氧化钠在一定条件下可以生成四硼酸钠,结构如图所示,四硼酸钠中含有的化学键类型为_______ ,O原子的杂化类型为_______ ,B原子与相连的3个O原子围成的图形为_______ ,第一电离能介于硼元素和氧元素之间的第二周期元素有_______ 种。

(3)硼和氮可以构成多种类型的晶体,其中一种晶体的晶胞如图所示,晶胞上下底面均为菱形,晶胞参数如图所示,该晶体的化学式为_______ ,晶胞密度为_______ (写出表达式即可)。

(1)基态硼原子的价电子排布式为
(2)硼酸与氢氧化钠在一定条件下可以生成四硼酸钠,结构如图所示,四硼酸钠中含有的化学键类型为

(3)硼和氮可以构成多种类型的晶体,其中一种晶体的晶胞如图所示,晶胞上下底面均为菱形,晶胞参数如图所示,该晶体的化学式为

您最近一年使用:0次
名校
解题方法
4 . 已知四种晶体的熔点:
由此得出的推论错误的是
| 物质 | CF4 | SiF4 | BF3 | AlF3 |
| 熔点/℃ | -184 | -90 | -127 | >1000 |
| A.CF4在常温常压下不是固体 | B.分子间作用力: SiF4>CF4 |
| C.BF3一定是分子晶体 | D.AlF3一定是原子晶体 |
您最近一年使用:0次
2022-06-03更新
|
145次组卷
|
2卷引用:上海市复旦大学附属中学2022届高三下学期5月线上测试化学试题
解题方法
5 . “低碳”、“碳中和”有利于全球气候改善。下列有关 的说法错误的是
的说法错误的是
 的说法错误的是
的说法错误的是A. 是极性键构成的非极性分子 是极性键构成的非极性分子 |
| B.“低碳”要求我们要不断地改进燃烧工艺,让燃料更充分燃烧 |
C.大棚种植中 可作为植物生长的“肥料” 可作为植物生长的“肥料” |
D.如果把干冰晶体内原子连接变成与 一样的方式,“干冰”的熔点将高于 一样的方式,“干冰”的熔点将高于 晶体 晶体 |
您最近一年使用:0次
6 . 下面有关晶体的叙述中,不正确的是
| A.干冰晶体中,每个CO2分子周围紧邻12个CO2分子 |
| B.氯化铯晶体中,每个Cs+周围紧邻8个C1- |
| C.氯化钠晶体中,每个Na+周围距离相等的Na+共有6个 |
| D.金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子 |
您最近一年使用:0次
2022-06-02更新
|
147次组卷
|
3卷引用:辽宁省丹东市凤城市第一中学2021-2022学年高二下学期第二次测试化学试题
名校
解题方法
7 . 根据量子力学计算,氮化碳结构有五种,其中一种氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料,已知该氮化碳的二维晶体结构如图所示,下列有关氮化碳的说法不正确的是

| A.氮化碳属于共价晶体 |
| B.氮化碳的化学式为C3N4 |
| C.该晶体中的熔点比金刚石的熔点低 |
| D.每个碳原子与四个氮原子相连,每个氮原子与三个碳原子相连 |
您最近一年使用:0次
名校
解题方法
8 . 下表是某些共价晶体的熔点和硬度,分析表中的数据,下列叙述正确的是
①构成共价晶体的原子种类越多,晶体的熔点越高
②构成共价晶体的原子间的共价键的键能越大,晶体的熔点越高
③构成共价晶体的原子半径越小,晶体的硬度越大
④构成共价晶体的原子半径越大,共价键的键能越大
| 共价晶体 | 金刚石 | 氮化硼 | 碳化硅 | 石英 | 硅 | 锗 |
| 熔点/℃ | 3900 | 3000 | 2700 | 1710 | 1410 | 1211 |
| 莫氏硬度 | 10 | 9.5 | 9.5 | 7 | 6.5 | 6 |
②构成共价晶体的原子间的共价键的键能越大,晶体的熔点越高
③构成共价晶体的原子半径越小,晶体的硬度越大
④构成共价晶体的原子半径越大,共价键的键能越大
| A.①② | B.③④ | C.②③ | D.②④ |
您最近一年使用:0次
9 . 下 列晶体性质的比较中不正确的是
| A.熔点:金刚石>碳化硅>晶体硅 |
| B.沸点: NH3>PH3 |
| C.硬度: K>Na>Li |
| D.熔点: SiI4>SiBr4>SiCl4 |
您最近一年使用:0次
名校
解题方法
10 . SiO2的晶体结构想象为:在晶体硅的Si- Si 键之间插入O原子。见下图,下列说法不正确的是


| A.石英晶体中每个Si原子通过Si- O极性键与4个O原子作用 |
| B.每个O原子也通过Si-O极性键与2个Si原子作用 |
| C.晶体中Si原子与O原子的原子个数比为1: 2,可用“SiO2”作为石英晶体的分子式 |
| D.SiO2晶体中所有键的键长都相同 |
您最近一年使用:0次



