名校
解题方法
1 . X、Y、Z、M为原子序数依次增大的四种短周期主族元素,Y与M同主族,X的一种1∶2型氢化物分子中既有 键又有π键,且所有原子共平面;Y的基态原子L层上有2个未成对电子;Z元素的原子在同周期原子中半径最大。下列说法正确的是
键又有π键,且所有原子共平面;Y的基态原子L层上有2个未成对电子;Z元素的原子在同周期原子中半径最大。下列说法正确的是
 键又有π键,且所有原子共平面;Y的基态原子L层上有2个未成对电子;Z元素的原子在同周期原子中半径最大。下列说法正确的是
键又有π键,且所有原子共平面;Y的基态原子L层上有2个未成对电子;Z元素的原子在同周期原子中半径最大。下列说法正确的是A.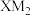 中心原子的杂化方式为sp 中心原子的杂化方式为sp | B.晶体Z的堆积方式为简单立方堆积 |
C.与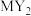 互为等电子体的分子有 互为等电子体的分子有 | D.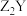 和 和 中化学键类型完全相同 中化学键类型完全相同 |
您最近一年使用:0次
2021-07-09更新
|
546次组卷
|
2卷引用:广东省肇庆市2020-2021学年高二下学期末教学质量检测化学(物质结构与性质)试题
2 . 煤电工业产生的烟气或汽车尾气中常含有NOx、CO等污染大气的气体,其中的NOx来源于如下反应:
反应Ⅰ:
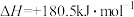
反应Ⅱ: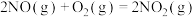
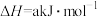
(1)反应Ⅱ在常温下就能自发进行,则a_______ 0。(填“>”或“<”)
(2)煤电工业烟气中的NO可利用“氨法脱硝”处理,其反应为
①反应中,生成 时,被
时,被 氧化的
氧化的 的质量为
的质量为_______ 。
②工业上可利用尿素[ ]水解制得
]水解制得 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(3)为避免汽车尾气中的NOx和CO直接排放到大气中,可利用“三元催化转换器”将其转化为 和
和 。
。
①已知含碳物质参与反应的能量变化如所示,则NO(g)和CO(g)转化为 和
和 的热化学方程式为
的热化学方程式为_______ 。
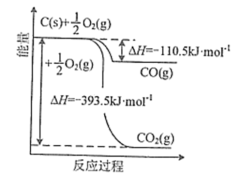
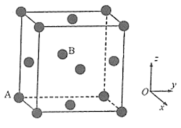
②“三元催化转换器”中用到了金属铂,如图为金属铂的晶胞结构示意图。金属铂晶体中,铂原子周围与之紧邻的其他铂原子数目为_______ 。若A原子的分数坐标为(0,0,0),则B原子的分数坐标为_______ 。
反应Ⅰ:

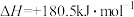
反应Ⅱ:
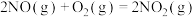
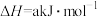
(1)反应Ⅱ在常温下就能自发进行,则a
(2)煤电工业烟气中的NO可利用“氨法脱硝”处理,其反应为

①反应中,生成
 时,被
时,被 氧化的
氧化的 的质量为
的质量为②工业上可利用尿素[
 ]水解制得
]水解制得 ,该反应的化学方程式为
,该反应的化学方程式为(3)为避免汽车尾气中的NOx和CO直接排放到大气中,可利用“三元催化转换器”将其转化为
 和
和 。
。①已知含碳物质参与反应的能量变化如所示,则NO(g)和CO(g)转化为
 和
和 的热化学方程式为
的热化学方程式为
②“三元催化转换器”中用到了金属铂,如图为金属铂的晶胞结构示意图。金属铂晶体中,铂原子周围与之紧邻的其他铂原子数目为

您最近一年使用:0次
名校
3 . 如图所示为金属原子的四种基本堆积(分别为:简单立方堆积、六方最密堆积、面心立方最密堆积、体心立方堆积、)模型,请回答以下问题:
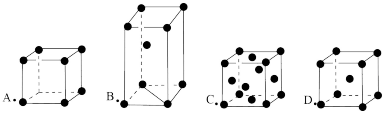
(1)图中原子堆积方式中,空间利用率最低 的是____ (在图中选择,填字母),由非密置层互相错位堆积而成的是_____ 。
(2)金属钛的晶胞为B型,其堆积方式的名称 为_____ 。
(3)某金属R的晶胞为D型,已知R原子半径为rcm,相对原子质量为M,阿佛加得德罗常数为NA,则R金属的密度____ 。(用含r、M、NA字母的式子表示)

(1)图中原子堆积方式中,空间利用率最
(2)金属钛的晶胞为B型,其堆积方式的
(3)某金属R的晶胞为D型,已知R原子半径为rcm,相对原子质量为M,阿佛加得德罗常数为NA,则R金属的密度
您最近一年使用:0次
名校
解题方法
4 . 铁有 、
、 、
、 三种晶体结构,在一定条件下可以相互转化。晶胞结构如图所示,晶胞中距离最近的铁原子均相切。下列说法错误的是
三种晶体结构,在一定条件下可以相互转化。晶胞结构如图所示,晶胞中距离最近的铁原子均相切。下列说法错误的是
 、
、 、
、 三种晶体结构,在一定条件下可以相互转化。晶胞结构如图所示,晶胞中距离最近的铁原子均相切。下列说法错误的是
三种晶体结构,在一定条件下可以相互转化。晶胞结构如图所示,晶胞中距离最近的铁原子均相切。下列说法错误的是
| A.铁的导电性、导热性、延展性都可以用电子气理论来解释 |
B. 、 、 、 、 铁的晶胞中铁原子个数比为1∶4∶2 铁的晶胞中铁原子个数比为1∶4∶2 |
C. 、 、 、 、 铁的晶胞边长的之比为 铁的晶胞边长的之比为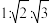 |
D. 铁在一定条件下转化为 铁在一定条件下转化为 铁后密度变小 铁后密度变小 |
您最近一年使用:0次
2021-05-31更新
|
815次组卷
|
2卷引用:辽宁省协作校2020-2021学年高二下学期期中考试化学试题
解题方法
5 . 金属铁有δ、γ、α三种结构,各晶胞如图。下列说法不正确的是
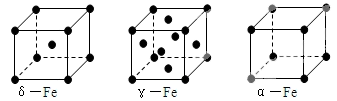

| A.三种晶胞中实际含有的铁原子的个数之比为2:4:1 |
| B.三种晶胞中铁原子的配位数之比为1:3:2 |
| C.三种晶胞密度之比为32: 37 :29 |
D.δ-Fe晶胞的空间利用率为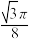 |
您最近一年使用:0次
名校
解题方法
6 . 按照要求回答下列问题。
(1)高温下,Cu2O比CuO稳定,原因是___________ 。
(2)过渡元素的原子或者离子很容易形成配合物,Fe(CO)5就是其一,它相当活泼,在一定条件下可生成Fe(CO)3(CH3OH)。1.5 mol Fe(CO)5中所含配位键的个数为___________ ,Fe(CO)3(CH3OH)的配位原子为___________ 。(填元素符号)
(3)第四周期第一电离能数值介于Ga和As之间的主族元素有:___________ 。(填名称)
(4)金属钛重量轻、强度高,航空发动机用的高温钛合金和机体用的结构钛合金是钛合金的主要发展方向。钛原子的外围电子排布图为___________ 。已知金属Be的堆积方式与金属钛相同,则堆积方式为___________ ,Be与NaOH溶液反应的离子方程式为___________ 。
(5)Sr晶体堆积方式与Cu相似,设Sr的原子直径为a,则Sr晶体的空间利用率为___________ 。(请用含有a的表达式表示,不要化简)
(1)高温下,Cu2O比CuO稳定,原因是
(2)过渡元素的原子或者离子很容易形成配合物,Fe(CO)5就是其一,它相当活泼,在一定条件下可生成Fe(CO)3(CH3OH)。1.5 mol Fe(CO)5中所含配位键的个数为
(3)第四周期第一电离能数值介于Ga和As之间的主族元素有:
(4)金属钛重量轻、强度高,航空发动机用的高温钛合金和机体用的结构钛合金是钛合金的主要发展方向。钛原子的外围电子排布图为
(5)Sr晶体堆积方式与Cu相似,设Sr的原子直径为a,则Sr晶体的空间利用率为
您最近一年使用:0次
解题方法
7 . (1)钛铁合金具有吸氢特性,工业在制造以氢为能源的热泵和蓄电池等方面有广阔的应用前景,金属Ti(六方最密堆积)的原子空间利用率约为_______ ,基态Ti原子核外有_______ 个运动状态不同的电子,在基态Ti2+中,电子占据的能量最高的轨道为_______ 。
(2)已知Si-Si键能为176 kJ/mol,Si-O键能为460 kJ/mol,O=O键能为497.3 kJ/mol,则可计算出1 mol硅与足量氧气反应时将放出_______ kJ的热量。
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关,一般为d0或d10排布时,无颜色;为d1~d9排布时,有颜色。如[Co(H2O)6]2+显粉红色,据此判断 [Mn(H2O)6]2+_______ (填“无”或“有”)颜色。
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。COCl2分子的空间构型为_______ ;Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g),反应过程中,断裂的化学键只有配位键,则形成的化学键类型是_______ 。
(5)最近,由镁、镍和碳三种元素组成的化合物引起了科学家的注意。据报道,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构可看作由镁原子和镍原子在一起进行面心立方最密堆积(如图),则该晶体中镁、碳、镍三种元素的原子个数比是_______ ,晶体中每个镁原子周围距离最近的镍原子有_______ 个。
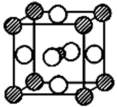
(图中:碳原子用小 球在晶体的体心,镍原子用大
球在晶体的体心,镍原子用大 球,镁原子用大
球,镁原子用大 球)
球)
(2)已知Si-Si键能为176 kJ/mol,Si-O键能为460 kJ/mol,O=O键能为497.3 kJ/mol,则可计算出1 mol硅与足量氧气反应时将放出
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关,一般为d0或d10排布时,无颜色;为d1~d9排布时,有颜色。如[Co(H2O)6]2+显粉红色,据此判断 [Mn(H2O)6]2+
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。COCl2分子的空间构型为
(5)最近,由镁、镍和碳三种元素组成的化合物引起了科学家的注意。据报道,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构可看作由镁原子和镍原子在一起进行面心立方最密堆积(如图),则该晶体中镁、碳、镍三种元素的原子个数比是

(图中:碳原子用小
 球在晶体的体心,镍原子用大
球在晶体的体心,镍原子用大 球,镁原子用大
球,镁原子用大 球)
球)
您最近一年使用:0次
名校
解题方法
8 . 下列关于晶体结构的说法错误的是
| A.碳化硅晶体中,所有原子都是sp3杂化,一个晶胞平均占有8个原子 |
| B.金属钾是非密置层在三维空间里堆积出来的,钾原子的配位数为8 |
| C.石墨晶体中C原子与C-C键个数比为1:3,金刚石晶体中C原子与C-C键个数比为1:4 |
| D.金属Ag的堆积类型为面心立方最密堆积,空间利用率78% |
您最近一年使用:0次
2021-04-30更新
|
146次组卷
|
2卷引用:河北省秦皇岛市第一中学2020-2021学年高二下学期第一次月考化学试题
名校
解题方法
9 . 金属铜的晶胞结构如图所示,下列有关说法正确的是
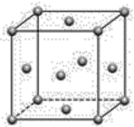

| A.金属钋也采取这种堆积方式 |
| B.这种堆积方式中,金属原子的配位数为12 |
| C.每个晶胞中含有4个Cu原子 |
| D.这种堆积方式的空间利用率较低 |
您最近一年使用:0次



