名校
解题方法
1 . 下列关于分离或提纯说法正确的是
| A.可用饱和食盐水溶液除去Cl2中的HCl气体 |
| B.粗盐提纯过程中涉及过滤、蒸发、分液等操作 |
| C.除去SO2中的H2S,可以通入酸性高锰酸钾溶液洗气 |
| D.除去FeCl2溶液中少量FeCl3,可以加入足量铜粉后过滤 |
您最近一年使用:0次
名校
解题方法
2 . 为贯彻低碳循环的绿色发展理念,实现对废旧电池的高效资源化回收,湖南科技大学研究团队通过双氧水氧化→酸浸→浸出液二次浸出的工艺,回收废旧磷酸铁锂电池正极材料( )中的锂,同时得到有用的磷酸铁(
)中的锂,同时得到有用的磷酸铁( ),其工艺流程如下。回答下列问题:
),其工艺流程如下。回答下列问题:

(1)基态Fe原子的价层电子轨道表达式为___________ , 的电子式为
的电子式为___________ 。
(2)第一次浸出实验在一定条件下,浸出时间和浸出温度对Li、Fe、P的浸出率影响如下图所示。

①考虑实验效率和实际工业生产要求,选择的最佳浸出时间:___________ ,最佳浸出温度___________ 。
②随着浸出温度的上升,一定温度后Li的浸出率呈现下降的趋势,可能的原因为___________ 。
③滤渣A的主要成分为___________ ,则第一次浸出时主要反应的化学方程式为_________ 。
(3)除杂时加入NaOH的作用为调节溶液pH,使 沉淀完全,则调pH不得低于
沉淀完全,则调pH不得低于_________ 。
(已知: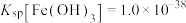 )
)
(4)提纯碳酸锂产品时得到的母液的主要成分是___________ (填化学式)。
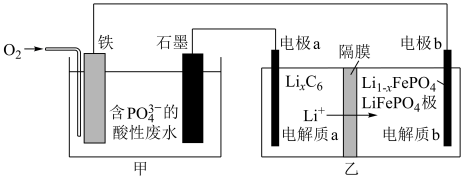
(5)某科研小组探究用磷酸铁锂电池处理含 的酸性废水,以得到有用的
的酸性废水,以得到有用的 ,其装置如图所示:请写出甲池中生成
,其装置如图所示:请写出甲池中生成 的反应方程式:
的反应方程式:___________ 。
 )中的锂,同时得到有用的磷酸铁(
)中的锂,同时得到有用的磷酸铁( ),其工艺流程如下。回答下列问题:
),其工艺流程如下。回答下列问题:
(1)基态Fe原子的价层电子轨道表达式为
 的电子式为
的电子式为(2)第一次浸出实验在一定条件下,浸出时间和浸出温度对Li、Fe、P的浸出率影响如下图所示。

①考虑实验效率和实际工业生产要求,选择的最佳浸出时间:
②随着浸出温度的上升,一定温度后Li的浸出率呈现下降的趋势,可能的原因为
③滤渣A的主要成分为
(3)除杂时加入NaOH的作用为调节溶液pH,使
 沉淀完全,则调pH不得低于
沉淀完全,则调pH不得低于(已知:
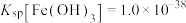 )
)(4)提纯碳酸锂产品时得到的母液的主要成分是
(5)某科研小组探究用磷酸铁锂电池处理含
 的酸性废水,以得到有用的
的酸性废水,以得到有用的 ,其装置如图所示:请写出甲池中生成
,其装置如图所示:请写出甲池中生成 的反应方程式:
的反应方程式:
您最近一年使用:0次
3 . 氯溴酸在医药和石化工业上有广泛用途,模拟工业制备氢溴酸的流程如图所示。下列说法不正确的是
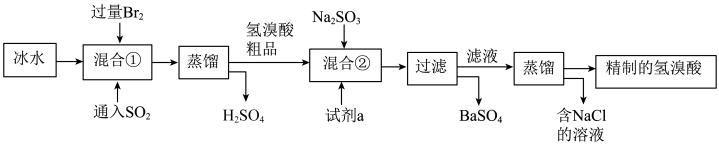

A.混合①使用冰水的目的是防止 和HBr挥发 和HBr挥发 |
B. 可除去氢溴酸粗品中的 可除去氢溴酸粗品中的 ,发生的离子反应为 ,发生的离子反应为 |
| C.蒸馏时,加完“滤液”后,先通冷凝水,再点燃酒精灯加热 |
D.工业氢溴酸常带有淡淡的黄色,可能是因为含有 |
您最近一年使用:0次
名校
解题方法
4 . 某兴趣小组设计如图实验装置制备次磷酸钠( )。
)。
已知:①白磷( )在空气中可自燃,与过量烧碱溶液混合,80~90℃时反应生成
)在空气中可自燃,与过量烧碱溶液混合,80~90℃时反应生成 和
和 。
。
② 是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成
是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成 。
。
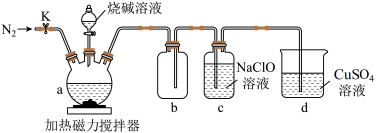
(1)仪器a的名称是___________ 。a中发生反应的化学方程式是___________ 。
(2)仪器b组成的装置的作用是___________ ,检查装置气密性后,应先打开K通入 一段时间,目的是
一段时间,目的是___________ 。
(3)下列有关说法正确的是___________。
(4)①仪器c中充分反应后生成 和NaCl,经过一系列操作可获得固体
和NaCl,经过一系列操作可获得固体 。相关物质的溶解度(S)如下:
。相关物质的溶解度(S)如下:
从下列选项a-g中选择合理的仪器或操作,补全如下步骤。
取仪器c中溶液,用蒸发皿___________ →用___________ (趁热过滤)→用烧杯(冷却结晶)→用漏斗(过滤得到 )→
)→___________ →干燥 粗品。
粗品。
选项:a.溶解 b.过滤 c.洗涤 d.普通三角漏斗 e.保温漏斗
f.蒸发浓缩至有大量晶体析出 g.蒸发浓缩至溶液表面出现晶膜
②写出c中发生反应的离子方程式___________ 。
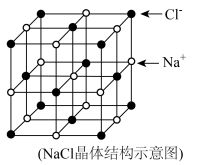
(5)NaCl晶胞结构如图,设距离最近的 间的距离为apm,
间的距离为apm, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为___________  。(列出计算式即可)
。(列出计算式即可)
 )。
)。已知:①白磷(
 )在空气中可自燃,与过量烧碱溶液混合,80~90℃时反应生成
)在空气中可自燃,与过量烧碱溶液混合,80~90℃时反应生成 和
和 。
。②
 是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成
是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成 。
。
(1)仪器a的名称是
(2)仪器b组成的装置的作用是
 一段时间,目的是
一段时间,目的是(3)下列有关说法正确的是___________。
A.次磷酸( )是三元酸 )是三元酸 |
| B.为加快反应速率,投料前应先在通风橱内将白磷碾成薄片状 |
C.反应结束后应继续通入 一段时间,可提高 一段时间,可提高 产率 产率 |
| D.d中所盛硫酸铜溶液可用酸性高锰酸钾溶液代替 |
(4)①仪器c中充分反应后生成
 和NaCl,经过一系列操作可获得固体
和NaCl,经过一系列操作可获得固体 。相关物质的溶解度(S)如下:
。相关物质的溶解度(S)如下: | S(25℃) | S(100℃) | |
| NaCl | 37 | 39 |
 | 100 | 667 |
取仪器c中溶液,用蒸发皿
 )→
)→ 粗品。
粗品。选项:a.溶解 b.过滤 c.洗涤 d.普通三角漏斗 e.保温漏斗
f.蒸发浓缩至有大量晶体析出 g.蒸发浓缩至溶液表面出现晶膜
②写出c中发生反应的离子方程式
(5)NaCl晶胞结构如图,设距离最近的
 间的距离为apm,
间的距离为apm, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为 。(列出计算式即可)
。(列出计算式即可)
您最近一年使用:0次
名校
解题方法
5 . 门捷列夫最早预言了具有半导体特性类硅元素锗(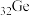 ),工业上用精硫锗矿(主要成分为
),工业上用精硫锗矿(主要成分为 )制取高纯度锗,其工艺流程如图所示:
)制取高纯度锗,其工艺流程如图所示:
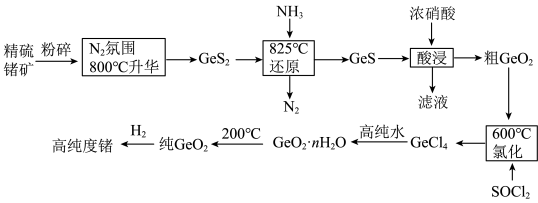
已知:①硅和锗是同主族相邻元素,结构和性质类似;
②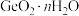 在5.3
在5.3  的盐酸中溶解度最小。
的盐酸中溶解度最小。
(1)基态锗原子的价层电子排布式为___________ ,晶体锗的晶体类型是___________ 。
(2)800℃,使精硫锗矿在 氛围中升华的原因:
氛围中升华的原因:___________ 。
(3)还原时发生反应: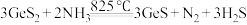 ,比较键角:
,比较键角:
___________  (填“>”“<”或“=”),其原因是(从杂化和价层电子对互斥角度解释)
(填“>”“<”或“=”),其原因是(从杂化和价层电子对互斥角度解释)___________ 。
(4)酸浸时温度不能过高的原因:___________ 。
(5)氯化除生成 外,反应还生成一种V形分子,写出相应的化学方程式:
外,反应还生成一种V形分子,写出相应的化学方程式:___________ 。
(6) 水解得到
水解得到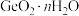 ,该步骤高纯水不能过量,原因是
,该步骤高纯水不能过量,原因是___________ 。
(7)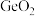 与碱反应可生成锗酸盐,其中
与碱反应可生成锗酸盐,其中 是一种难溶电解质,一定温度下,
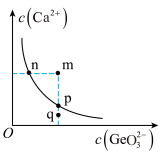
是一种难溶电解质,一定温度下, 在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是___________(填标号)。
在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是___________(填标号)。
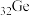 ),工业上用精硫锗矿(主要成分为
),工业上用精硫锗矿(主要成分为 )制取高纯度锗,其工艺流程如图所示:
)制取高纯度锗,其工艺流程如图所示:
已知:①硅和锗是同主族相邻元素,结构和性质类似;
②
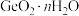 在5.3
在5.3  的盐酸中溶解度最小。
的盐酸中溶解度最小。(1)基态锗原子的价层电子排布式为
(2)800℃,使精硫锗矿在
 氛围中升华的原因:
氛围中升华的原因:(3)还原时发生反应:
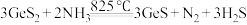 ,比较键角:
,比较键角:
 (填“>”“<”或“=”),其原因是(从杂化和价层电子对互斥角度解释)
(填“>”“<”或“=”),其原因是(从杂化和价层电子对互斥角度解释)(4)酸浸时温度不能过高的原因:
(5)氯化除生成
 外,反应还生成一种V形分子,写出相应的化学方程式:
外,反应还生成一种V形分子,写出相应的化学方程式:(6)
 水解得到
水解得到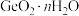 ,该步骤高纯水不能过量,原因是
,该步骤高纯水不能过量,原因是(7)
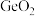 与碱反应可生成锗酸盐,其中
与碱反应可生成锗酸盐,其中 是一种难溶电解质,一定温度下,
是一种难溶电解质,一定温度下, 在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是___________(填标号)。
在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是___________(填标号)。
A.n点与p点对应的 相等 相等 |
B.q点无 沉淀生成 沉淀生成 |
| C.通过蒸发可以使溶液由q点变到p点 |
D.加入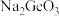 可以使溶液由n点变到m点 可以使溶液由n点变到m点 |
您最近一年使用:0次
2023-09-01更新
|
1140次组卷
|
8卷引用:广西柳州高级中学2023-2024学年高三上学期10月月考化学试题
名校
解题方法
6 . 实验室中用山梨酸和乙醇催化合成山梨酸乙酯的过程如下所示,下列说法错误的是
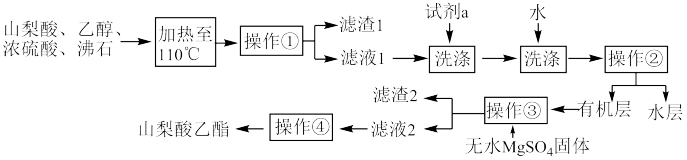

| A.反应时不能用水浴进行加热 |
| B.试剂a可以是5%NaOH溶液,目的是除去滤液1中的山梨酸和硫酸杂质 |
| C.操作①和操作③基本原理相同,操作②和操作④基本原理不同 |
| D.加入无水MgSO4固体的目的是除去有机物中的水分 |
您最近一年使用:0次
2023-02-21更新
|
1445次组卷
|
13卷引用:广西柳州高级中学2023-2024学年高三上学期10月月考化学试题
广西柳州高级中学2023-2024学年高三上学期10月月考化学试题江西省赣州市重点中学九校联盟2022-2023学年高二下学期第一次月考化学试题湖南省名校大联考2024届高三上学期第一次质量检测化学试题湖南省炎德英才联考2024届高三上学期第一次质量检测化学试题江西省宜春市宜丰中学创新部2023-2024学年高三上学期第一次月考化学试题湖南省长沙市湖南师范大学附属中学2023-2024学年高三上学期第一次质量检测化学试题福建省福州高级中学2023-2024学年高三第二次阶段考试化学试题山东省威海市2022-2023学年高三上学期期末考试化学试题(已下线)山东省青岛市2023届高三下学期一模化学试题变式题(选择题6-10)(已下线)素养卷08 微型化学工艺流程分析-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)湖南四大名校2024届高三上学期第一次联考化学试题湖南省长沙市长郡中学、衡阳市第八中学2024届高三8月大联考化学试题河南省兰考县第一高级中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
7 . 刚玉在工业上有广泛的用途,其主要成分为 氧化铝。利用铝灰(主要成分为
氧化铝。利用铝灰(主要成分为 ,含少量杂质
,含少量杂质 、FeO、
、FeO、 )制备刚玉的工艺流程如下:
)制备刚玉的工艺流程如下: 是酸性氧化物,且不与水反应。
是酸性氧化物,且不与水反应。
回答下列问题:
(1)滤渣的主要成分是_____ (填化学式);过滤时用到的玻璃仪器有漏斗、烧杯和______ 。
(2)“氧化”操作的目的为_______ ,该过程中发生反应的离子方程式为_______ 。
(3)已知:生成氢氧化物沉淀的pH如下表所示。
用氨水“调节pH”,pH的范围是_______ 。
(4)写出用氨水调节pH生成 沉淀的离子方程式:
沉淀的离子方程式:_______ 。
(5)往 中滴加NaOH溶液,可以看到沉淀溶解,写出反应的化学方程式:
中滴加NaOH溶液,可以看到沉淀溶解,写出反应的化学方程式:_______ 。
 氧化铝。利用铝灰(主要成分为
氧化铝。利用铝灰(主要成分为 ,含少量杂质
,含少量杂质 、FeO、
、FeO、 )制备刚玉的工艺流程如下:
)制备刚玉的工艺流程如下:
 是酸性氧化物,且不与水反应。
是酸性氧化物,且不与水反应。回答下列问题:
(1)滤渣的主要成分是
(2)“氧化”操作的目的为
(3)已知:生成氢氧化物沉淀的pH如下表所示。
| 氢氧化物 |  |  |  |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
(4)写出用氨水调节pH生成
 沉淀的离子方程式:
沉淀的离子方程式:(5)往
 中滴加NaOH溶液,可以看到沉淀溶解,写出反应的化学方程式:
中滴加NaOH溶液,可以看到沉淀溶解,写出反应的化学方程式:
您最近一年使用:0次
2023-01-06更新
|
138次组卷
|
3卷引用:广西柳州高级中学2023-2024学年高一上学期寒假月考四化学试题
名校
8 . 羟基氧化镍 常作为锌镍电池的正极活性物质,也是重要的化工原料。工业上用含NiO的废料(杂质为
常作为锌镍电池的正极活性物质,也是重要的化工原料。工业上用含NiO的废料(杂质为 、CaO、ZnO,CuO等)制备羟基氧化镍的一种工艺流程如下:
、CaO、ZnO,CuO等)制备羟基氧化镍的一种工艺流程如下:

已知:相关金属离子形成氢氧化物沉淀的pH如下表(各离子浓度均为 )。
)。
请回答下列问题:
(1)酸浸时需将废料粉碎,目的是_______ 。
(2)某实验小组用 的硫酸进行酸浸。绘制了如图:
的硫酸进行酸浸。绘制了如图:


①由图一可知,固液比与镍浸出率的关系是_______ 。
②由图二可知,酸浸时合适的浸出温度是_______ ℃左右,若温度过高,则滤渣1中有氢氧化镍产生。
(3)向滤液2中加入FeS是为了除去 ,
, 。当
。当 恰好沉淀完全时,
恰好沉淀完全时,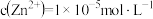 ,则
,则
_______  。[已知
。[已知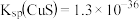 ,
, ]
]
(4)加入 溶液的作用是
溶液的作用是_______ 。试剂X用于调节溶液的pH,则应调节pH的范围是_______ 。
 常作为锌镍电池的正极活性物质,也是重要的化工原料。工业上用含NiO的废料(杂质为
常作为锌镍电池的正极活性物质,也是重要的化工原料。工业上用含NiO的废料(杂质为 、CaO、ZnO,CuO等)制备羟基氧化镍的一种工艺流程如下:
、CaO、ZnO,CuO等)制备羟基氧化镍的一种工艺流程如下:
已知:相关金属离子形成氢氧化物沉淀的pH如下表(各离子浓度均为
 )。
)。| 离子 |  |  |  |
| 开始沉淀的pH | 1.9 | 7.0 | 7.1 |
| 沉淀完全的pH | 3.2 | 9.0 | 9.2 |
(1)酸浸时需将废料粉碎,目的是
(2)某实验小组用
 的硫酸进行酸浸。绘制了如图:
的硫酸进行酸浸。绘制了如图:

①由图一可知,固液比与镍浸出率的关系是
②由图二可知,酸浸时合适的浸出温度是
(3)向滤液2中加入FeS是为了除去
 ,
, 。当
。当 恰好沉淀完全时,
恰好沉淀完全时,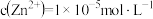 ,则
,则
 。[已知
。[已知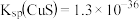 ,
, ]
](4)加入
 溶液的作用是
溶液的作用是
您最近一年使用:0次
9 . 以绿矾(主要成分为FeSO4·7H2O,部分Fe2+已被氧化为Fe3+)为原料,生产铁红(Fe2O3)的工艺流程如下:

(1)“转化”过程中,加入Fe粉的作用是___________ 。转化前将绿矾研碎,转化中进行搅拌和加热,目的是___________ 。
(2)“结晶”时,控制温度在75°C左右进行(相关物质的溶解度见下图),从溶液中析出的晶体是___________ (填化学式)。

(3)“滤液”中的溶质为___________ (填化学式)。利用该滤液将工业废水中的Cr2O 还原为Cr3+,然后投加石灰乳,使Cr3+转化为Cr(OH)3沉淀,理论上完全反应消耗的n(Cr2O
还原为Cr3+,然后投加石灰乳,使Cr3+转化为Cr(OH)3沉淀,理论上完全反应消耗的n(Cr2O ):n(FeSO4)=
):n(FeSO4)=___________ 。
(4)“煅烧”过程中,每生成1mol铁红,需消耗___________ molO2,同时生成___________ molSO3和___________ molH2O。

(1)“转化”过程中,加入Fe粉的作用是
(2)“结晶”时,控制温度在75°C左右进行(相关物质的溶解度见下图),从溶液中析出的晶体是

(3)“滤液”中的溶质为
 还原为Cr3+,然后投加石灰乳,使Cr3+转化为Cr(OH)3沉淀,理论上完全反应消耗的n(Cr2O
还原为Cr3+,然后投加石灰乳,使Cr3+转化为Cr(OH)3沉淀,理论上完全反应消耗的n(Cr2O ):n(FeSO4)=
):n(FeSO4)=(4)“煅烧”过程中,每生成1mol铁红,需消耗
您最近一年使用:0次
2022-03-16更新
|
162次组卷
|
2卷引用:广西柳州市鹿寨县鹿寨中学2021-2022学年高二上学期第三次统测化学试题
名校
解题方法
10 . 某研究小组以工厂废渣(含Fe3O4、Al2O3、SiO2)为原料制取Fe2O3工艺流程如图。回答下列问题:

已知:SiO2不溶于水,不与H2SO4反应,能与NaOH溶液反应。
(1)“酸溶”时发生反应的化学方程式为____ 。
(2)“操作a”的名称为____ ,用到的玻璃仪器有玻璃棒、____ 。
(3)①“氧化”的目的是___ 。检验氧化不完全可加入的试剂是___ 。___ 用H2O2代替O2(填“能”或“不能”)。
②若O2完全“氧化”溶液中的溶质,取出部分被完全氧化后的溶液,将Cu片放入,反应一段时间后取出Cu片,溶液中c(Fe3+):c(Fe2+)=2:3,则溶液中Cu2+和Fe3+的物质的量之比为___ (不考虑溶液体积变化)
(4)“沉铁”步骤可观察到现象是____ 。___ 用氨水代替NaOH溶液(填“能”或“不能”)。
(5)操作c中所发生的化学反应方程式为____ 。

已知:SiO2不溶于水,不与H2SO4反应,能与NaOH溶液反应。
(1)“酸溶”时发生反应的化学方程式为
(2)“操作a”的名称为
(3)①“氧化”的目的是
②若O2完全“氧化”溶液中的溶质,取出部分被完全氧化后的溶液,将Cu片放入,反应一段时间后取出Cu片,溶液中c(Fe3+):c(Fe2+)=2:3,则溶液中Cu2+和Fe3+的物质的量之比为
(4)“沉铁”步骤可观察到现象是
(5)操作c中所发生的化学反应方程式为
您最近一年使用:0次



