名校
解题方法
1 . 下列关于分离或提纯说法正确的是
| A.可用饱和食盐水溶液除去Cl2中的HCl气体 |
| B.粗盐提纯过程中涉及过滤、蒸发、分液等操作 |
| C.除去SO2中的H2S,可以通入酸性高锰酸钾溶液洗气 |
| D.除去FeCl2溶液中少量FeCl3,可以加入足量铜粉后过滤 |
您最近一年使用:0次
解题方法
2 . 氯氧化铋(BiOCl)广泛用于彩釉调料、塑料助剂、油漆调色等。工业上常用辉铋矿(主要成分是 ,还含有少量
,还含有少量 、铁的氧化物等杂质)为原料制备氯氧化铋。
、铁的氧化物等杂质)为原料制备氯氧化铋。 在
在 时开始水解,
时开始水解,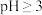 时几乎完全水解为白色的BiOCl沉淀;
时几乎完全水解为白色的BiOCl沉淀;
②该工艺下,有关金属离子开始沉淀和沉淀完全的pH见下表。
(1)铋与氮同主族,且位于元素周期表的第六周期,基态Bi的价电子排布式为___________ 。
(2)“浸渣”的主要成分是S和___________ ,“浸取”时生成S的离子方程式为___________ 。
(3)“充分搅拌”时加入盐酸羟胺的目的是___________ 。
(4)加入碳酸钠粉末制取BiOCl时,溶液pH值需控制的合理范围为___________ ,发生反应的化学方程式为___________ 。
(5)氯氧化铋(BiOCl)可用作钾离子电池(有机物作离子导体)的负极材料,充电时嵌入 ,BiOCl被还原为Bi,则阴极的电极反应式是
,BiOCl被还原为Bi,则阴极的电极反应式是___________ 。
(6)铋的一种氧化物的立方晶胞结构如图所示,已知最近的两个铋离子之间的距离为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该晶体的密度为
,则该晶体的密度为___________  (列出计算式即可)。
(列出计算式即可)。
 ,还含有少量
,还含有少量 、铁的氧化物等杂质)为原料制备氯氧化铋。
、铁的氧化物等杂质)为原料制备氯氧化铋。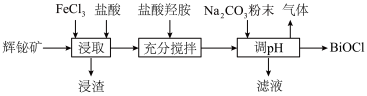
 在
在 时开始水解,
时开始水解,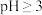 时几乎完全水解为白色的BiOCl沉淀;
时几乎完全水解为白色的BiOCl沉淀;②该工艺下,有关金属离子开始沉淀和沉淀完全的pH见下表。
| 金属离子 |  |  |
| 开始沉淀的pH | 1.9 | 7.2 |
| 沉淀完全的pH | 2.9 | 8.2 |
(1)铋与氮同主族,且位于元素周期表的第六周期,基态Bi的价电子排布式为
(2)“浸渣”的主要成分是S和
(3)“充分搅拌”时加入盐酸羟胺的目的是
(4)加入碳酸钠粉末制取BiOCl时,溶液pH值需控制的合理范围为
(5)氯氧化铋(BiOCl)可用作钾离子电池(有机物作离子导体)的负极材料,充电时嵌入
 ,BiOCl被还原为Bi,则阴极的电极反应式是
,BiOCl被还原为Bi,则阴极的电极反应式是(6)铋的一种氧化物的立方晶胞结构如图所示,已知最近的两个铋离子之间的距离为
 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式即可)。
(列出计算式即可)。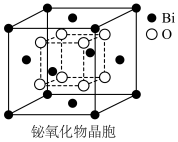
您最近一年使用:0次
2024-04-01更新
|
506次组卷
|
3卷引用:广西壮族自治区柳州市2024届高三第三次模拟考试化学试题
广西壮族自治区柳州市2024届高三第三次模拟考试化学试题广西柳州市2024届高三下学期第三次模拟考试(三模)化学试题(已下线)题型10 工艺流程题(25题)-2024年高考化学常考点必杀300题(新高考通用)
名校
解题方法
3 . 对某溶液中部分离子的定性检测流程如下。相关分析正确的是

| A.步骤①所加试剂可以是浓KOH溶液 |
| B.可以用湿润的蓝色石蕊试纸检验生成的无色气体 |
C.步骤②发生的反应为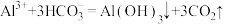 |
D. 遇铁氰化钾会生成蓝色溶液 遇铁氰化钾会生成蓝色溶液 |
您最近一年使用:0次
2024-03-06更新
|
553次组卷
|
14卷引用:【全国百强校】广西柳州高级中学2018届高三5月冲刺模拟理科综合化学试题
【全国百强校】广西柳州高级中学2018届高三5月冲刺模拟理科综合化学试题四川省成都市2018届高三第二次诊断性检测理综化学试题四川省成都外国语学校2017-2018学年高二6月(零诊模拟)月考化学试题山东省泰安第一中学2020届高三上学期期中模拟联合考试化学试题宁夏固原市五原中学补习部2021届高三上学期期中考试化学试题陕西省宝鸡市金台区2021届高三11月检测理综化学试题辽宁省沈阳市郊联体2021届高三上学期期末考试化学试题(已下线)专题04 离子反应(缺项配平、离子检验、离子推断、共存)-2021年高考化学必做热点专题(已下线)小题07 描述型实验选择题(侧重物质检验、定量实验) ——备战2021年高考化学经典小题考前必刷(全国通用)黑龙江省哈尔滨市第九中学2020-2021学年高二下学期6月月考化学试题2024届四川省成都市第七中学高三下学期二模诊断考试理综试题-高中化学 2024届四川省成都市第七中学高三下学期二诊模拟考试理综试卷-高中化学2024届四川省仁寿第一中学校(北校区)二模理综试题-高中化学(已下线)化学(山东卷02)-2024年高考押题预测卷
名校
4 . 实验室模拟侯氏制碱法制备 的主要过程如下,下列说法正确的是
的主要过程如下,下列说法正确的是
 的主要过程如下,下列说法正确的是
的主要过程如下,下列说法正确的是
A.实验时应先向饱和食盐水中通入足量 再通入 再通入 |
| B.过程①②③均涉及过滤操作 |
C.向溶液A中加入 的作用是增大 的作用是增大 浓度,促进 浓度,促进 结晶析出 结晶析出 |
D.实验过程中可循环使用的物质只有 |
您最近一年使用:0次
名校
5 . 某废催化剂含 、ZnS、CuS及少量的
、ZnS、CuS及少量的 ,某实验小组以该废催化剂为原料,制备锌和铜的硫酸盐的结晶水合物,设计实验流程如下:
,某实验小组以该废催化剂为原料,制备锌和铜的硫酸盐的结晶水合物,设计实验流程如下:
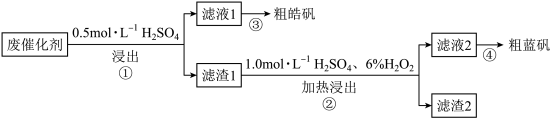
下列说法正确的是
 、ZnS、CuS及少量的
、ZnS、CuS及少量的 ,某实验小组以该废催化剂为原料,制备锌和铜的硫酸盐的结晶水合物,设计实验流程如下:
,某实验小组以该废催化剂为原料,制备锌和铜的硫酸盐的结晶水合物,设计实验流程如下:
下列说法正确的是
A.步骤①操作中,生成的气体需用NaOH溶液或 溶液吸收 溶液吸收 |
B.步骤②操作中,应先加 ,然后不断搅拌下缓慢加入 ,然后不断搅拌下缓慢加入 |
C.滤渣2成分为 ,能与NaOH溶液或氢氟酸反应,是两性氧化物 ,能与NaOH溶液或氢氟酸反应,是两性氧化物 |
D.检验滤液1中是否含有 ,可以选用KSCN溶液和新制的氯水 ,可以选用KSCN溶液和新制的氯水 |
您最近一年使用:0次
名校
解题方法
6 . 利用废旧铁铜粉可以制备补血剂原料碳酸亚铁和杀菌剂胆矾。流程如下图所示:

(1)“滤液1”中一定含有的金属阳离子________ ,写出检验该金属阳离子的方法_________ 。
(2)写出“沉淀”过程中发生反应的离子方程式___________ 。
(3)向 固体中加入热蒸馏水,固体未见明显减少,一段时间后,难溶物上方出现红褐色氢氧化物并有气泡产生。试写出所发生的化学方程式
固体中加入热蒸馏水,固体未见明显减少,一段时间后,难溶物上方出现红褐色氢氧化物并有气泡产生。试写出所发生的化学方程式___________ 。
(4)“溶解1”过程温度不宜过高的原因是___________ 。
(5)胆矾结晶水测定:称量干燥坩埚的质量为 ,加入胆矾后总质量为
,加入胆矾后总质量为 ,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为
,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为 。根据实验数据,胆矾分子中结晶水的个数为
。根据实验数据,胆矾分子中结晶水的个数为___________ (写表达式),下列操作中,会导致结晶水数目测定值偏高的是___________ 。
A.胆矾未充分干燥 B.坩埚未置于干燥器中冷却 C.加热时有少胆矾迸溅出来

(1)“滤液1”中一定含有的金属阳离子
(2)写出“沉淀”过程中发生反应的离子方程式
(3)向
 固体中加入热蒸馏水,固体未见明显减少,一段时间后,难溶物上方出现红褐色氢氧化物并有气泡产生。试写出所发生的化学方程式
固体中加入热蒸馏水,固体未见明显减少,一段时间后,难溶物上方出现红褐色氢氧化物并有气泡产生。试写出所发生的化学方程式(4)“溶解1”过程温度不宜过高的原因是
(5)胆矾结晶水测定:称量干燥坩埚的质量为
 ,加入胆矾后总质量为
,加入胆矾后总质量为 ,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为
,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为 。根据实验数据,胆矾分子中结晶水的个数为
。根据实验数据,胆矾分子中结晶水的个数为A.胆矾未充分干燥 B.坩埚未置于干燥器中冷却 C.加热时有少胆矾迸溅出来
您最近一年使用:0次
名校
解题方法
7 . 为贯彻低碳循环的绿色发展理念,实现对废旧电池的高效资源化回收,湖南科技大学研究团队通过双氧水氧化→酸浸→浸出液二次浸出的工艺,回收废旧磷酸铁锂电池正极材料( )中的锂,同时得到有用的磷酸铁(
)中的锂,同时得到有用的磷酸铁( ),其工艺流程如下。回答下列问题:
),其工艺流程如下。回答下列问题:

(1)基态Fe原子的价层电子轨道表达式为___________ , 的电子式为
的电子式为___________ 。
(2)第一次浸出实验在一定条件下,浸出时间和浸出温度对Li、Fe、P的浸出率影响如下图所示。

①考虑实验效率和实际工业生产要求,选择的最佳浸出时间:___________ ,最佳浸出温度___________ 。
②随着浸出温度的上升,一定温度后Li的浸出率呈现下降的趋势,可能的原因为___________ 。
③滤渣A的主要成分为___________ ,则第一次浸出时主要反应的化学方程式为_________ 。
(3)除杂时加入NaOH的作用为调节溶液pH,使 沉淀完全,则调pH不得低于
沉淀完全,则调pH不得低于_________ 。
(已知: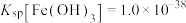 )
)
(4)提纯碳酸锂产品时得到的母液的主要成分是___________ (填化学式)。
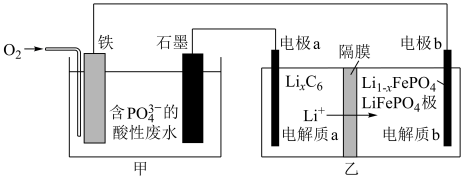
(5)某科研小组探究用磷酸铁锂电池处理含 的酸性废水,以得到有用的
的酸性废水,以得到有用的 ,其装置如图所示:请写出甲池中生成
,其装置如图所示:请写出甲池中生成 的反应方程式:
的反应方程式:___________ 。
 )中的锂,同时得到有用的磷酸铁(
)中的锂,同时得到有用的磷酸铁( ),其工艺流程如下。回答下列问题:
),其工艺流程如下。回答下列问题:
(1)基态Fe原子的价层电子轨道表达式为
 的电子式为
的电子式为(2)第一次浸出实验在一定条件下,浸出时间和浸出温度对Li、Fe、P的浸出率影响如下图所示。

①考虑实验效率和实际工业生产要求,选择的最佳浸出时间:
②随着浸出温度的上升,一定温度后Li的浸出率呈现下降的趋势,可能的原因为
③滤渣A的主要成分为
(3)除杂时加入NaOH的作用为调节溶液pH,使
 沉淀完全,则调pH不得低于
沉淀完全,则调pH不得低于(已知:
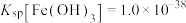 )
)(4)提纯碳酸锂产品时得到的母液的主要成分是
(5)某科研小组探究用磷酸铁锂电池处理含
 的酸性废水,以得到有用的
的酸性废水,以得到有用的 ,其装置如图所示:请写出甲池中生成
,其装置如图所示:请写出甲池中生成 的反应方程式:
的反应方程式:
您最近一年使用:0次
8 . 氯溴酸在医药和石化工业上有广泛用途,模拟工业制备氢溴酸的流程如图所示。下列说法不正确的是
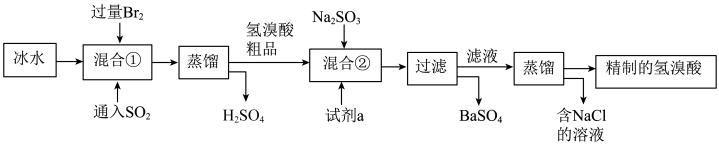

A.混合①使用冰水的目的是防止 和HBr挥发 和HBr挥发 |
B. 可除去氢溴酸粗品中的 可除去氢溴酸粗品中的 ,发生的离子反应为 ,发生的离子反应为 |
| C.蒸馏时,加完“滤液”后,先通冷凝水,再点燃酒精灯加热 |
D.工业氢溴酸常带有淡淡的黄色,可能是因为含有 |
您最近一年使用:0次
名校
解题方法
9 . 某兴趣小组设计如图实验装置制备次磷酸钠( )。
)。
已知:①白磷( )在空气中可自燃,与过量烧碱溶液混合,80~90℃时反应生成
)在空气中可自燃,与过量烧碱溶液混合,80~90℃时反应生成 和
和 。
。
② 是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成
是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成 。
。
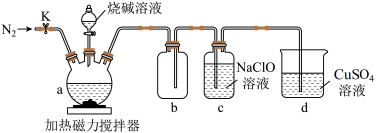
(1)仪器a的名称是___________ 。a中发生反应的化学方程式是___________ 。
(2)仪器b组成的装置的作用是___________ ,检查装置气密性后,应先打开K通入 一段时间,目的是
一段时间,目的是___________ 。
(3)下列有关说法正确的是___________。
(4)①仪器c中充分反应后生成 和NaCl,经过一系列操作可获得固体
和NaCl,经过一系列操作可获得固体 。相关物质的溶解度(S)如下:
。相关物质的溶解度(S)如下:
从下列选项a-g中选择合理的仪器或操作,补全如下步骤。
取仪器c中溶液,用蒸发皿___________ →用___________ (趁热过滤)→用烧杯(冷却结晶)→用漏斗(过滤得到 )→
)→___________ →干燥 粗品。
粗品。
选项:a.溶解 b.过滤 c.洗涤 d.普通三角漏斗 e.保温漏斗
f.蒸发浓缩至有大量晶体析出 g.蒸发浓缩至溶液表面出现晶膜
②写出c中发生反应的离子方程式___________ 。
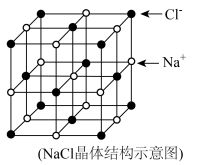
(5)NaCl晶胞结构如图,设距离最近的 间的距离为apm,
间的距离为apm, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为___________  。(列出计算式即可)
。(列出计算式即可)
 )。
)。已知:①白磷(
 )在空气中可自燃,与过量烧碱溶液混合,80~90℃时反应生成
)在空气中可自燃,与过量烧碱溶液混合,80~90℃时反应生成 和
和 。
。②
 是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成
是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成 。
。
(1)仪器a的名称是
(2)仪器b组成的装置的作用是
 一段时间,目的是
一段时间,目的是(3)下列有关说法正确的是___________。
A.次磷酸( )是三元酸 )是三元酸 |
| B.为加快反应速率,投料前应先在通风橱内将白磷碾成薄片状 |
C.反应结束后应继续通入 一段时间,可提高 一段时间,可提高 产率 产率 |
| D.d中所盛硫酸铜溶液可用酸性高锰酸钾溶液代替 |
(4)①仪器c中充分反应后生成
 和NaCl,经过一系列操作可获得固体
和NaCl,经过一系列操作可获得固体 。相关物质的溶解度(S)如下:
。相关物质的溶解度(S)如下: | S(25℃) | S(100℃) | |
| NaCl | 37 | 39 |
 | 100 | 667 |
取仪器c中溶液,用蒸发皿
 )→
)→ 粗品。
粗品。选项:a.溶解 b.过滤 c.洗涤 d.普通三角漏斗 e.保温漏斗
f.蒸发浓缩至有大量晶体析出 g.蒸发浓缩至溶液表面出现晶膜
②写出c中发生反应的离子方程式
(5)NaCl晶胞结构如图,设距离最近的
 间的距离为apm,
间的距离为apm, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为 。(列出计算式即可)
。(列出计算式即可)
您最近一年使用:0次
名校
解题方法
10 . 某火电厂收捕到的粉煤灰的主要成分为 等。研究小组对其进行综合处理的流程如下:
等。研究小组对其进行综合处理的流程如下:

已知:①滤液1中仍有 剩余;
剩余;
②相关金属离子形成氢氧化物沉淀的 范围如下:
范围如下:
请回答下列问题:
(1)滤渣1的主要成分是___________ (填化学式),为了提高粉煤灰浸出速率,在“酸浸”时可采取的措施有___________
(2)流程中加入铁粉“反应”过程的离子方程式为___________ ;怎样判断 沉淀已经洗涤干净,操作是
沉淀已经洗涤干净,操作是___________
(3)加入双氧水调节溶液 时离子方程式为
时离子方程式为___________ ;滤液2应调节 的范围为:
的范围为:___________ 。
(4)滤液3在蒸发结晶制备 时应注意
时应注意___________ 。
 等。研究小组对其进行综合处理的流程如下:
等。研究小组对其进行综合处理的流程如下:
已知:①滤液1中仍有
 剩余;
剩余;②相关金属离子形成氢氧化物沉淀的
 范围如下:
范围如下:| 金属离子 |  |  |  |  |
开始沉淀时 | 7.5 | 2.2 | 3.7 | 8.9 |
完全沉淀时 | 9.0 | 3.2 | 4.7 | 10.9 |
(1)滤渣1的主要成分是
(2)流程中加入铁粉“反应”过程的离子方程式为
 沉淀已经洗涤干净,操作是
沉淀已经洗涤干净,操作是(3)加入双氧水调节溶液
 时离子方程式为
时离子方程式为 的范围为:
的范围为:(4)滤液3在蒸发结晶制备
 时应注意
时应注意
您最近一年使用:0次



