名校
1 . 海洋植物如海带、海藻中含有丰富的碘元素。如图为从海带中提取碘的工业生产过程,有关说法正确的是
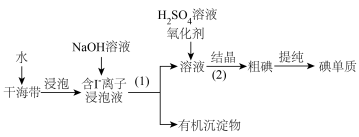
| A.工业上不直接从海水中提取碘是因为海水中碘的总储量很少 |
| B.干海带浸泡液中的碘离子可用淀粉溶液检验 |
| C.操作(1)时,需要用到玻璃仪器有玻璃棒、蒸发皿、酒精灯 |
| D.从海带中提碘的过程中利用了氧化还原反应原理 |
您最近半年使用:0次
2 . 实验室制备柠檬酸铁铵的流程如下:
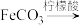 柠檬酸亚铁
柠檬酸亚铁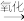 柠檬酸铁
柠檬酸铁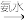 柠檬酸铁铵
柠檬酸铁铵 柠檬酸铁铵晶体
柠檬酸铁铵晶体
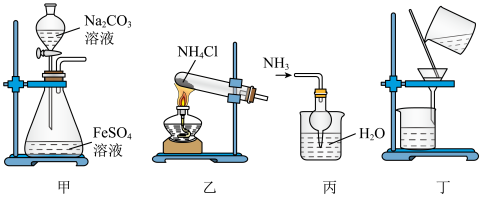
下列实验装置或操作不能 达到实验目的的是
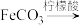 柠檬酸亚铁
柠檬酸亚铁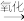 柠檬酸铁
柠檬酸铁 柠檬酸铁铵
柠檬酸铁铵 柠檬酸铁铵晶体
柠檬酸铁铵晶体下列实验装置或操作

A.用装置甲制取 | B.用装置乙制取 |
| C.用装置丙制取氨水 | D.用装置丁分离出柠檬酸铁铵晶体 |
您最近半年使用:0次
解题方法
3 . “海水提碘”的实验中,提取后;可用“反萃取法”萃取、富集碘单质,试剂常用 ,实验步骤,已知:
,实验步骤,已知: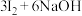 (浓)
(浓)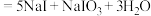 ;酸性条件下
;酸性条件下 和
和 发生归中反应。下面说法错误的是
发生归中反应。下面说法错误的是
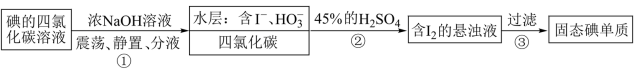
| A.步骤①不可以用酒精作萃取剂 |
| B.分液时有机层从分液漏斗下口放出 |
C.步骤②中发生反应的离子方程式为 |
| D.步骤⑤操作中需要的玻璃仪器为漏斗、烧杯和玻璃棒 |
您最近半年使用:0次
名校
4 . 从干海带中提取碘的实验流程如下,下列有关说法

| A.氧化过程可以用过氧化氢代替氯水 |
B.试剂X可以选择使用NaOH,发生反应为:3I2 + 6OH- = 5I- + IO +3H2O +3H2O |
| C.萃取时可使用无水乙醇代替CCl4以节约成本 |
| D.操作I需要使用到普通漏斗、烧杯和玻璃棒 |
您最近半年使用:0次
5 . 以下实验装置一般不用于分离物质的是
A.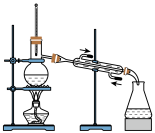 | B. | C.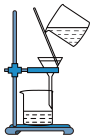 | D.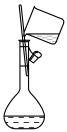 |
您最近半年使用:0次
6 . 我国科学家侯德榜发明了联合制碱法,对世界制碱工业做出了卓越贡献。联合制碱法以氯化钠、氨及二氧化碳为原料,同时生产纯碱和氯化铵两种产品
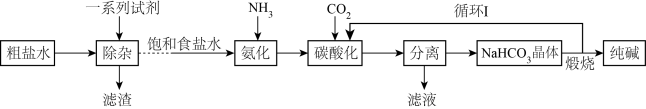
(1)粗盐水中含有Ca2+、 、Mg2+,“除杂”时依次加入过量的NaOH、BaCl2、Na2CO3。加入Na2CO3的目的
、Mg2+,“除杂”时依次加入过量的NaOH、BaCl2、Na2CO3。加入Na2CO3的目的_______ 。在实验室分离出“滤渣”所需的玻璃仪器有玻璃棒、烧杯、_______ 。
(2)“氨化”和“碳酸化”的顺序不能对调,理由是_______ 。在循环1中,参与循环的物质是_______ 。
(3)上述流程中,NaCl转化为NaHCO3的化学方程式_______ 。
(4)根据NaCl和NH4Cl的溶解度曲线(见图),从“滤液”中制得NH4Cl晶体的操作包括_______ 、过滤、洗涤、干燥。

(5)纯碱样品中常含有少量NaHCO3杂质。为测定样品中Na2CO3的质量分数,设计下列三种实验方案。不能达到实验目的的是_______ 。
A.称取a克样品,充分加热后,固体质量减少b克
B.称取a克样品,加入足量稀盐酸。将所得气体通入过量的碱石灰,充分吸收后
C.称取a克样品,加入足量稀盐酸。充分反应后,将所得溶液蒸发结晶

(1)粗盐水中含有Ca2+、
 、Mg2+,“除杂”时依次加入过量的NaOH、BaCl2、Na2CO3。加入Na2CO3的目的
、Mg2+,“除杂”时依次加入过量的NaOH、BaCl2、Na2CO3。加入Na2CO3的目的(2)“氨化”和“碳酸化”的顺序不能对调,理由是
(3)上述流程中,NaCl转化为NaHCO3的化学方程式
(4)根据NaCl和NH4Cl的溶解度曲线(见图),从“滤液”中制得NH4Cl晶体的操作包括

(5)纯碱样品中常含有少量NaHCO3杂质。为测定样品中Na2CO3的质量分数,设计下列三种实验方案。不能达到实验目的的是
A.称取a克样品,充分加热后,固体质量减少b克
B.称取a克样品,加入足量稀盐酸。将所得气体通入过量的碱石灰,充分吸收后
C.称取a克样品,加入足量稀盐酸。充分反应后,将所得溶液蒸发结晶
您最近半年使用:0次
7 . 以废旧锂离子电池正极材料(主要成分为镍钴锰酸锂,还有少量镁铝合金和含铁化合物)为原料,回收 、
、 、
、 的过程可表示为:
的过程可表示为:
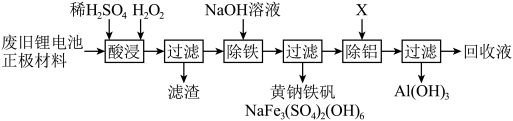
(1)“酸浸”时,三价镍、三价钴、四价锰转化为 、
、 、
、 进入溶液,则在该过程中
进入溶液,则在该过程中 是
是_______ (填“氧化剂”或“还原剂”)。保持其他条件相同,搅拌相同时间,测得60℃时镍、钴、锰的浸出率最大:温度既不能过低也不能过高的可能原因是________ 。
(2)“过滤”时所用到的玻璃仪器有烧杯、________ 。
(3)“除铁”时加入 溶液控制溶液的
溶液控制溶液的 为1.5~1.8,则
为1.5~1.8,则 转化为黄钠铁矾[
转化为黄钠铁矾[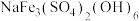 ]沉淀的离子方程式是
]沉淀的离子方程式是________ 。
(4)回收液可用于合成锂离子电池正极材料,合成前需测定其中 等离子的浓度。
等离子的浓度。
测定原理:用过量标准 溶液氧化经预处理的回收液样品中的
溶液氧化经预处理的回收液样品中的 ,再用标准
,再用标准 溶液滴定过量的
溶液滴定过量的 溶液。反应方程式为:
溶液。反应方程式为: 。
。
测定过程:取预处理后的回收液样品20.00mL,向其中加入:20.00mL
 溶液,充分反应;再用
溶液,充分反应;再用
 溶液滴定反应后的溶液,消耗
溶液滴定反应后的溶液,消耗 溶液12.00mL。
溶液12.00mL。
计算预处理后的回收液样品中 的物质的量浓度
的物质的量浓度_______ 。(写出计算过程)
 、
、 、
、 的过程可表示为:
的过程可表示为:
(1)“酸浸”时,三价镍、三价钴、四价锰转化为
 、
、 、
、 进入溶液,则在该过程中
进入溶液,则在该过程中 是
是(2)“过滤”时所用到的玻璃仪器有烧杯、
(3)“除铁”时加入
 溶液控制溶液的
溶液控制溶液的 为1.5~1.8,则
为1.5~1.8,则 转化为黄钠铁矾[
转化为黄钠铁矾[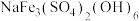 ]沉淀的离子方程式是
]沉淀的离子方程式是(4)回收液可用于合成锂离子电池正极材料,合成前需测定其中
 等离子的浓度。
等离子的浓度。测定原理:用过量标准
 溶液氧化经预处理的回收液样品中的
溶液氧化经预处理的回收液样品中的 ,再用标准
,再用标准 溶液滴定过量的
溶液滴定过量的 溶液。反应方程式为:
溶液。反应方程式为: 。
。测定过程:取预处理后的回收液样品20.00mL,向其中加入:20.00mL

 溶液,充分反应;再用
溶液,充分反应;再用
 溶液滴定反应后的溶液,消耗
溶液滴定反应后的溶液,消耗 溶液12.00mL。
溶液12.00mL。计算预处理后的回收液样品中
 的物质的量浓度
的物质的量浓度
您最近半年使用:0次
名校
8 . 实验室以水泥厂的废料(主要成分为MgO,含少量MnO、 、FeO、
、FeO、 、
、 等杂质)为原料制备
等杂质)为原料制备 的实验流程如下:
的实验流程如下:
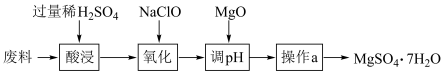
下列与流程相关的装置或操作正确且能达到实验目的的是

 、FeO、
、FeO、 、
、 等杂质)为原料制备
等杂质)为原料制备 的实验流程如下:
的实验流程如下:
下列与流程相关的装置或操作正确且能达到实验目的的是

| A.可在装置甲中进行“酸浸”操作 |
B.按图乙所示操作检验“氧化”步骤中 是否完全氧化 是否完全氧化 |
| C.用装置丙过滤“调pH”后所得悬浊液 |
D.用装置丁加热烘干 晶体 晶体 |
您最近半年使用:0次
2024-02-26更新
|
389次组卷
|
2卷引用:江苏省南京市2023-2024学年高二下学期期初学业质量调研化学试卷
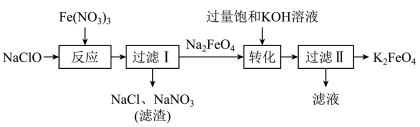
9 . 高铁酸钾( )能溶于水,微溶于浓
)能溶于水,微溶于浓 溶液,难溶于无水乙醇,低温碱性条件下比较稳定。工业上湿法制备
溶液,难溶于无水乙醇,低温碱性条件下比较稳定。工业上湿法制备 的流程如下,下列说法不正确的是
的流程如下,下列说法不正确的是
 )能溶于水,微溶于浓
)能溶于水,微溶于浓 溶液,难溶于无水乙醇,低温碱性条件下比较稳定。工业上湿法制备
溶液,难溶于无水乙醇,低温碱性条件下比较稳定。工业上湿法制备 的流程如下,下列说法不正确的是
的流程如下,下列说法不正确的是
| A.“过滤I”中用到的玻璃仪器有分液漏斗、玻璃棒、烧杯 |
| B.“反应”中,氧化剂和还原剂的物质的量之比为3:2 |
C.“转化”能进行说明该条件下 的溶解度小于 的溶解度小于 |
D.“过滤Ⅱ”所得 晶体可用无水乙醇洗涤 晶体可用无水乙醇洗涤 |
您最近半年使用:0次

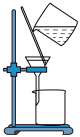
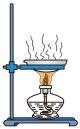

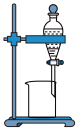
 沉淀和溶液
沉淀和溶液