1 . 碲被誉为金属性最强的非金属,某科研小组从碲渣(主要含有Cu2Te )中提取粗碲的工艺流程如图所示。下列有关说法错误的是
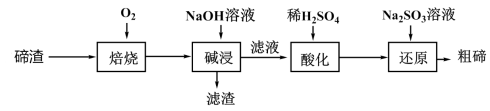
| A.“焙烧”后铜以Cu2O形式存在 |
| B.“碱浸”后过滤用到的主要仪器有:烧杯、漏斗、玻璃棒 |
| C.“酸化”后生成Te(SO4)2 |
| D.“还原”后,溶液的酸性减弱 |
您最近半年使用:0次
2 . 市售食用油中常添加叔丁基对苯二酚(TBHQ)作抗氧化剂。实验室制备TBHQ的原理:
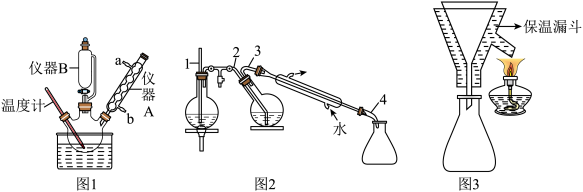
①在下图1装置的三颈烧瓶中依次加入1.1 g对苯二酚、8 mL 85%磷酸和10 mL甲苯。
②用热水浴加热使反应瓶中混合物升温至90℃,用滴管向反应瓶中分批滴加1 mL叔丁醇(密度为0.775 g·cm ),控制温度在90~95℃搅拌20 min,直至混合物中的固体全部溶解。
),控制温度在90~95℃搅拌20 min,直至混合物中的固体全部溶解。
③趁热将反应物转入分液漏斗中,分出磷酸层,向有机层加入10 mL水,进行水蒸气蒸馏,如下图2。蒸馏完毕,将剩余物趁热过滤,弃去不溶物,如下图3所示。滤液转入烧杯中,若剩余液体体积不足10 mL,应补加热水,使产物被热水所提取。
④将滤液在冰浴中冷却,析出白色晶体,抽滤,并用少量冷水洗涤两次,在氮气中干燥。得到1 g产品。
回答下列问题:
(1)仪器B的名称是______ ,三颈烧瓶宜选择的规格是______ (填标号)。
A.50mL B.100mL C.200mL D.500mL
(2)本实验中甲苯的作用是______ ,步骤②中分批加入叔丁醇的目的是____________ 。
(3)步骤③中用水蒸气蒸馏的目的是____________ ,蒸馏终点的现象是____________ 。
(4)步骤③趁热过滤的目的是____________ 。
(5)如果上图3锥形瓶内壁有白色晶体析出,需采取的措施是____ 。步骤④“在氮气中干燥”的优点是____ 。
(6)TBHQ的产率为______ (保留3位有效数字)%。
 +(CH3)3COH
+(CH3)3COH
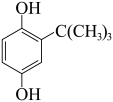 +H2O
+H2O
①在下图1装置的三颈烧瓶中依次加入1.1 g对苯二酚、8 mL 85%磷酸和10 mL甲苯。
②用热水浴加热使反应瓶中混合物升温至90℃,用滴管向反应瓶中分批滴加1 mL叔丁醇(密度为0.775 g·cm
 ),控制温度在90~95℃搅拌20 min,直至混合物中的固体全部溶解。
),控制温度在90~95℃搅拌20 min,直至混合物中的固体全部溶解。③趁热将反应物转入分液漏斗中,分出磷酸层,向有机层加入10 mL水,进行水蒸气蒸馏,如下图2。蒸馏完毕,将剩余物趁热过滤,弃去不溶物,如下图3所示。滤液转入烧杯中,若剩余液体体积不足10 mL,应补加热水,使产物被热水所提取。
④将滤液在冰浴中冷却,析出白色晶体,抽滤,并用少量冷水洗涤两次,在氮气中干燥。得到1 g产品。
| 物质 | 甲苯 | 对苯二酚 | 2—叔丁基对苯二酚 | 磷酸 | 甲苯—水共沸物 |
| 熔点/℃ | -94 | 175.5 | 128 | 42.35 | |
| 沸点/℃ | 110.63 | 286 | 295 | 213 | 84.1 |
(1)仪器B的名称是
A.50mL B.100mL C.200mL D.500mL
(2)本实验中甲苯的作用是
(3)步骤③中用水蒸气蒸馏的目的是
(4)步骤③趁热过滤的目的是
(5)如果上图3锥形瓶内壁有白色晶体析出,需采取的措施是
(6)TBHQ的产率为
您最近半年使用:0次
3 . 屠呦呦等科学家受东晋葛洪的《肘后备急方》中记载:“青蒿一握,以水二升渍。绞取汁,尽服之……”可治疟疾的启发用易挥发的乙醚提取青蒿有效成分,最终分离出一种无色结晶,并命名为青蒿素。下列说法错误的是
| A.“以水二升渍,绞取汁”涉及到的分离操作是萃取、过滤 |
| B.用“水渍、绞汁”替代“水煎”说明青蒿素高温会被破坏 |
| C.乙醚的作用与水相同,但沸点比水高 |
| D.青蒿素的溶解度:乙醚中>水中 |
您最近半年使用:0次
名校
解题方法
4 .  是生活中常用的消毒剂。工业制备方法之一为
是生活中常用的消毒剂。工业制备方法之一为
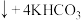 ,下列叙述正确的是
,下列叙述正确的是
 是生活中常用的消毒剂。工业制备方法之一为
是生活中常用的消毒剂。工业制备方法之一为
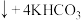 ,下列叙述正确的是
,下列叙述正确的是A. 是该反应的催化剂 是该反应的催化剂 |
| B.氧化剂、还原剂的物质的量之比为2∶1 |
C.锰酸钾在水中的电离方程式: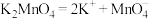 |
D.实验结束,可以采用“过滤”操作分离出 |
您最近半年使用:0次
2024-03-22更新
|
85次组卷
|
2卷引用:辽宁省朝阳市建平县实验中学2023-2024学年高一上学期2月期末化学试题
名校
解题方法
5 . 盐湖卤水(主要含Na+、Mg2+、Li+、Cl-、 和硼酸根等)是锂盐的重要来源。一种以高镁卤水为原料经两段除镁制备
和硼酸根等)是锂盐的重要来源。一种以高镁卤水为原料经两段除镁制备 的工艺流程如图:
的工艺流程如图:
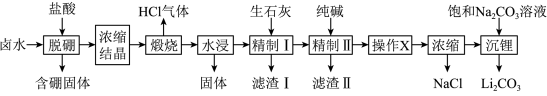
已知:常温下, 。相关化合物的溶解度与温度的关系如图所示。
。相关化合物的溶解度与温度的关系如图所示。

回答下列问题:
(1)含硼固体中的B(OH)3在水中存在平衡: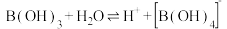 (常温下,
(常温下, );B(OH)3与
);B(OH)3与 溶液反应可制备硼砂
溶液反应可制备硼砂 。常温下,在
。常温下,在 硼砂溶液中,
硼砂溶液中,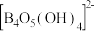 水解生成等物质的量浓度的B(OH)3和
水解生成等物质的量浓度的B(OH)3和 ,该水解反应的离子方程式为
,该水解反应的离子方程式为___________ ,该溶液pH=___________ 。
(2)滤渣Ⅰ的主要成分是___________ (填化学式);精制Ⅰ后溶液中Li+浓度为 ,则常温下精制Ⅱ过程中
,则常温下精制Ⅱ过程中 浓度应控制在
浓度应控制在___________  以下。若脱硼后直接进行精制Ⅰ,除无法回收HCl外,还将增加
以下。若脱硼后直接进行精制Ⅰ,除无法回收HCl外,还将增加___________ 的用量(填化学式)。
(3)精制Ⅱ的目的是___________ ;进行操作X时应选择的试剂是___________ 。
 和硼酸根等)是锂盐的重要来源。一种以高镁卤水为原料经两段除镁制备
和硼酸根等)是锂盐的重要来源。一种以高镁卤水为原料经两段除镁制备 的工艺流程如图:
的工艺流程如图:
已知:常温下,
 。相关化合物的溶解度与温度的关系如图所示。
。相关化合物的溶解度与温度的关系如图所示。 
回答下列问题:
(1)含硼固体中的B(OH)3在水中存在平衡:
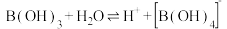 (常温下,
(常温下, );B(OH)3与
);B(OH)3与 溶液反应可制备硼砂
溶液反应可制备硼砂 。常温下,在
。常温下,在 硼砂溶液中,
硼砂溶液中,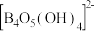 水解生成等物质的量浓度的B(OH)3和
水解生成等物质的量浓度的B(OH)3和 ,该水解反应的离子方程式为
,该水解反应的离子方程式为(2)滤渣Ⅰ的主要成分是
 ,则常温下精制Ⅱ过程中
,则常温下精制Ⅱ过程中 浓度应控制在
浓度应控制在 以下。若脱硼后直接进行精制Ⅰ,除无法回收HCl外,还将增加
以下。若脱硼后直接进行精制Ⅰ,除无法回收HCl外,还将增加(3)精制Ⅱ的目的是
您最近半年使用:0次
2024-03-14更新
|
471次组卷
|
2卷引用:辽宁省沈阳市东北育才学校2023-2024学年高三下学期第六次模拟考试化学试卷
名校
解题方法
6 . 从干海带中提取碘的实验流程如下:
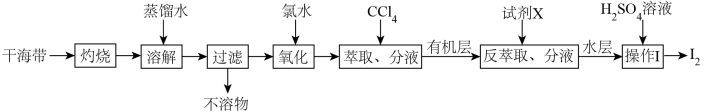
下列说法错误的是

下列说法错误的是
| A.氧化步骤中氯水可用过氧化氢代替 |
B.试剂X可以为 ,反萃取的离子方程式为: ,反萃取的离子方程式为: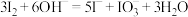 |
C. 可循环利用以有效提高干海带提碘的产率 可循环利用以有效提高干海带提碘的产率 |
| D.操作Ⅰ要用到普通漏斗、烧杯和玻璃棒 |
您最近半年使用:0次
2024-01-28更新
|
543次组卷
|
4卷引用:辽宁省五校联考2023-2024学年高三上学期期末考试化学试题
7 . 工业上可通过“酸性歧化法”制备KMnO4:将软锰矿(主要成分为MnO2)先氧化成K2MnO4,进而在酸性条件下制备KMnO4,流程如下图所示。实验室中模拟“酸性歧化法”制备KMnO4下列说法正确的是

| A.“熔融”操作应在石英坩埚中进行 |
| B.“酸化”反应中氧化产物与还原产物的物质的量之比为2:1 |
| C.“酸化”时可改用盐酸代替CO2 |
| D.“结晶”过程中加热蒸发至有较多晶体析出时停止加热 |
您最近半年使用:0次
8 . 从酸性含铬废水(主要阴离子为 )中回收铬元素(
)中回收铬元素( )的部分工艺流程如图所示。
)的部分工艺流程如图所示。
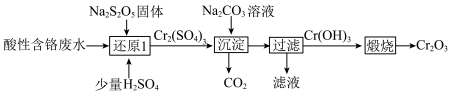
下列有关说法正确的是
 )中回收铬元素(
)中回收铬元素( )的部分工艺流程如图所示。
)的部分工艺流程如图所示。
下列有关说法正确的是
| A.“过滤”时需用玻璃棒搅拌 |
| B.“煅烧”过程中发生了氧化还原反应 |
C.若分别用 、 、 还原等量的 还原等量的 ,消耗 ,消耗 与 与 的物质的量之比为1∶3 的物质的量之比为1∶3 |
D.“还原1”时反应的离子方程式为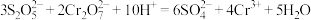 |
您最近半年使用:0次
2024-01-08更新
|
250次组卷
|
6卷引用:辽宁省阜新市高级中学2023-2024学年高一上学期12月月考化学试题
9 . 下列装置与对应操作正确的是
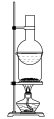 | 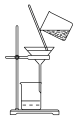 | 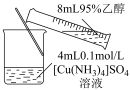 |  |
A.碘晶体(含 )的提纯 )的提纯 | B.分离苯酚和水的混合物 | C.析出 晶体 晶体 | D.测定 溶液的浓度 溶液的浓度 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-12-27更新
|
874次组卷
|
3卷引用:辽宁省沈阳市东北育才学校2023-2024学年高三下学期第六次模拟考试化学试卷
10 . 《本草纲目》中记载了粗食盐的一种制作过程:“取盐于池旁耕地沃以池水,每得南风急,则宿夕成盐。”若将粗食盐在实验室提纯,不涉及的操作是
| A.溶解 | B.蒸发 | C.过滤 | D.蒸馏 |
您最近半年使用:0次
2023-11-29更新
|
2373次组卷
|
3卷引用:辽宁省鞍山市普通高中2023-2024学年高三上学期期末联考化学试题



